1月24日,《柳叶刀-微生物》(The Lancet Microbe)刊登了题为《Safety and immunogenicity of the SARS-CoV-2 ARCoV mRNA vaccine in Chinese adults: a randomized, double-blind, placebo-controlled, phase 1 trial》的报告,正式公布了新冠mRNA疫苗ARCoVaX(ARCoV)的I期临床试验数据。值得一提的是,ARCoVaX也是国内首个进入临床试验的mRNA新冠疫苗。
ARcoVax由中国人民解放军军事科学院军事医学研究院、艾博生物与沃森生物共同研制,由脂质纳米粒(LNPs) 包裹,靶向SARS-CoV-2棘突蛋白RBD区域。研究结果显示,100μg剂量可诱导高水平中和抗体,1000μg剂量无明显的不良反应,单剂或两剂ARCoVaX免疫可在小鼠和非人类灵长类动物中激发抗多种流行SARS-CoV-2毒株的强大抗体和T细胞应答。
此次柳叶刀公布的是ARCoVaX在浙江省杭州市树兰医院进行的一项单中心、双盲、随机、安慰剂对照的 I 期临床试验结果,试验旨在评估其在新冠病毒spike蛋白受体结合域(RBD)的的初步安全性、耐受性和免疫原性。
在2020年10月30日至12月2日期间,共有120名18-59岁新冠病毒感染阴性的健康成年人参与试验。受试者随机分为6组( 5 个剂量水平+安慰剂组),剂量水平分别为 5 μg、10μg、15μg、20μg、25 μg。所有受试者都接种了第一剂疫苗,118人接种了第二剂疫苗。
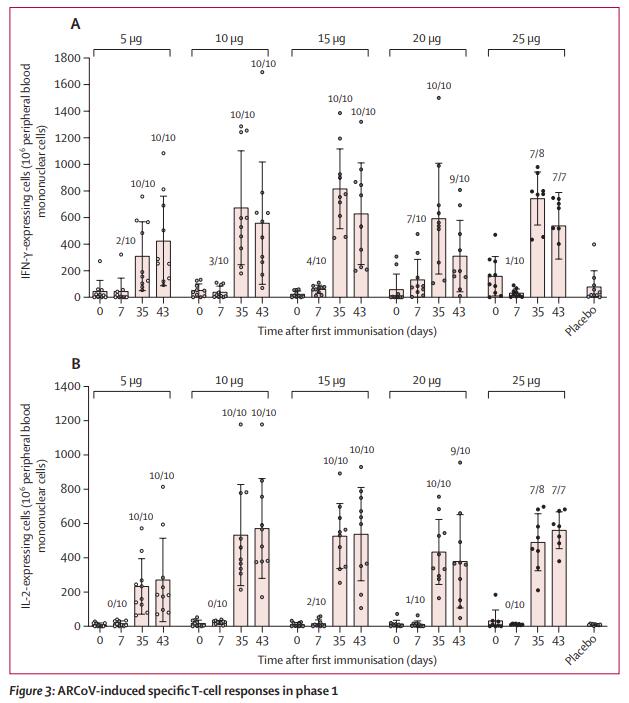
中和抗体滴度方面,第二次接种后的第7天,RBD抗体(IgG)和中和抗体等体液免疫反应显着增加,并在第14-28天内达到峰值。特异性T细胞反应在完全接种(两针接种)后7-14天达到高峰。其中,15μg诱导了最高滴度的中和抗体,约为COVID-19恢复期患者的2倍,而20μg、25μg组中和抗体水平则与低剂量组表现类似。
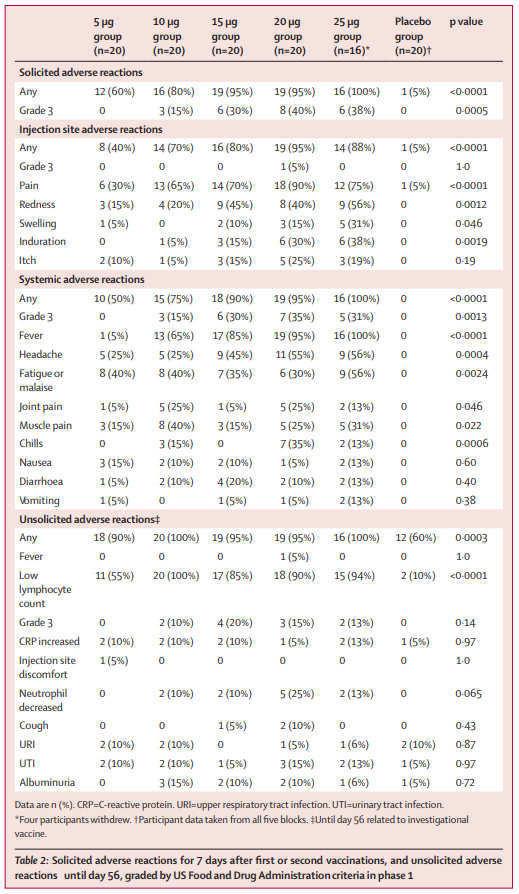
安全性方面,接种后56天内无严重不良反应事件,且大多数不良事件为轻度或中度,其中最常见不良反应为发热,按美国FDA标准,这一反应在5 μg、10μg、15μg、20μg、25 μg剂量组的比例为分别为5%(1/20)、65%(13/20)、85%(17/20)、95%(19/20)、100%(16/16),发生率与辉瑞的 mRNA 疫苗相似。同时,所有受试者在接种疫苗后2天内发烧消退,ARCoV疫苗第一次接种和第二次接种造成的不良事件发生率相似。
报告显示,以上数据皆提示ARcoVax疫苗在5种剂量下均显示了安全性和良好的耐受性,并能诱导强烈的体液和细胞免疫反应。此结果也为疫苗未来做更大规模的临床试验奠定了基础。
目前,艾博生物已于2021年7月启动了ARCoVaX的国内III期临床试验,于2021年9月启动了ARCoVaX的国际多中心III期临床试验,并于2021年11月获得了新冠mRNA疫苗《药品生产许可证》。
当前全球已上市两款mRNA疫苗,包括辉瑞/BioNTech的BNT162b2,以及Moderna的mRNA-1273,国内方面目前获得临床批件的厂商包括艾博生物、斯微生物和丽凡达生物,其中艾博生物进入临床Ⅲ期。此外,7月14日,复星医药透露其与BioNTech合作的mRNA新冠疫苗进入行政审批阶段的消息。
为你推荐
 资讯
资讯 两款IgA肾病新药获批
6月9日,荣昌生物发布公告称,近日,荣昌生物制药(烟台)股份有限公司收到国家药品监督管理局(NMPA)核准签发的《药品注册证书》,泰它西普注射液(代号:RC18)治疗免疫球蛋...
2026-06-09 11:33
 资讯
资讯 第五年,2026年纠正医药购销领域和医疗服务中不正之风工作要点
《通知》围绕年度重点任务和既往工作中发现的突出问题,聚焦重点领域和关键环节,在坚持党建引领行风、强化医德医风建设、加强正向宣传引导、防范化解风险隐患、严守医疗数据安...
2026-06-09 09:14
 资讯
资讯 华超神控完成亿元天使系列融资,自研 AI 超声脑机平台开辟无创深脑调控新赛道
本轮融资分为天使轮与天使 + 轮两期,天使轮由经纬创投独家领投,天使 + 轮由德联资本、道远资本联合领投,行业知名机构持续加注,循光资本担任本次系列融资独家财务顾问。
2026-06-08 17:05
 资讯
资讯 Cytiva与鼎康生物合作GMP-2扩建项目投产, 共筑“中国速度,全球交付”新标杆
GMP-2生产基地专为临床后期及商业化生产打造,可为全球生物药合作伙伴提供灵活且可扩展的生产解决方案,助力加速产品商业化进程并保障全球稳定供应。
2026-06-08 16:41
 资讯
资讯 默沙东欣瑞来(注射用索特西普)重磅上市,引领肺动脉高压(PAH)迈向“治本” 新里程碑
用于治疗世界卫生组织功能分级(WHO FC)Ⅱ-Ⅲ级的肺动脉高压(PAH,WHO第1组)成年患者
2026-06-08 16:36
 资讯
资讯 GCP2026修订版发布,2020版废止
6月8日,国家药监局、国家卫生健康委、国家中医药局、国家疾控局联合发布《药物临床试验质量管理规范(2026年修订)》,自2026年9月1日起施行。国家药监局、国家卫生健康委《关...
2026-06-08 16:21
 资讯
资讯 博腾股份终止斯洛文尼亚研发生产基地建设,保留对诺华子公司主张索赔的权利
近日,博腾股份公告称,鉴于诺华斯洛文尼亚子公司已向博腾股份全资子公司PSI发出解除通知,PSI在该场地内的投资和建设已面临重大不确定性,公司决定终止投资建设斯洛文尼亚研发...
2026-06-08 13:10
 资讯
资讯 全球首款CD7 CAR-T儿童适应症一期临床启动
据安科生物和博生吉医药消息,安科生物参股公司博生吉医药自主研发的全球首款进入临床阶段的靶向CD7自体CAR-T产品PA3-17儿童适应证临床试验启动会在组长单位中国医学科学院血液...
2026-06-08 10:57
 资讯
资讯 一家医疗器械企业被调入港股通
6月5日收市,上海证券交易所官网发布最新港股通标的调整通知,共6家企业调入,包括广受关注的大模型企业智谱(02513 HK)、GPU企业壁仞科技(06082 HK)等,其中生物医药、医...
2026-06-07 21:20
 资讯
资讯 第二批全国中药饮片集采首轮报价结果公示
6月5日深夜,山东省医保局官网发布《全国中药饮片联盟集中采购拟入围结果公示》,共计822家企业入围,与资格审核通过企业数量相比,淘汰了约20%企业。
2026-06-07 13:11
 资讯
资讯 全国首例,侵入式脑机接口让视障患者复明临床试验取得重大突破
6月6日,记者从中南大学湘雅医院了解到,由许惠卓教授团队牵头开展的侵入式脑机接口视觉重建临床试验取得突破性进展。失明多年的受试者在术后恢复良好,已初步实现视觉功能重建。
2026-06-06 17:54
 资讯
资讯 国家药监局批准第四代BTK抑制剂洛布替尼片
近日,国家药品监督管理局通过优先审评审批程序,附条件批准广州麓鹏制药有限公司申报的1类创新药洛布替尼片(商品名:麓可达)上市,该药适用于既往接受过至少两种系统性治疗(...
2026-06-05 15:07
 资讯
资讯 开盘大涨 50.22%!抗过敏创新药企上市首日受热捧
6 月 5 日,天辰生物医药(苏州)股份有限公司(证券简称:天辰生物 - B,股票代码:01779 HK)正式于香港联合交易所挂牌上市,依托港股 18A 生物科技企业上市规则登陆资本市场。
2026-06-05 14:30
 资讯
资讯 百度健康AI智慧门诊落地中科大附一院,已规模覆盖近二十家三甲医院
6月5日,百度健康与中国科学技术大学附属第一医院(以下简称“中科大附一院”)正式达成战略合作。双方将围绕AI智慧门诊、医生IP打造、全病
2026-06-05 14:20
 资讯
资讯 出海BD宣布后落地的细节
自2024年以来,出海、BD已成为创新药企响亮的名片。相关数据现实,2025年中国创新药对外授权交易总金额超过1300亿美元,近期又有恒瑞医药与BMS、信达生物与辉瑞、云顶新耀与TVTX...
2026-06-05 09:28
 资讯
资讯 徕卡生物科技与 CellCarta 拓展伴随诊断合作开发模式,加速全球商业化进程
该合作模式旨在适应生物制药企业多样化的研发需求,通过紧密协作与并行推进,建立灵活的全球伴随诊断(CDx)开发框架,助力项目从早期检测开发到商业化诊断的更高效转化。
2026-06-04 19:39
 资讯
资讯 瀚森制药双靶点GLP-1减重产品上市申请获受理
瀚森制药今日发布公告,公司创新药奥莱泊肽注射液上市许可申请(NDA)获中国国家药品监督管理局(NMPA)受理,适用于肥胖或超重成人,奥莱泊肽是一款瀚森制药自主研发的每周一次给药...
2026-06-04 13:40
 资讯
资讯 中国生物技术发展中心:抗原特异性免疫细胞激活新技术临床研究备案指引(第1版)
本指引所指的抗原特异性免疫细胞激活新技术是指将不同类型的抗原或抗原载体注射到人体, 经过抗原递呈细胞识别、 吞噬、 加工处理等过程, 诱导机体内产生抗原特异性的免疫...
2026-06-04 10:54