近年来,真实世界研究如过江之鲫、热度愈涨。真实世界研究最初仅被定位为满足上市后药物安全相关的监管要求,至今突破层层限制,越来越被广泛应用于医疗健康行业。自2016年12月美国公布《21世纪治愈法案》以来,探索利用真实世界证据支持已上市药品的新适应症批准,以及上市后研究需求已经成为可能。我国关于真实世界研究的起步较晚,但也陆续发布《真实世界证据支持药物研发与审评的指导原则(试行)》、《用于产生真实世界证据的真实世界数据指导原则(试行)》(2021)等文件,为药物研发给出明确的信号和政策保障。
国内外政策的大力支持,让企业纷纷布局,相应的联盟、协会和平台中心应运而生,真实世界研究市场热闹非凡,风头无两。但不可否认的是,一切才刚刚开始,产业发展依然面临诸多技术和伦理的挑战,数据质量、合规问题、临床可靠性等均是行业发展的掣肘。
联仁健康医疗大数据科技股份有限公司
联仁健康医疗大数据科技股份有限公司(以下简称“联仁健康”)作为健康医疗大数据独角兽企业,具备省级单位的区域医疗健康数据合规运营资质,基于多年数据科技能力沉淀,以区域数据平台为载体,进行深度的数据挖掘、清洗和分析,持续探索临床有效性、患者管理新模式等领域,实现数据医学价值挖掘放大以及商业价值延伸。在“数据二十条”政策背景激励和创新型国有企业市场化条件下,激活医疗数据要素赋能新药开发和上市后再评价方面,联仁健康形成了一条运营合规、数据安全、价值明确、持续赋能的垂直领域“数商”通路。
良莠不齐,真实世界研究的数据之困
真实世界研究是起源于实用性的临床试验,以患者为中心,特点是在较大的样本量基础上,集中挖掘出信息,同时还节约了临床研究成本。这当中,真实世界研究数据质量的控制是确保研究真实性、准确性和可靠性的关键,只有满足适用性的真实世界数据才有可能产生真实世界证据,从而辅助临床研发和医学决策。但是在实际研究过程中常常面临着数据质量、数据编码差异问题、院外的数据缺失等众多问题,导致结果呈现偏倚和混杂;同样的研究样本量大、数据异构性强,易缺失变量,使得研究证据适用性、科学性及可解释性等受到挑战。
面对这些问题,大数据企业的涉足将发挥重要作用,不仅高效完成数据治理,还能实现多场景、多组学、多维度的数据互联互通。
大有可为,大数据公司的优势所在
医疗健康大数据行业的壁垒建立在关注患者全生命周期、数据全方位运营的基础上,从早期数据集采的接口管控,中期医学自然语言知识体系建立,到后期应用于真实世界研究,每一个环节有的放矢的布局得以提供高质量的真实世界研究服务。简单来说,数据、治理、人才形成了大数据公司布局真实世界研究的核心优势。
就联仁健康而言,通过搭建海量规模数据库和多种数据治理模型,涵盖数据汇治用的全链路闭环流程,以临床研究场景需求为导向,最大程度保障数据的可溯源性和透明性。此外,联仁健康采用医工结合的数据专项治理和分析,按照相关法规监管要求,实现对原始数据的保留和精准提取;基于自研疾病模型和医学知识体系,以信息拆分与本体识别、多疾病与肿瘤形态学混合识别等前沿技术为擎,进行智能编码和计算决策,自动填充数据缺失值,实现变量归一化、文本结构化和数据完整化,保障数据关联性、准确性和时效性。截至目前,联仁健康运营区域数据中心覆盖总人口超1亿;覆盖医疗机构超千家,汇聚成数据湖,能够较为全面反映真实世界诊疗状况。
可以说,从数据中发现临床实践差异,并从差异中洞见医学策略是使药械产品生命周期健康可持续发展的最优选择。
俯拾即是,真实世界研究应用丰富
目前业内普遍认为,真实世界研究可以为临床证据添砖加瓦,像是指导临床研究设计,参与外部对照的单臂试验以及解决临床试验运营问题等。不光如此,还可以为医药企业运营细分市场提供足够的决策依据,助力系统掌握产品的适应症和临床用药特点,为药物进一步推广提供有效信息和获取更多研究收益。
基于丰富的大数据治理经验,联仁健康深入数据临床价值,提供回顾性和前瞻性真实世界研究所需的高质量数据、智能化工具和专业人员支撑,已开展多项药械临床价值和药物经济学研究。
值得一提的是,联仁健康现与多家国内外知名药企合作,成功在多个疾病领域给出了大数据解决方案并实现快速交付,例如:肿瘤领域的原发性肝癌治疗现状、膀胱癌患者旅程、乳腺肿瘤恶性影响因素分析,脑血管病领域的急性缺血性脑卒中患者现状分析,自身免疫领域的重度哮喘预研究,罕见病领域的运动神经元病诊治旅程等诸多成功案例。通过对自营数据和外采数据的治理应用,联仁健康不断拓展医疗数据服务药企业务能力边界,挖掘医疗产品使用的真实世界证据,提升药企核心竞争力。
膀胱癌患者旅程
具体来看真实世界研究的应用落地,在危险因素探索场景中,联仁健康陆续开展了多项真实世界研究。其中,联仁健康协助某跨国药企进行早产儿唿吸衰竭治疗失败的危险因素分析,进行数据的汇聚、治理和分析,完成可视化数据展示,对一系列结果进行研讨和再研究:对患有唿吸衰竭的早产儿人口学基数特征进行描述,分析早中晚期早产儿唿吸衰竭的治疗模式,寻找治疗失败的危险因素;并拟公开发表高水平论文,收获医学科研价值。
以探索上市药品新适应症场景为例,联仁健康与国内头部创新药企合作,协助完成FGFR抑制剂产品相关的临床研究,探索其在其他肿瘤领域的有效性和安全性。联仁健康通过远程数据录入的创新数据采集方式,配以OCR辅助录入和人工校验结合的数据汇聚方式,实现7个瘤种方向在10家中心的同步开展,覆盖共计200例FGFR突变肿瘤的患者信息统计和分析,为客户开展营销推广提供了重要的临床证据。
总而言之,随着大数据技术的不断完善和指导原则的日趋成熟,真实世界研究必会在病因诊断、治疗、预后、随访及临床预测等多元场景发挥更大价值。
随着各类医疗信息系统、数据采集系统的建设和广泛应用,真实世界数据产生的渠道和路径在近几年得到长足发展,数据质量和可及性也随之改善。未来,联仁健康将持续赋能真实世界研究,提供数据技术服务,支撑来源于多个渠道的真实世界数据,转化为可溯源、满足研究需求的真实世界证据,促进新药开发降本增速,推动生命科学产业往更高标准发展,构建智慧健康新生态。
来源:医谷网
为你推荐
 资讯
资讯 我武生物撤回人脐带间充质干细胞II型注射液IND申请,需完善部分药学研究
我武生物今日发布公告称,公司间接控股子公司浙江我武干细胞科技有限公司撤回“人脐带间充质干细胞II型注射液”药物临床试验申请。
2026-06-11 17:01
 资讯
资讯 GSK十多年来最大一笔交易,106亿美元收购Nuvalent
当地时间6月9日,葛兰素史克(GSK)宣布与Nuvalent达成收购协议,将在10个工作日内以每股124美元的价格现金收购后者所有A类和B类普通股。此次交易的总股本价值估计为106亿美元(...
2026-06-11 16:11
 资讯
资讯 晶泰控股与一家国际知名药企达成超4亿美元AI药物研发合作
6月10日,晶泰控股发布公告称,公司与一家国际知名生物制药公司达成战略合作。双方将针对一个GPCR(G蛋白偶联受体)靶点,共同开发具备同类最佳(Best-in-Class)潜力的创新口服...
2026-06-11 15:55
 资讯
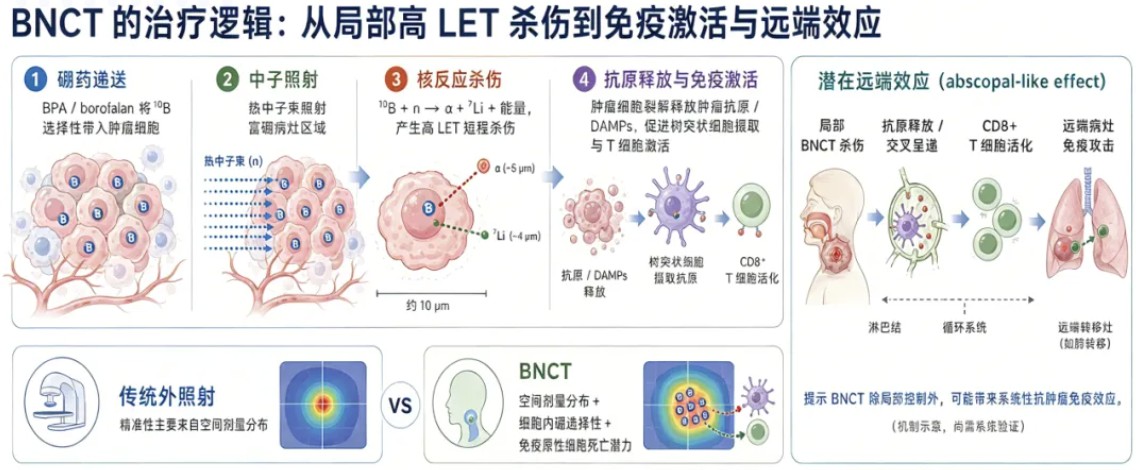
资讯 国产硼药联合国产BNCT设备I期临床治疗后30天观察期结束,预计今年第三季度将启动II期临床
本次试验采用普利制药的注射用硼[10B]法仑及国科中子的BNCT治疗系统,旨在系统评估该方案治疗复发性头颈部恶性肿瘤的安全性、有效性,并开展药代动力学研究。试验于2025年7月正...
2026-06-11 15:29
 资讯
资讯 国家药监局今日批准四款创新药物上市
中山康方生物医药有限公司申报的古莫奇单抗注射液(商品名:奇佑康)上市,用于治疗适合接受系统治疗或光疗的中度至重度斑块状银屑病成人患者。
2026-06-11 15:17
 资讯
资讯 这家药企停牌,ST,面临退市风险
6月10日晚间,湖南南新制药(688189 SH)发布公告,公司于6月9日收到中国证监会湖南监管局出具的《行政处罚事先告知书》(〔2026〕6号)。公司涉嫌信息披露违法违规行为被依法...
2026-06-10 22:27
 资讯
资讯 凯思凯迪完成 3.18 亿元 D 轮融资,加码胆汁酸代谢赛道,加速全球首创肝病创新药临床落地
本轮融资由太平医疗健康基金、上海科创集团联合领投,粤开资本、昭德投资、涟邦基金等多家专业医疗投资机构跟投
2026-06-10 18:56
 资讯
资讯 诺华泰菲乐联合迈吉宁新适应症获批,为BRAF V600E突变阳性RAIR-DTC患者带来精准治疗新选择
用于治疗BRAF V600E突变阳性、放射性碘难治或不适用、且血管内皮生长因子酪氨酸激酶抑制剂(VEGFR-TKI)治疗失败的局部晚期或转移性分化型甲状腺癌成人患者。
2026-06-10 18:08
 资讯
资讯 3个项目完成首批生物医学新技术临床研究备案
6月8日,中国生物技术发展中心发布生物医学新技术临床研究备案完成项目清单(第1批),自5月1日《生物医学新技术临床研究和临床转化应用管理条例》正式生效以来,5月1日至5月22...
2026-06-10 17:51
 资讯
资讯 35.7亿元!来凯医药PI3Kα抑制剂达成达成海外BD
来凯医药将授予Vasque Bio LAE118在全球范围内(不含中国大陆、中国香港、中国澳门、中国台湾地区)的独家开发、生产制造及商业化权益,全权负责该药物海外市场的全流程研发与...
2026-06-10 14:28
 资讯
资讯 腾讯、阿里等入股脑机接口企业阶梯医疗,博睿康完成上市辅导
公开资料显示,近日上海阶梯医疗科技有限公司发生工商变更,新增阿里巴巴关联公司杭州灏月企业管理有限公司、腾讯关联公司上海启善投资有限公司等为股东,同时注册资本由100万元...
2026-06-10 10:06
 资讯
资讯 药明康德、诺禾致源等被美国列入“中国军工企业”名单
今日,药明康德发布公告称,公司注意到,2026年6月8日(美国时间),美国国防部错误地将药明康德列入其根据1260H条款认定的“中国军工企业”正式更新版名单中。
2026-06-09 21:24
 资讯
资讯 微眸医疗完成近亿元A轮融资,全国首个眼科手术机器人多中心随机对照注册临床试验同期收官
本轮A轮融资由元航资本领投,老牌投资机构明桂资本持续加码追投,多家行业知名投资机构联合参与投资,伊嘉资本担任本次融资财务战略合作伙伴。
2026-06-09 20:20
 资讯
资讯 礼来公布口服小分子GLP-1 药物关键研究完整数据,潜在T2D新口服方案表现亮眼
礼来公司在美国糖尿病协会(ADA)第86届科学年会上公布了口服小分子GLP-1受体激动剂orforglipron在ACHIEVE系列三项3期临床研究中的详细数据。
2026-06-09 19:57
 资讯
资讯 因美纳发布StrataMap Spatial Solution:高性能的端到端空间全转录组研究解决方案
StrataMap Spatial支持研究人员以真正的单细胞分辨率开展空间生物学研究,拓展科学发现的边界
2026-06-09 19:52
 资讯
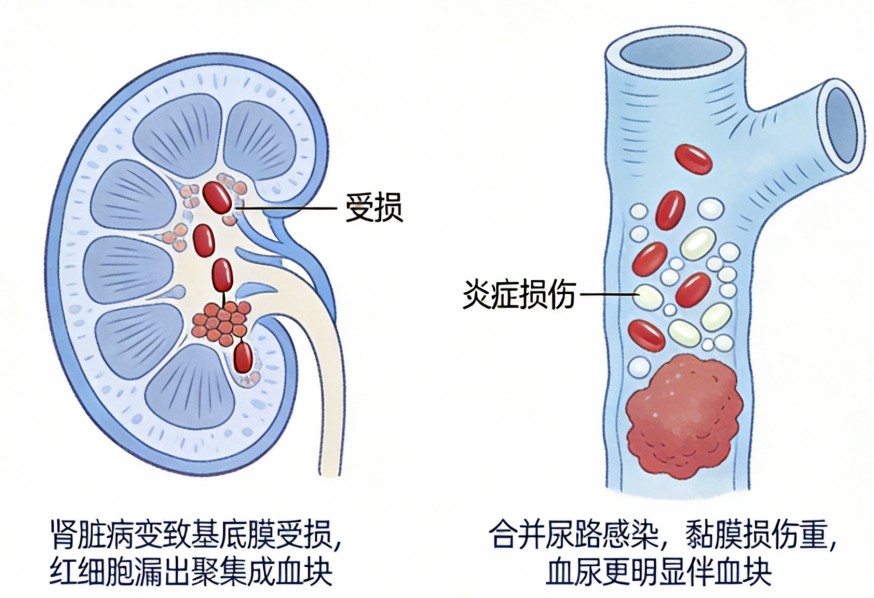
资讯 两款IgA肾病新药获批
6月9日,荣昌生物发布公告称,近日,荣昌生物制药(烟台)股份有限公司收到国家药品监督管理局(NMPA)核准签发的《药品注册证书》,泰它西普注射液(代号:RC18)治疗免疫球蛋...
2026-06-09 11:33
 资讯
资讯 第五年,2026年纠正医药购销领域和医疗服务中不正之风工作要点
《通知》围绕年度重点任务和既往工作中发现的突出问题,聚焦重点领域和关键环节,在坚持党建引领行风、强化医德医风建设、加强正向宣传引导、防范化解风险隐患、严守医疗数据安...
2026-06-09 09:14
 资讯
资讯 华超神控完成亿元天使系列融资,自研 AI 超声脑机平台开辟无创深脑调控新赛道
本轮融资分为天使轮与天使 + 轮两期,天使轮由经纬创投独家领投,天使 + 轮由德联资本、道远资本联合领投,行业知名机构持续加注,循光资本担任本次系列融资独家财务顾问。
2026-06-08 17:05





