医谷编者按:最近以来,CFDA动作不断,出台新的《药品、医疗器械产品注册收费标准》,“飞检”,《开展药物临床试验数据自查核查工作》,《严控药品再注册》等,一系列的动作都在表明CFDA针对相关的药品注册和药品研发、生产不规范以及药品注册积压、审评周期长的现状在进行调整和改变,以下是一份网络流传的CFDA工作思路,仅供大家参考。
一、解决积压品种及审评审批管理的规范(内部消息)
分类处理措施:
1、加快审评一批自主创新和临床亟需的品种;
2、坚决退审一批研究质量不好的品种;
3、严格查处一批弄虚作假的品种;
4、至2016年底基本形成审评审批和受理的进出平衡,至2018年全国实现更严格的审评审批技术规范,按规定时限审批。
二、十大要点
1、按照《国务院?意见》,仿制药品应按与原研药品的质量和疗效一致的原则审批。不再受理不是按照原研药品仿制的申请。对已经受理的仿制药申请,任按原审评标准审批,但上市后需要补做与原研药的一致性评价。鼓励企业报与原研药质量和疗效一致的重新申请。凡重新申报的,按新的收费标准缴费后,单独排队进行审评审批。批准上市的不再参与仿制药质量一致性评价。
2、在药品审评过程中,发现临床试验资料不完全,不真实,不予审批。
发现弄虚造假,严格依法处理,并向社会公布申请人、临床试验机构、合同研究组织的信息,三年内不再受理该申请人提出的药品注册申请,不再接收相应临床试验机构、合同研究组织参与研究的药品注册申报资料。
3、对临床试验和BE申请,重点审查受试者的??
申报资料无重大缺陷的,附加要求申请人按技术指南完善相关研究,有条件批准其开展临床试验,申请BE的申请人,应按SFDA制订管理规范与技术要求提交备案申请,SPDA一个月内未提出异议的,申请人可自行开展BE。
4、对同品种的注册申请实行集中审评,统一审评标准和尺度,提高效率。集中审评过程中,不符合规定的,及时作出不予批准的决定,符合规定的,按申报顺序作出审批决定并制发证明文件;
5、对创对创新药在审评过程中,允许变更申请人,变更临床适应症,审评中发现存在重大技术缺陷,不具备继续审评价值的,直接作出审评不通过的结论,如有可以弥补的技术缺项,需申请人补充资料的,告知其需要继续补充研究的有关事项,并补报相关资料。SFDA收到资料后继续开展审评。仿制药进行技术审评后不再允许补充资料。
6、建立药品注册申请立卷制度、严格控制一次性??审评,不批准。
7、对申请改变原研药剂型、改变酸根、碱基以及改变给药途径的注册申请,要严格控制,应采用新技术,以提高药品质量和安全性,与原剂型比较具有明显的临床应有优势,凡无法证明具备上述优势的,不予批准。
8、已在中国注册专利的药品,申请人可在该专利期满2年或4年内提出仿制药注册申请。不符合此规定的,不受理其注册申请,已经受理的,予以退回。对专利提出挑战的另行处理
9、对2008年以来,在注册申报资料核查中,无法确认研究资料真实性,申报资料存在雷同,数据试验无法溯源,以及仿制未公布处方和工艺的中药制剂品种,一律不予批准,将相关注册申请退回申请人。
10、凡活性成分不明确,结构不清楚或疗效不确切的仿制药一律不予批准。相关被仿制药品已经在中国上市的,SFDA公布品种名单,要求相关企业在五年内开展再评价,未能通过再评价的,药品批准文号有效期期满后不予再注册,注销其批准文号。
11、适时发布《限制审批品种目录》,引入限制审批的品种范围。
(1) 市场需求供大于求的品种
(2)与已上市同品种相比,不具备临床优势或安全性风险更高的品种。
(3)安全性或有效性存在风险的已上市品种的仿制药
(4)剂型或规格不合理的品种
引入目录的不再受理该品种的注册申请,对已受理的停止批准,已上市的由SFDA分期分批进行质量一致性评价。
12、技术审核结论有重大技术争议的,申请人可以提出复审申请,由审评部门组织召开专家、申请人、审评人员共同参加的会议,公开进行论证,并将论证结果向社会公开。
13、儿童药品、国内国际同步注册的品种单列审评审批。
来源:江苏省医药联盟
为你推荐
 资讯
资讯 华东医药独家商业化产品CXG87上市申请获受理,呼吸治疗赛道布局深化
华东医药股份有限公司(以下简称“华东医药”或“公司”)全资子公司华东医药(杭州)有限公司独家商业化产品CXG87(布地奈德福莫特罗吸入粉雾剂(IV)胶囊型)用于治疗哮喘的药...
2026-04-22 17:53
 资讯
资讯 指南更新,巨星发声:医疗创新与公众教育双轮驱动OSA诊疗革新
日前,中国《成人阻塞性睡眠呼吸暂停诊治指南(2025)》发布,首次系统性引入药物治疗——GIP GLP-1双受体激动剂替尔泊肽获最高级别推荐,用于合并肥胖症的中至重度阻塞性睡眠...
2026-04-22 10:04
 资讯
资讯 江苏2025年癌症发病情况
近日,江苏省发布2025年癌症发病情况数据。据2025年最新肿瘤监测数据显示,江苏省癌症发病率为392 84 10万,较2024年(380 50 10万)增长3 24%。同期江苏全省癌症死亡率为2...
2026-04-21 16:39
 资讯
资讯 中国生物制药发布了其PD-1/VEGF双抗的初步临床试验数据
4月19日,中国生物制药发布了其PD-1 VEGF双抗(药物研发代号为MK-2010 LM-299)的初步临床试验数据。
2026-04-21 13:25
 资讯
资讯 天境生物将菲泽妥单抗大中华区权益转售给渤健
4月20日,天境生物(TJ Biopharma)与渤健(Biogen,纳斯达克代码:BIIB)共同宣布,双方已达成一项最终协议,渤健将从天境生物获得菲泽妥单抗的大中华区(包括中国大陆、香港...
2026-04-21 11:00
 资讯
资讯 云顶新耀发布EVM16个性化肿瘤治疗性疫苗首次人体临床试验数据
4月20日,云顶新耀在2026年美国癌症研究协会(AACR)年会上公布了其自主研发的mRNA个性化肿瘤治疗性疫苗EVM16单药治疗及联合PD-1抑制剂(替雷利珠单抗 百济神州)治疗晚期实体...
2026-04-21 09:15
 资讯
资讯 剂泰科技通过港交所聆讯,携全球首个 AI 纳米递送平台冲刺 "AI 药物递送第一股"
剂泰科技成立于 2020 年,由美国工程院院士陈红敏博士以及 MIT 科学家赖才达博士、王文首博士联合创立,是一家专注于 AI 驱动纳米材料创新的高科技企业。
2026-04-20 17:25
 资讯
资讯 飞眸医疗完成近亿元天使轮融资,加速打造国际领先个性化全飞秒屈光系统平台
近日,深圳市飞眸医疗器械技术有限公司(以下简称 "飞眸医疗")正式宣布完成近亿元天使轮融资,本轮融资由元生创投领投,清科控股、清科大
2026-04-20 17:18
 资讯
资讯 倍乐锐(注射用玛贝兰妥单抗)获批用于治疗二线及以上多发性骨髓瘤成年患者
与达雷妥尤单抗的三联疗法相比,倍乐锐®联合治疗方案可降低死亡风险42%,并延长中位无进展生存期近三倍。
2026-04-20 16:58
 资讯
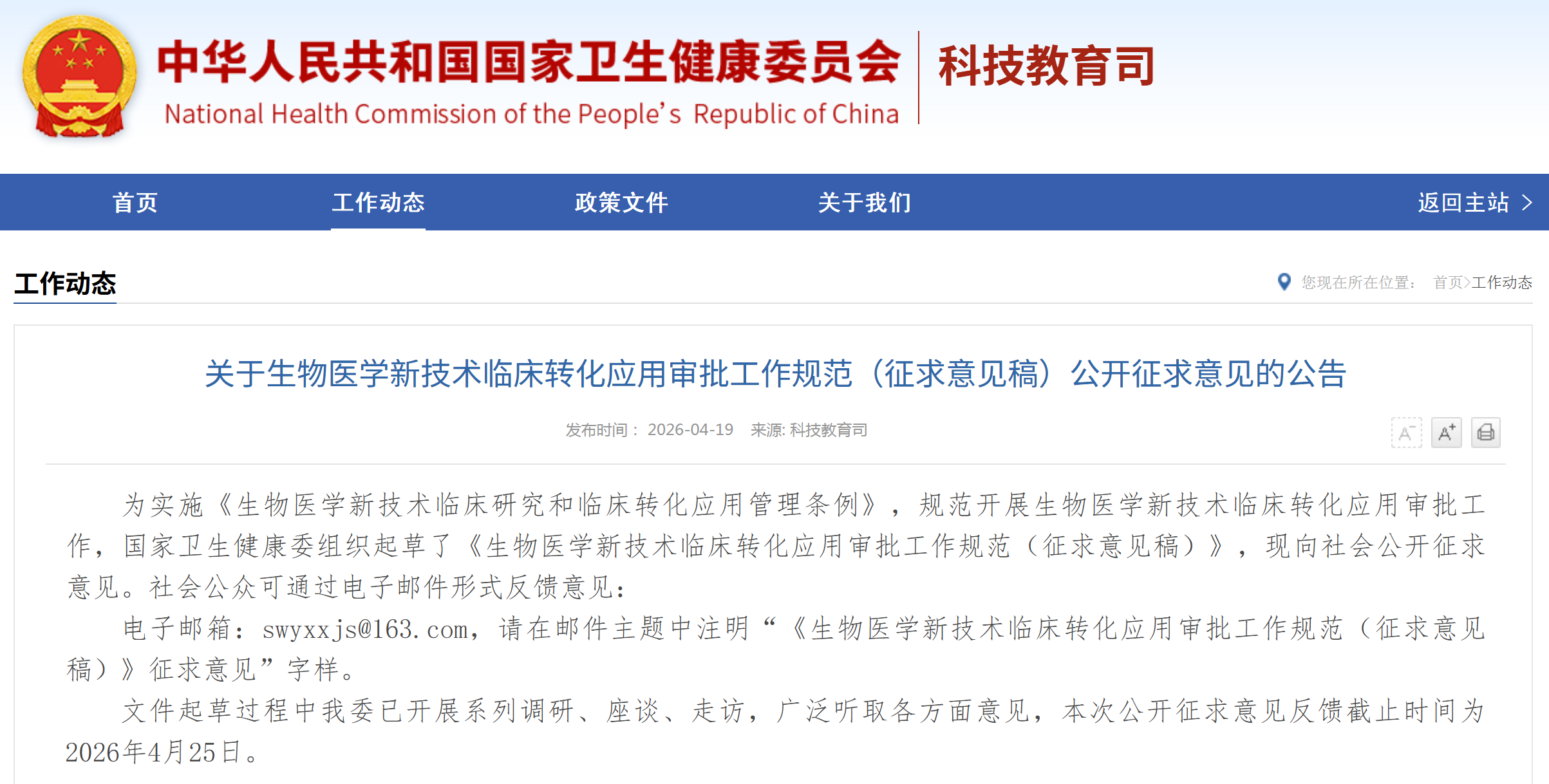
资讯 818政策落地细则,如何临床转化应用细则征求意见稿发布
4月19日,备受业内关注的“818政策”终于迎来了第一份实施细则。国家卫健委正式对外发布《生物医学新技术临床转化应用审批工作规范(征求意见稿)》。
2026-04-19 23:51
 资讯
资讯 长春高新口服小分子生长激素再获新适应症IND
近日,长春高新发布公告,子公司长春金赛收到国家药品监督管理局核准签发的《药物临床试验批准通知书》,金赛药业GS3-007a干混悬剂境内生产药品注册临床试验申请获得批准。受理...
2026-04-19 16:02
 资讯
资讯 OpenAI 发布首款药物研发专用 AI 模型 GPT-Rosalind
不同于通用大模型,GPT-Rosalind 是 OpenAI 首个针对单一行业构建的前沿推理模型
2026-04-17 15:33
 资讯
资讯 创新泡沫剂型银屑病药物恩适达(卡泊三醇倍他米松泡沫剂)在华获批
是中国首个且目前唯一用于成人斑块状银屑病外用治疗的泡沫剂,专利的起泡装置可帮助患者轻松将药物均匀涂抹于皮肤,包括有毛发的部位。
2026-04-17 15:17