12月9日,武汉友芝友生物制药股份有限公司(以下简称“友芝友”)向港交所递交招股书,拟香港主板IPO上市。
5款产品进入临床开发阶段
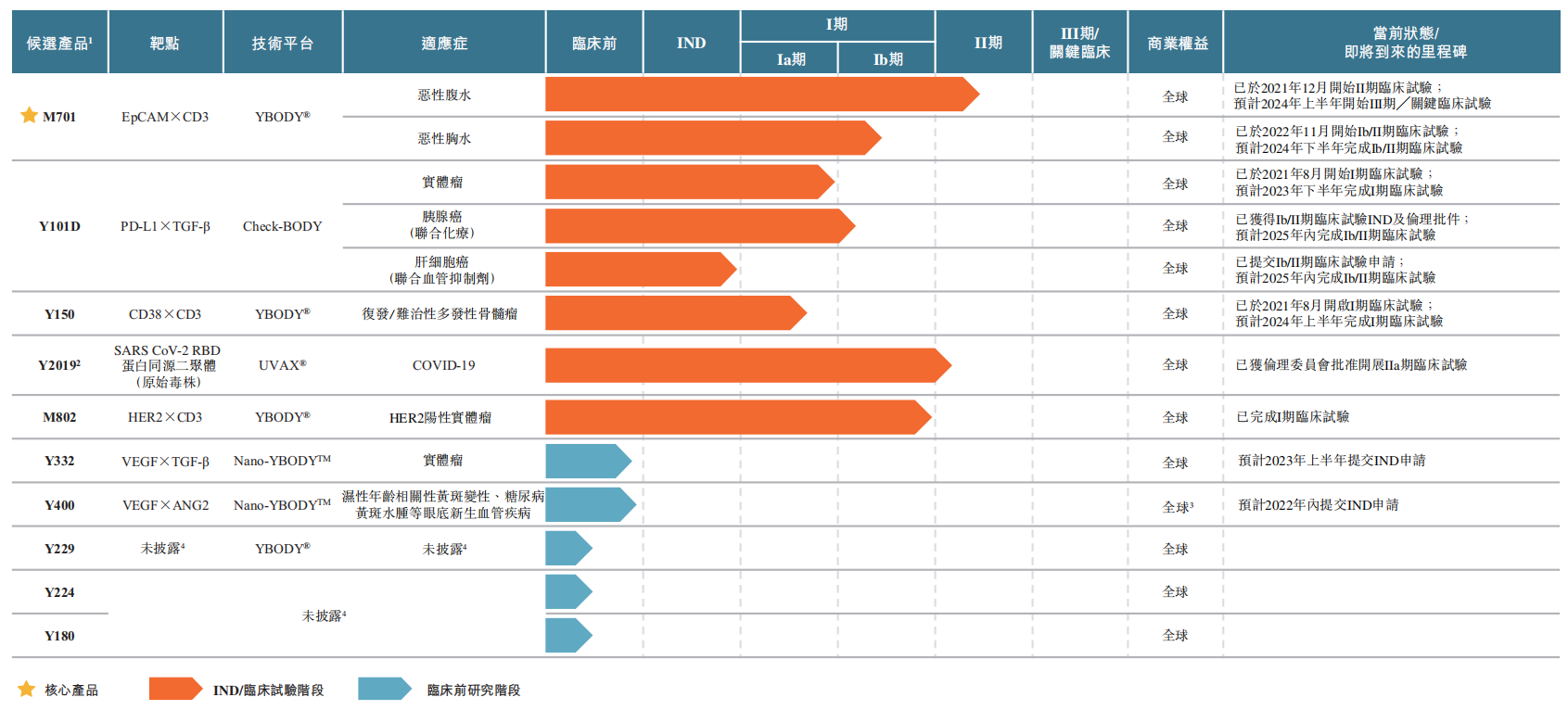
友芝友成立于2010年,专注于双特异性抗体(BsAb)靶向和肿瘤免疫疗法的开发,目前拥有四个创新平台,包括YBODY平台、Check-BODY平台、Nano-YBODY、UVAX平台。基于以上平台,友芝友目前共开发10款候选药物管线,其中5款在中国处于临床开发阶段,另外5款处于研制和临床前阶段。这些候选药主要包括:
(1)3种T细胞接合的BsAb——M701、M802和Y150
M701是一种重组BsAb,靶向EpCAM表达的癌细胞及CD3表达的T细胞,此外M701还通过抗体依赖性细胞毒性(ADCC)和补体依赖的细胞毒性(CDC)显示出对肿瘤细胞的细胞毒性。M701主要适应症为EpCAM阳性肿瘤的恶性腹水/胸水,根据弗若斯特沙利文的资料,M701是全球首款及唯一进入II期临床试验的治疗MA的EpCAM × CD3 BsAb。
M802是一种抗人表皮生长因子受体2(HER2)及抗CD3人源化BsAb,目前正在开发用于治疗HER2阳性实体瘤。在中国完成的1期临床试验数据表明,M802具有良好的安全性。根据弗若斯特沙利文的资料,M802是国内首款取得IND审批的国内自主研发BsAb。
Y150是一款重组抗CD38和抗CD3人源化BsAb,目前正处于I期临床试验中,根据弗若斯特沙利文的资料,Y150是中国唯一一款进入临床开发的靶向分化簇38(CD38)及T细胞接合的BsAb。
(2)2种靶向肿瘤微环境(TME)的候选药物——Y101D和Y332
Y101D是一种重组抗PD-L1和抗TGF-β人源化BsAb,拟用于晚期实体瘤。据悉,Y101D专门用于同时抑制PD-1/PD-L1轴和TGF-β信号通路,因此具有释放协同抗肿瘤活性和缓解耐药性的潜力。目前,Y101D正在I期临床试验中评估单药治疗转移性或局部晚期实体瘤的数据。
Y332是一款重组抗血管内皮生长因子(VEGF)及抗TGF-β BsAb,拟用于治疗多种实体瘤,目前Y332正在进行CMC研究,计划于2023年上半年向国家药监局提交IND申请。
(3)治疗老年病的靶向疗法——Y400
Y400是一款重组抗血管内皮生长因子(VEGF)和抗血管生成素-2(ANG2)的BsAb。目前Y400已完成CMC研究,预期于2022年底前向国家药监局提交IND。今年7月,友芝友与康哲药业达成关于Y400的合作,目前友芝友已收到500万美元的全额首付款。
截至最后实际可行日期,友芝友在中国拥有20项已颁发专利,在美国拥有7项已颁发专利,在其他司法权区拥有3项已颁发专利。目前,该公司还拥有47项专利申请,其中包括14项待决中国专利申请、5项待决美国专利申请。同时,根据弗若斯特沙利文的资料,在中国拥有专有双特异性平台的所有竞争对手中,友芝友的T细胞接合的BsAb在开发阶段及数量方面位列第一。
石药集团子公司为主要股东之一
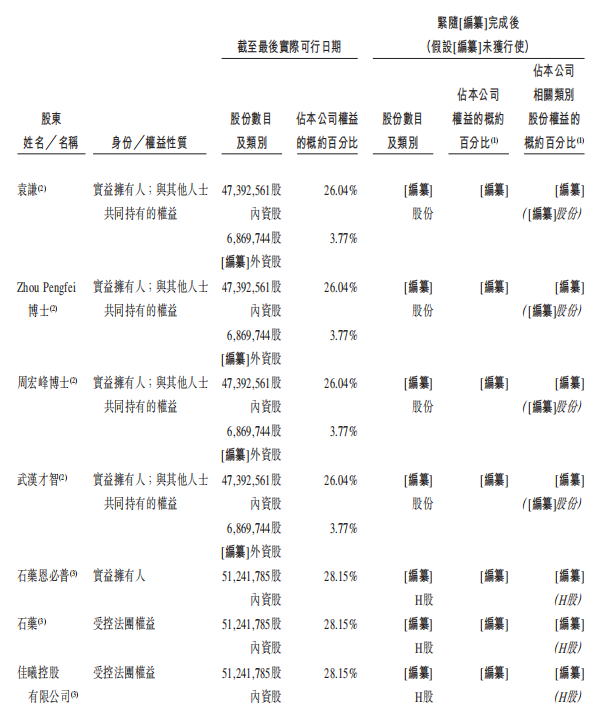
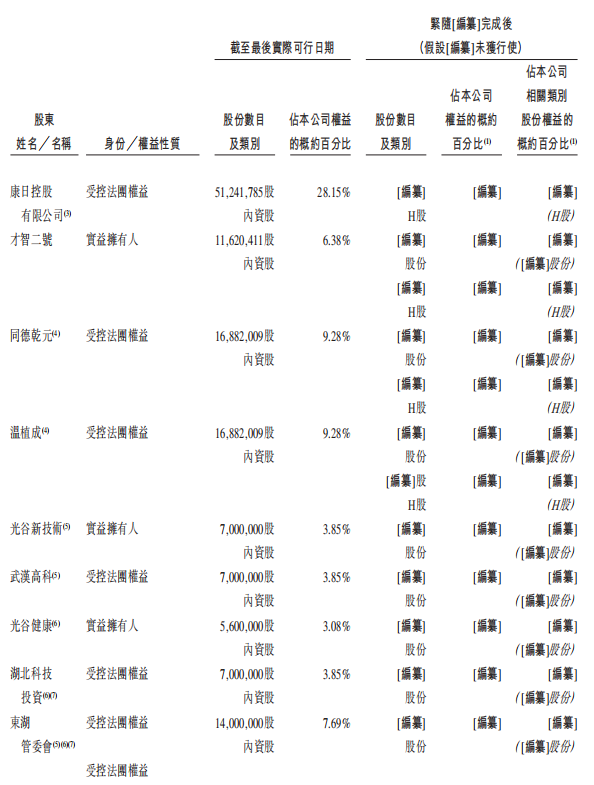
资料显示,此次IPO前友芝友共完成五轮融资,包括1.57亿元A轮、1.69亿元B轮、2000万元B+轮、7350万元B++轮、2亿元C轮,C轮后估值26亿元。
根据其招股书,本次上市前石药集团及公司石药恩必普、袁谦、武汉才智、才智二号、周宏峰、汇友兴曜、长星成长、海南博友、广瑞弘祥、光谷新技术、Zhou Pengfei和光谷健康分别持股28.15%、11.21%、9.23%、6.38%、5.60%、5.57%、4.35%、4.19%、3.95%、3.85%、3.77%和3.08%,其中石药恩必普为主要股东之一。
暂未实现商业化
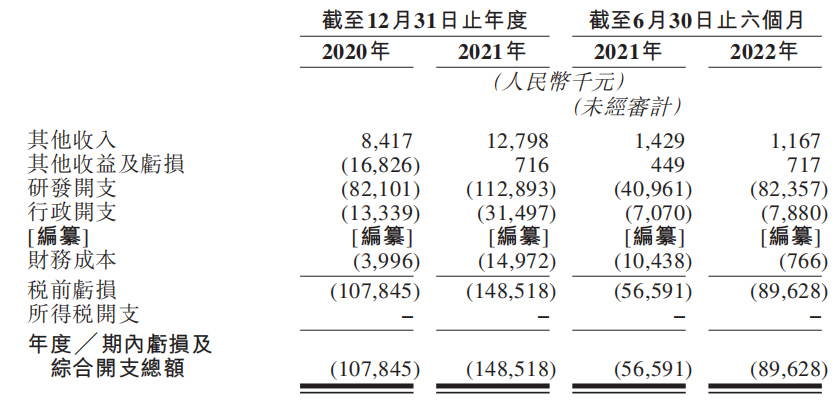
目前,友芝友尚无产品获批准进行商业销售,且没有从产品销售中产生任何收入。招股书显示,2020年、2021年和2022年上半年,友芝友的其他收入分别为841.7万元、1279.8万元和116.7万元,净亏损分别为1.08亿元、1.49亿元和8962.8万元。2020年、2021年和2021年上半年末,友芝友生物的资产总值分别为2.09亿元、2.00亿元和1.50亿元,资产净值(负债净额)分别为-3074.3万元、1.43亿元和9661.0万元,权益总额分别为-3074.3万元、1.43亿元和9661.0万元。
对于亏损,友芝友生物表示主要由研发开支、行政开支和融资成本所致。2020年、2021年及2022年上半年,友芝友的研发开支分别为8210.1万元、1.13亿元、8235.7万元。同时,
友芝友称,自成立以来已产生净亏损,并且预计于可预见未来将继续产生净亏损,且或不能产生充足收益达到或维持盈利能力,以及药品的研究、开发及商业化在所有重要方面均受到严密监管。
根据招股书,友芝友此次递表港交所,募集资金将主要用作候选药物M701、Y101D、Y150、Y2019的临床开发和商业化,推进其他候选药物(包括Y400、Y332和其他临床前候选药物)的临床前和临床研究。同时,该公司还将通过内外部投入,进一步开发和提升公司的双特异性抗体技术平台。
为你推荐
 资讯
资讯 因美纳推出TruPath Genome,树立基因组洞察新标准
2026年2月24日,因美纳(纳斯达克股票代码:ILMN)宣布推出TruPath™ Genome,为遗传病研究领域的高质量、全面的全基因组洞察树立新标准。
2026-02-27 12:04
 资讯
资讯 济川药业引入国产非激素类创新药为湿疹治疗添新解
济川药业(股票代码:600566)宣布与泽德曼医药正式签署合作协议,济川药业将获得泽德曼医药泽立美®本维莫德乳膏在中华人民共和国(不含香港、澳门特别行政区和台湾地区)的独...
2026-02-27 11:54
 资讯
资讯 因美纳发布NovaSeq X创新升级路线图: 数据质量、读数产出、速度与灵活性全面提升
读数产出提升40%至350亿、最高可达Q70质量分值、更快周转时间与“交错启动”等升级将陆续面向所有NovaSeq X测序仪推出,推动精准医疗发展,并为客户带来持续叠加价值
2026-02-27 11:42
 资讯
资讯 礼来ACHIEVE-3完整数据公布:orforglipron在头对头研究中优于口服司美格鲁肽
2026年2月26日,礼来正式公布了ACHIEVE-3研究的完整数据。该研究结果同步发表于国际权威医学期刊《柳叶刀》。
2026-02-27 11:38
 资讯
资讯 诺和诺德大幅下调司美格鲁肽价格
近日,诺和诺德宣布,将将大幅下调美国的司美格鲁肽药物官方标价(批发采购成本)其中减重版司美格鲁肽Wegovy降幅度50%,降糖版Ozempic降幅约35%。
2026-02-26 13:37
 资讯
资讯 新版《鼓励进口服务目录》发布,生命健康领域有哪些?
2月25日,商务部等七部门联合发布新版《鼓励进口服务目录》,目录主要包含研发设计服务、节能环保服务、环境服务、咨询服务、其他专业服务和医疗与健康服务六大板块。
2026-02-26 11:29
 资讯
资讯 长春高新一项拟用于改善特发性原因导致儿童小阴茎的临床试验获批
2月24日晚间,长春高新(000661 SZ) 发布公告称,旗下核心子公司金赛药业自主研发的GenSci141软膏(双氢睾酮软膏) 正式获得国家药监局临床试验批准通知书。
2026-02-25 22:32
 资讯
资讯 “童颜针”预灌装剂型获批
2月24日,国家药监局发布医疗器械批准证明文件送达信息显示,上海汇悦妍生物科技有限公司全资子公司和妍(上海)医疗器械有限公司申报的“注射用聚左旋乳酸微球填充剂”成功获得...
2026-02-25 14:03
 资讯
资讯 CDE:新药全球同步研发中基于多区域临床试验数据进行获益-风险评估的指导原则(试行)
前是中国审评机构评价MRCT所遵循的主要依据。中国审评机构鼓励申办者基于ICH E17指导原则开展MRCT,加速全球新药在中国市场的同步研发进程,并促进全球新药在中国的同步申报、...
2026-02-25 10:59
 资讯
资讯 李强主持召开国务院常务会议,研究推进银发经济和养老服务发展有关工作
会议指出,我国银发经济潜力很大,要完善支持举措、强化政策落实,促进养老事业和养老产业发展,为应对人口老龄化提供有力支撑。
2026-02-25 10:09
 资讯
资讯 基石药业PD-1在英国获批新适应症
2月24日,基石药业发布公告称,公司PD-1产品舒格利单抗的新适应症申请已获英国MHRA批准,单药用于治疗肿瘤细胞PD-L1表达≥1%、无表皮生长因子受体(EGFR)敏感突变或ALK、ROS1基...
2026-02-24 16:47
 资讯
资讯 9.5亿美元里程碑付款,前沿生物两款小核酸药物授权GSK
2月23日晚间,前沿生物发布公告称,已与全球领先生物制药企业葛兰素史克(GSK)签署独家授权许可协议,葛兰素史克将获得两款小核酸(siRNA)管线产品在全球范围内的独家开发、生...
2026-02-24 13:49
 资讯
资讯 独家生产品种纳入国家基本药物目录应当经过单独论证,新版《国家基本药物目录管理办法》发布
国家基本药物工作协调机制由国家卫生健康委、国家发展改革委、工业和信息化部、财政部、商务部、市场监管总局、国家医保局、国家中医药局、国家疾控局、国家药监局和中央军委后...
2026-02-13 16:05
 资讯
资讯 玄言生物完成数千万元Pre-A轮融资,加速AI驱动精准诊疗产品落地
本轮融资资金将主要用于推进公司AI驱动的精准诊疗产品在多中心临床验证、注册申报及规模化应用中的落地进程,进一步夯实核心技术平台优势,拓展产品管线布局,助力AI医疗从科研...
2026-02-13 12:18