近期,罗氏宣布关键lidERA BC研究[1]取得重磅阳性结果,giredestrant成为全球首个在HR+/HER2-早期乳腺癌辅助治疗中,实现无浸润性疾病生存期(iDFS)统计学与临床意义双重显著的口服选择性雌激素受体降解剂(SERD),填补了口服SERD在早期辅助治疗领域的空白。继evERA BC研究[2]在晚期CDK4/6抑制剂经治的耐药人群证实获益后,这一结果标志着口服SERD完成了从晚期解救到早期治愈的关键跨越。
Giredestrant的突破性进展并非孤证,而是罗氏乳腺癌全周期布局的重要组成部分。近二十多年来,从覆盖HER2阳性、TNBC等亚型的靶向与免疫治疗药物,到HR+/HER2-领域构建起完整证据链条,罗氏的乳腺癌诊疗布局正在日益完善。
李滨博士(左)、沈淑仪博士(右)正在分享
为深度解码lidERA BC研究的划时代价值、解析罗氏乳腺癌领域的战略布局,医脉通特邀罗氏制药中国医学事务副总裁李滨博士与罗氏全球产品开发中国中心临床科学负责人沈淑仪博士,共同剖析该研究成果的突破性临床价值与重点患者人群获益,分享罗氏以患者需求为核心的研发战略远见,展望乳腺肿瘤诊疗新方向。
医脉通:lidERA BC研究的成功给全球乳腺癌临床实践带来了哪些关键意义?giredestrant从晚期治疗成功走向早期辅助治疗,这一突破背后体现了罗氏怎样的研发策略与临床设计智慧?
沈淑仪博士:evERA BC研究已证实giredestrant能为CDK4/6抑制剂经治的晚期患者,包括存在ESR1突变耐药的患者带来显著获益,满足了晚期治疗的需求。而lidERA BC研究作为首个此类药物在早期辅助治疗中取得阳性结果的III期研究,其意义更为深远。不仅标志着HR+早期乳腺癌治疗从相对同质化走向“精准强化”,为中高危患者提供了更优选择;更有望通过其疗效与可耐受性优化长期管理,在关键窗口期内为患者奠定更坚实的治愈基础,直击“远期复发”的临床痛点,主动干预并改写疾病长期病程。
李滨博士:这背后体现了罗氏深刻的科学洞见与前瞻的研发勇气。
我们不仅追求延长晚期患者生命,更追求早期患者的“治愈”,因此致力于在早期在微转移阶段就有效扼制高危因素,推动该疾病真正走向治愈。同时,开展这样一项耗时久、投入大的早期辅助治疗研究,需要打破现状的决心,这体现了我们从“跟跑”迈向“领跑”的努力。此外,我们也致力于构建从早期到晚期的完整证据链,以期在全疾病周期为患者提供精准的解决方案。
医脉通:在这一关键研究背后,有哪些令人印象深刻的研发故事或经历?
沈淑仪博士:每一项研究的成功都凝聚着不懈的探索与严谨求实的精神。对于giredestrant而言,其研发始于对雌激素受体结构的深刻理解,通过精密的构效关系研究,才设计出这款兼具高效降解活性与良好口服生物利用度的分子[3],为后续开发奠定了坚实基础。回顾整个临床开发计划(CDP),有两点令我尤为深刻。
其一是在II期coopERA研究[4]中,作为概念验证(Proof of Concept)研究,我们创新地选择在新辅助治疗“机会窗口”(window of opportunity)内开展,以生物标志物Ki67的变化快速验证概念,为后续投入大规模III期研究提供了决定性信心。
其二是在III期阶段,我们采取多个适应症平行推进的策略,尤其是大胆布局了样本量巨大的早期辅助治疗研究。这既体现了公司在竞争中的决心,更源于我们对HR+患者在不同疾病阶段真实需求的深刻认识,希望为尚处早期的患者争取治愈机会。
医脉通:从HER2阳性领域二十余年的引领,到如今HR+/HER2-领域的重大突破(如伊那利塞、Giredestrant)。罗氏乳腺癌研发管线的背后体现了怎样的战略视野与研发初心?
李滨博士:罗氏的战略始终是“先患者之需而行”,针对不同类型与阶段的乳腺癌提供创新方案。在HER2+领域,我们从确立联合治疗标杆到开发便捷的皮下制剂,是一个从“做加法”到“做减法”以提升患者生活质量的过程。在HR+领域,我们打出“组合拳”以构建全周期精准防线:包括针对PIK3CA突变的精准药物伊那利塞、作为基石药物的口服SERD giredestrant,以及针对CDK4/6抑制剂耐药而引入的CDK4/2抑制剂RGT-419B等。对于三阴性乳腺癌(TNBC),我们也通过自研与合作进行多维攻坚,力争为每一位患者提供综合性治疗方案。
医脉通:过去,罗氏与中国乳腺学界的长期合作取得了有目共睹的成就。您如何看待这一历程?未来,您认为可在哪些方面继续开展更深层次的协作?
沈淑仪博士:这是一段共同成长的振奋历程。中国研究者已从早年临床研究的“执行者”逐步蜕变为如今全球研发的“共同创造者”,能够将中国的临床实践洞见有效融入全球研发体系与试验方案设计中。展望未来,我们期望中国不仅能继续在III期研究中发挥关键作用,更能深入参与从早期剂量探索到概念验证的全临床开发计划,将中国临床思路融入早期研究。
李滨博士:我们将秉持“从中国为中国,从中国为全球”(In China for China;In China for Global)的理念,从三方面深化协作。
一是搭建“创新桥梁”,通过合作引入本土优秀创新产品并助力其走向全球。
二是打造“能力平台”,共建研究者发起的研究(IIT)合作平台,将中国经验转化为全球证据。
三是培育“人才沃土”,通过赋能合作助力中国临床研究能力提升,推动中国乳腺癌诊疗实现从“参与”到“引领”的跨越。
医脉通:未来,罗氏将如何继续巩固其在乳腺癌领域的前沿引领地位,继续惠及更多中国患者?
李滨博士:首先,我们将持续深化创新药物的研发与拓展,强化在各亚型、各临床阶段的布局。其次,我们将探索“诊疗管”一体化的综合解决方案,从药物治疗、诊断分型到疾病管理,提供全周期管理赋能。最后,我们将持续赋能中国专家,助力其临床研究能力提升,实现从“并跑”到“领跑”。未来期望产出更多能影响全球指南的高质量中国证据,最终将中国患者的预后提升至全新高度。
参考文献
[1] https://clinicaltrials.gov/study/NCT04961996
[2] Mayer E, et al. Giredestrant (GIRE), an oral selective oestrogen receptor (ER) antagonist and degrader, + everolimus (E) in patients (pts) with ER-positive, HER2-negative advanced breast cancer (ER+, HER2– aBC) previously treated with a CDK4/6 inhibitor (i): Primary results of the Phase III evERA BC trial. ESMO 2025. LBA #16.
[3] Liang J, et al. X. GDC-9545 (Giredestrant): A Potent and Orally Bioavailable Selective Estrogen Receptor Antagonist and Degrader with an Exceptional Preclinical Profile for ER+ Breast Cancer. J Med Chem. 2021 Aug 26;64(16):11841-11856. doi: 10.1021/acs.jmedchem.1c00847. Epub 2021 Jul 12. PMID: 34251202.
[4] Hurvitz SA, et al. coopERA Breast Cancer study group. Neoadjuvant palbociclib plus either giredestrant or anastrozole in oestrogen receptor-positive, HER2-negative, early breast cancer (coopERA Breast Cancer): an open-label, randomised, controlled, phase 2 study. Lancet Oncol. 2023 Sep;24(9):1029-1041.
来源:医脉通
为你推荐
 资讯
资讯 入选不足4月,和黄医药申请将达唯珂移出首版商保创新药目录
国家医疗保障局办公室今日发布通知,自2026年3月9日起,撤销氢溴酸他泽司他片(商品名:达唯珂)在全国各省级医药采购平台挂网资格,并根据企业申请,将该药品移出《商业健康保...
2026-03-09 22:09
 资讯
资讯 CDE:抗肿瘤药物生物等效性及药代动力学比对研究受试者人群选择考虑
本指导原则主要基于小分子化学药物及单抗类药物的研究经验,为抗肿瘤药物 BE PK 比对研究中受试者人群的选择考虑提供建议。
2026-03-07 10:59
 资讯
资讯 四家知名药企被暂停军队采购
近日,军队采购网发布一批“军队采购暂停名单”,其中涉及四家药企被列入暂停名单,具体为北京费森尤斯卡比医药有限公司、齐鲁制药有限公司、宜昌人福药业有限责任公司和江苏新...
2026-03-07 10:41
 资讯
资讯 新一代 cAMP 偏向型 GLP-1 受体激动剂埃诺格鲁肽(先维盈)获批用于中国成人体重管理
在一项大型III期临床研究中展现出具有临床意义的减重效果:治疗48周时,受试者的平均体重下降达15 4%,其中92 8%的受试者实现了5%以上的体重减轻。
2026-03-06 12:38
 资讯
资讯 11.8亿美元!德琪医药自免TCE双抗ATG-201授权优时比
德琪医药将其自主研发的CD19 CD3双特异性T细胞连接抗体(TCE)ATG-201的全球开发、生产及商业化独家权益授予优时比,用于治疗B细胞相关自身免疫性疾病。
2026-03-04 20:05
 资讯
资讯 君实生物被调出科创50
近日,上海证券交易所,中证指数有限公司联合发布《关于科创50等指数一季度定期调整结果的公告》,本次调整,调入3家,调出3家,其中君实生物被调出科创50指数,此次调整将于202...
2026-03-04 15:30
 资讯
资讯 吉利德比克替拉韦与来那帕韦单片治疗方案在更换抗反转录病毒治疗药物的 HIV 感染者中维持病毒学抑制
新型在研药物组合将全球指南推荐、具有高耐药屏障的整合酶链转移抑制剂比克替拉韦,与同类首创衣壳抑制剂来那帕韦相结合
2026-03-04 13:41
 资讯
资讯 全球首创便携式宫颈无创光动力治疗药物希维她在华获批
CIN2的治疗决策一直是妇科宫颈上皮内病变治疗临床实践中的核心挑战,宫颈环形电切术(LEEP)等切除性手术虽为临床常用的治疗方案,但其可能导致宫颈结构改变、宫颈机能不全,进...
2026-03-04 13:32
 资讯
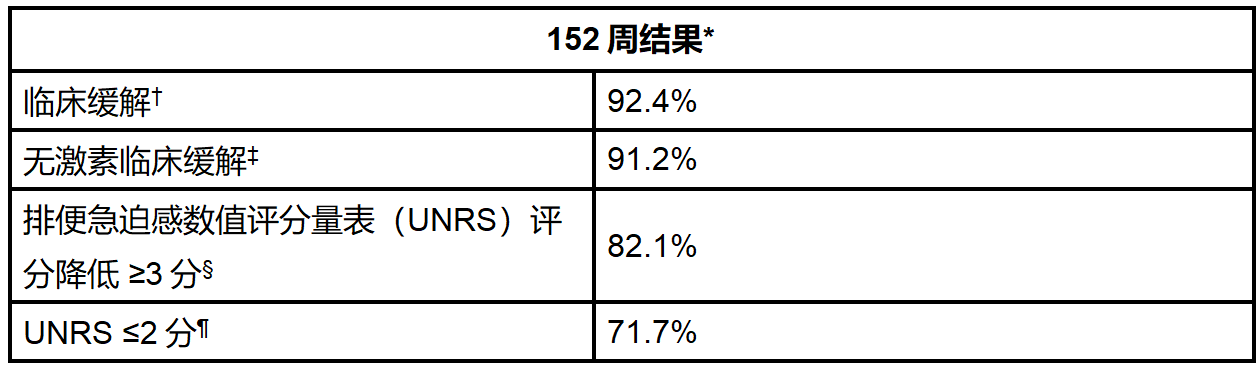
资讯 礼来安妥来利和安妥来(米吉珠单抗)可使克罗恩病患者维持长达三年的无激素缓解
具有里程碑意义的VIVID-2研究数据显示,在治疗后一年实现无激素缓解的患者中,超过90%在三年内仍维持无激素缓解
2026-03-04 13:22
 资讯
资讯 甘李药业一款PROTAC在研药品获批临床试验
3月2日晚间,甘李药业发布公告,在研药品 GLR2037 片的取得国家药监局《药物临床试验批准通知书》。受理号为 CXHL2600098、CXHL2600099,通知书编号为 2026LP00526、2026LP0...
2026-03-03 13:51
 资讯
资讯 非共价(可逆)BTK抑制剂匹妥布替尼获批新适应症
3月2日晚间,信达生物发布公告,公司与礼来中国共同宣布非共价(可逆)BTK抑制剂捷帕力(匹妥布替尼)正式获得中国国家药品监督管理局(NMPA)批准新增适应症,用于治疗既往经过...
2026-03-03 13:19
 资讯
资讯 ICON发布2025年中国生物技术行业调研报告:中国创新领跑全球,95%受访者对未来充满信心
调研显示,中国正成为全球药物创新关键引擎,在细胞疗法、心血管及肿瘤领域持续领跑,AI应用与全球化布局正驱动行业发展
2026-03-03 10:58









