4月19日,备受业内关注的“818政策”终于迎来了第一份实施细则。国家卫健委正式对外发布《生物医学新技术临床转化应用审批工作规范(征求意见稿)》。
2025年9月28日,国务院令第818号发布,正式公布《生物医学新技术临床研究和临床转化应用管理条例》,这是我国首部关于生物医学新技术临床研究和临床转化应用的国务院行政法规。政策的最大核心是《条例》覆盖“临床研究-转化应用-上市后监管”全生命周期,形成了全链条可操纵的规程,并明确对临床研究证明安全、有效的生物医药新技术,可转化为临床应用收费,构建了细胞治疗、基因治疗等前沿生物医学技术临床研究转化的商业化闭环。因此,受到业内广泛关注,被业内简称为“818号令”或“818政策”。
4月19日发布的《生物医学新技术临床转化应用审批工作规范(征求意见稿)》即是大家最为关切的如何临床转化应用的操作细则。
可转化的生物医学新技术
根据征求意见稿第三条,可转化的生物医学新技术为个性化程度高,国内尚没有使用同类机制原理的药品获得上市许可或者已启动确证性临床试验;或用于治疗国家卫生健康委公布的《罕见病目录》收录的罕见病,国内尚没有使用同类机制原理、针对相同适应症的药品获得上市许可或者已启动确证性临床试验。
这意味目前已经取得IND或者已经进入临床试验的在研细胞、基因药物将无法转化为技术。个性化程度高,意味着非通用性,同时从适应症的角度,主要面向罕见病,意味着大适应症的前沿技术依然要走药品路线。
此外,征求意见稿第三条还明确对符合《医疗器械监督管理条例》医疗器械定义的,应当按照医疗器械法规要求开展相关注册工作,不纳入生物医学新技术临床转化应用审批范围。这意味着目前备受关注的外泌体技术如果转化为诊断,依然要走医疗器械路径。
受理机构
征求意见稿明确中国生物技术发展中心(以下简称生物中心)作为专业机构,承担生物医学新技术临床转化应用专业审查工作,协同配合转化应用后再评估工作。中国生物技术发展中心类似于药监体系下的CDE职责,同时其还是人类遗传的管理机构。
国家卫生健康委医疗管理服务指导中心作为专业机构,承担转化应用后再评估工作,协同配合生物医学新技术临床转化应用的机构和人员资质、临床应用操作规范审查工作。
国家卫生健康委负责全国生物医学新技术临床转化应用审查批准和监督管理工作。县级以上人民政府卫生健康主管部门负责本行政区域的生物医学新技术临床转化应用的监督管理工作。
如何审评
根据材料核查、技术评估和伦理评估情况,生物中心组织专家提出“建议批准”、“建议不予批准”、“延期再审”、“终止审查”等评估意见,并撰写评估报告。
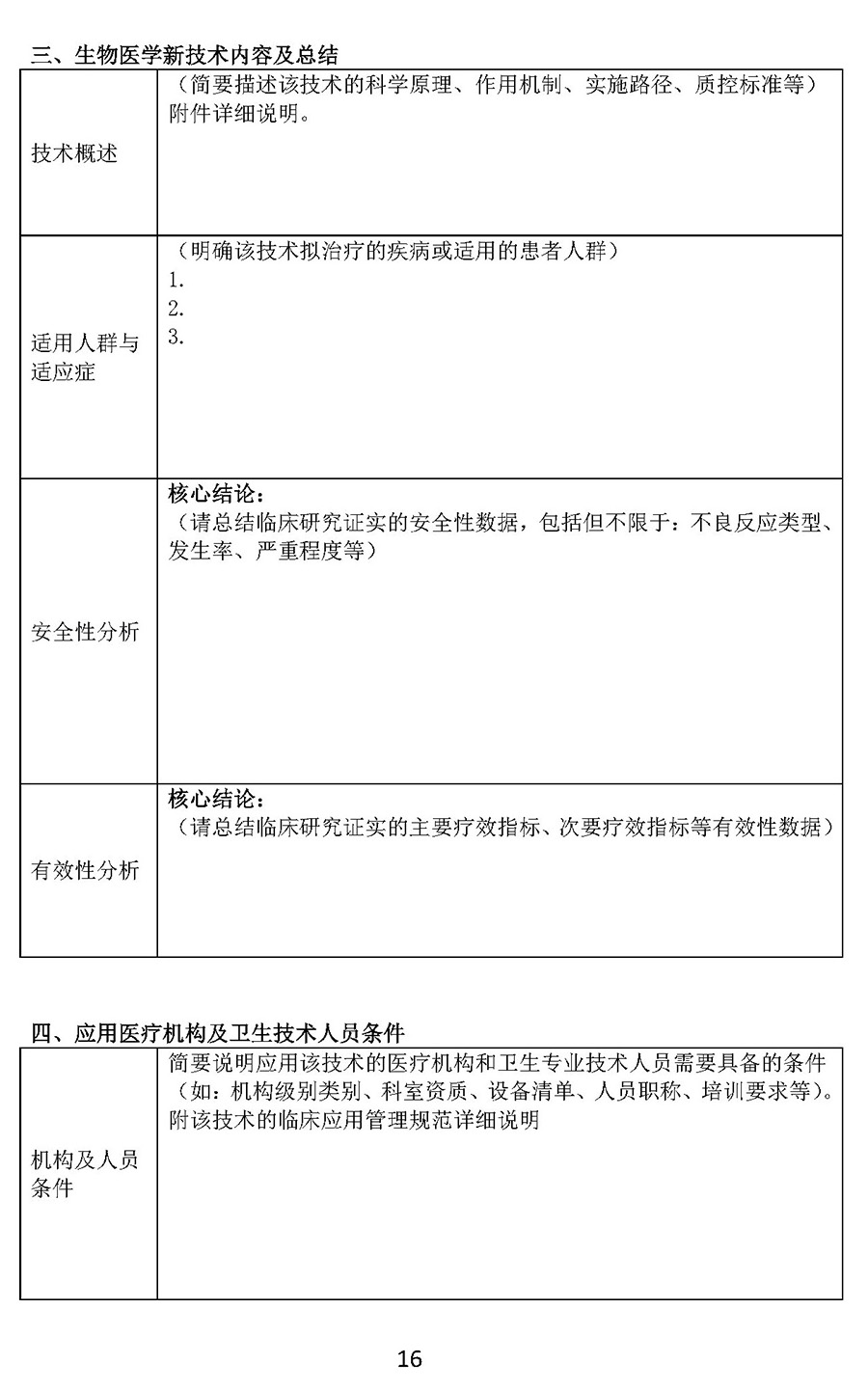
对于“建议批准”的生物医学新技术,由生物中心撰写技术解读材料,随评估报告、应用该技术的医疗机构和卫生专业技术人员需要具备的条件、临床应用操作规范一同上报国家卫生健康委。
对于“建议不予批准”或“终止审查”的技术,由生物中心向申请机构发放《告知书》说明理由。申请机构可以在接到《告知书》15个工作日内,基于已提交的申报材料提出异议,生物中心结合申请机构的异议意见进行评估并反馈申请机构。申请机构对评估结果仍有异议的,生物中心应当组织专家论证,并综合专家论证结果形成最终的审评结论并报国家卫生健康委。
建议“延期再审”的生物医学新技术,由生物中心向申请机构出具《延期再审通知书》,一次性告知补充材料内容及时限。申请机构按要求提交补充材料后,生物中心再次组织评估。
国家卫生健康委自收到生物中心报送的评估意见之日起15个工作日内,作出是否批准的决定。
决定“批准”的生物医学新技术,由国家卫生健康委在官方网站及时发布公告,公布批准的技术名称、风险等级、应用该技术的医疗机构和卫生专业技术人员应当具备的条件以及临床应用操作规范,由生物中心制作《批准通知书》,加盖行政许可专用印章后送达申请机构。
决定“不予批准”或“终止审查”的技术,由生物中心制作《不予行政许可决定书》或《终止审查通知书》,说明理由,并告知申请机构依法申请行政复议或提起行政诉讼的权利和期限,加盖行政许可专用印章后统一送达申请机构。
优先审评
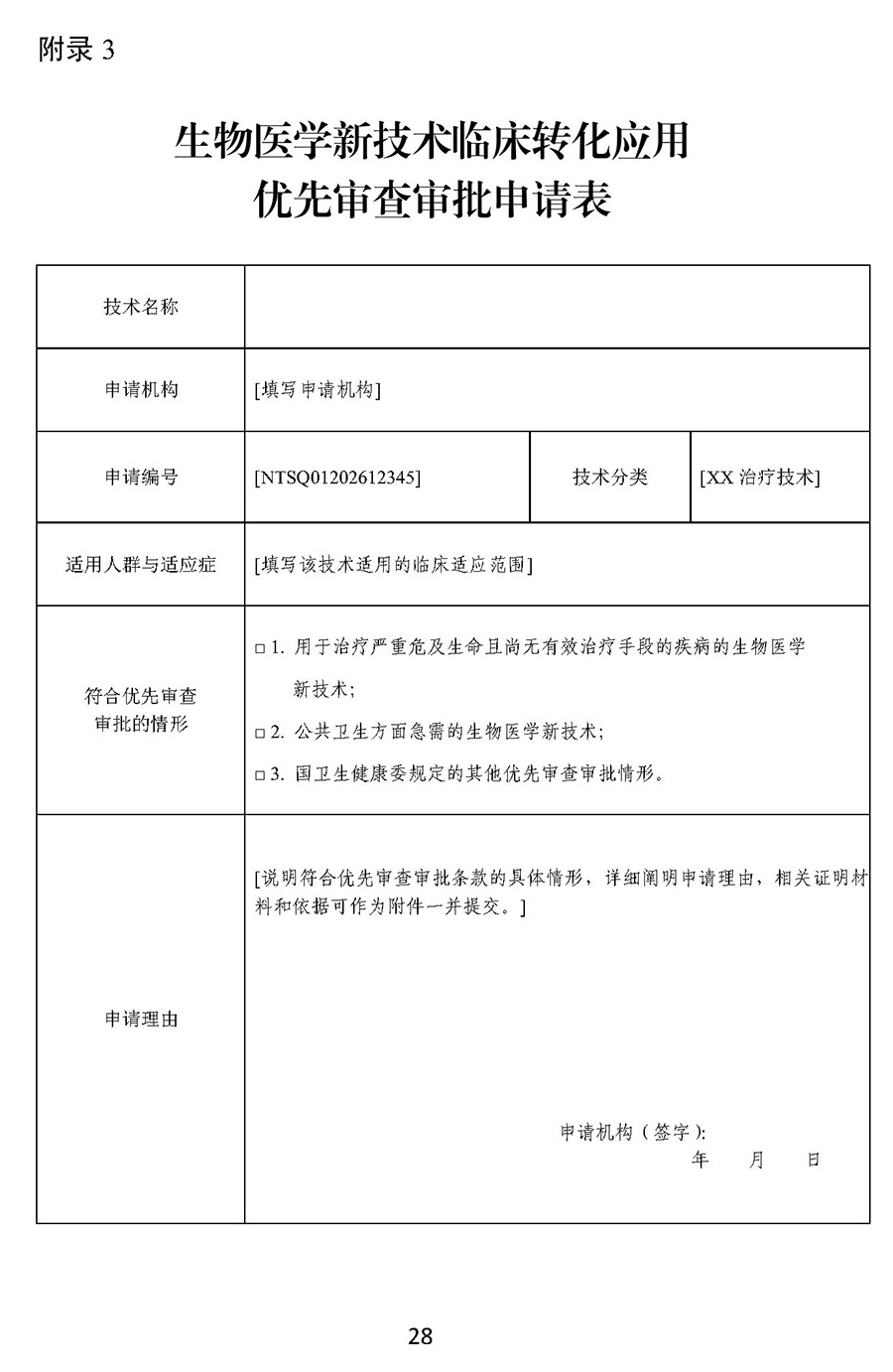
用于治疗严重危及生命且尚无有效治疗手段的疾病以及公共卫生方面急需的生物医学新技术,申请机构可在提出转化应用申请前与生物中心沟通是否符合优先审查审批要求,符合要求的可在提出转化应用申请同时提交优先审查审批申请。
《生物医学新技术风险分级指南》
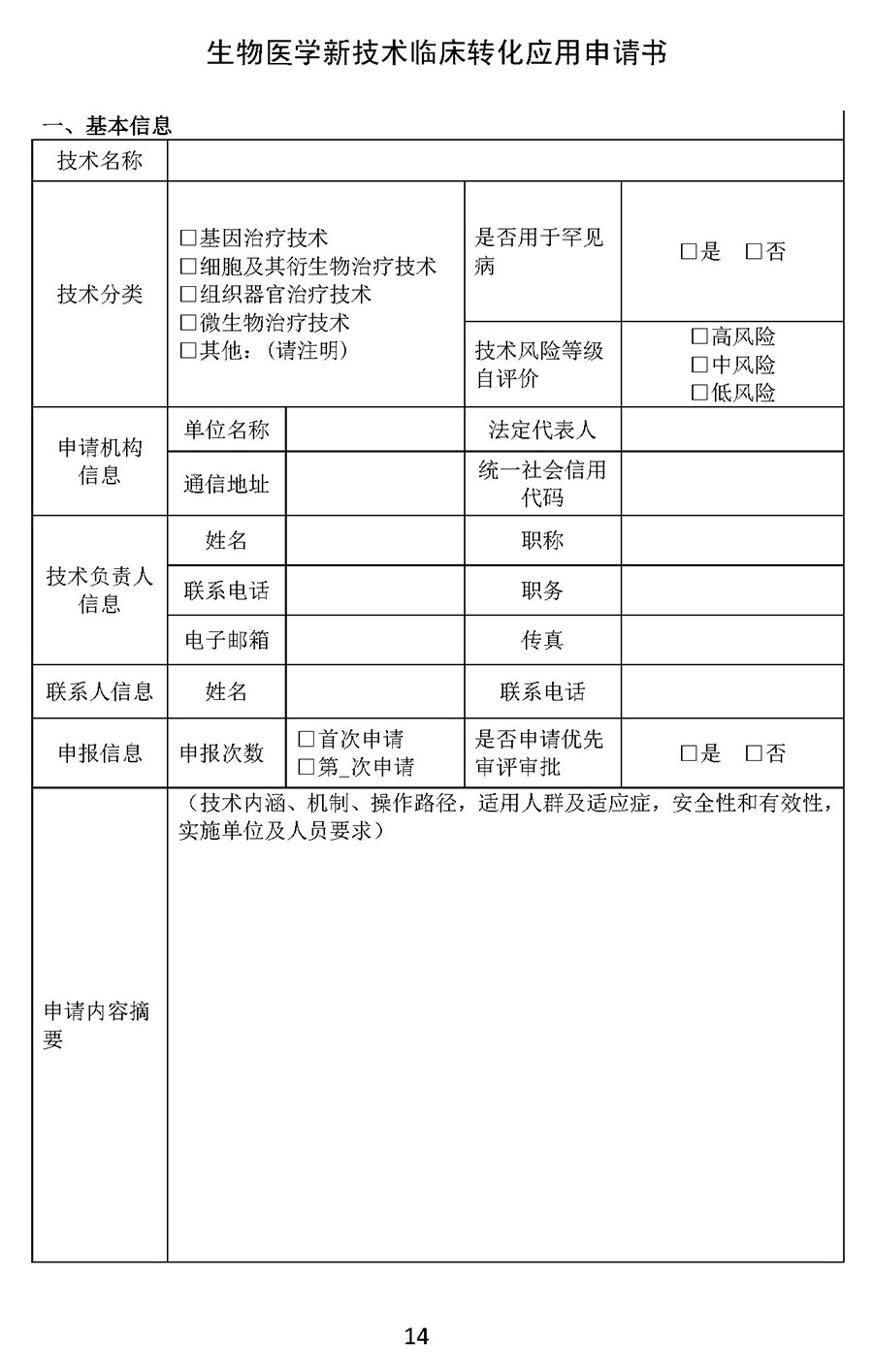
根据征求意见稿,生物医学新技术将分为高风险、中风险和低风险。《生物医学新技术风险分级指南》由生物中心会同医管中心另行制定。申请转化应用的申请人在填写《生物医学新技术临床转化应用申请书》时,需标明是高风险、中风险还是低风险。
在审批通过后,高风险技术批准后5年内、中风险技术批准后3年内、低风险技术批准后1年内仅限在该技术的临床研究机构(含多中心)内开展,各机构每年定期上报应用情况和安全性数据;期满后符合规定或者再评估证实收益远大于风险的,其他符合条件的医疗机构和人员方可按规定使用。
申请转化应用需开展多中心临床验证
《专利法》规定疾病诊疗方法不授予专利权。《条例》规定生物医学新技术临床转化应用获批后,需公布临床应用操作规范,符合条件的机构和人员可以按规定使用。为保障人民群众健康,确保经审批的技术成熟、稳定、可重复,其他机构人员遵守规范应用可获得一致性结果,此次提出多中心独立验证的要求,即要申请临床转化应用的生物医学新技术必须开展多中心临床验证。
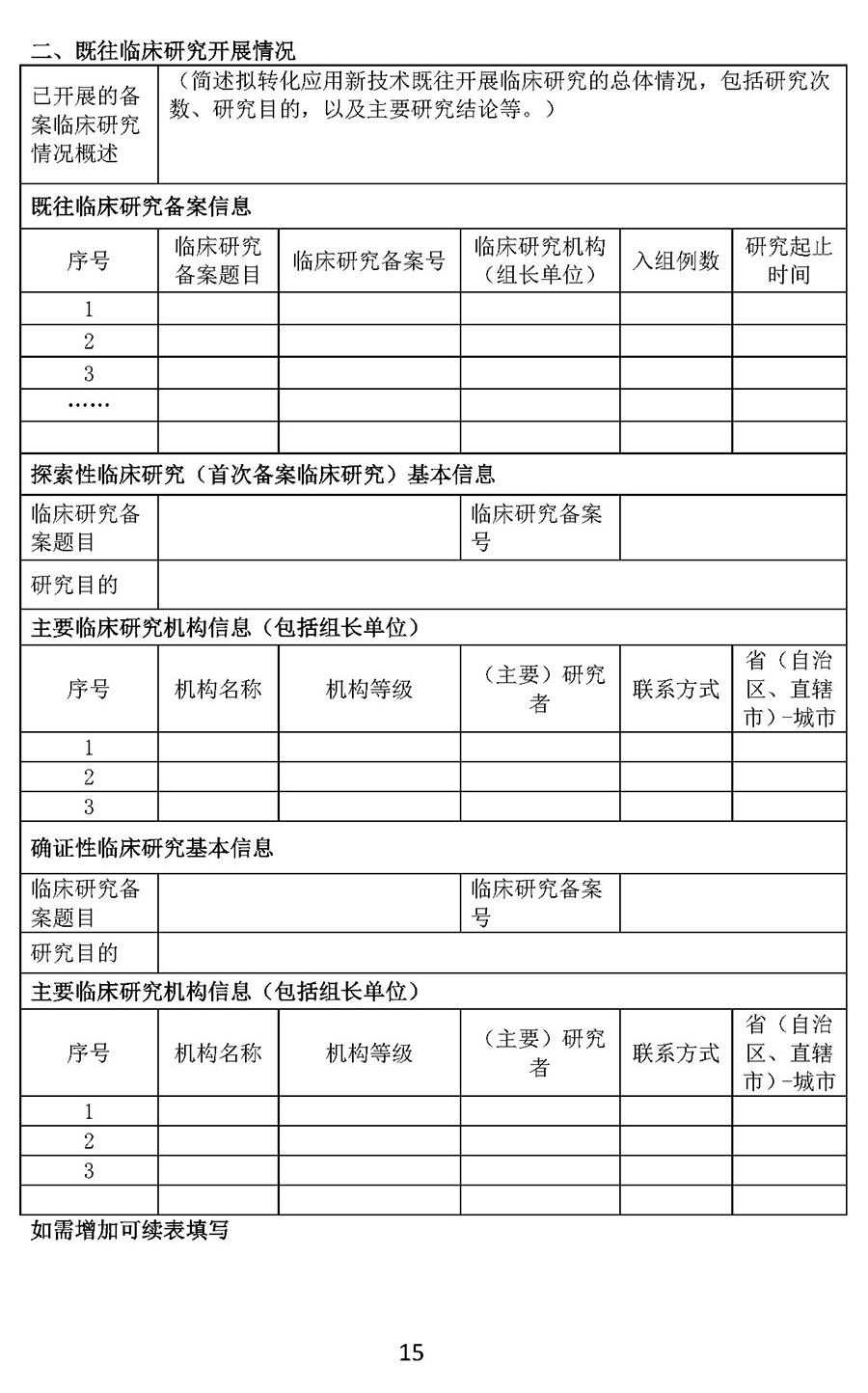
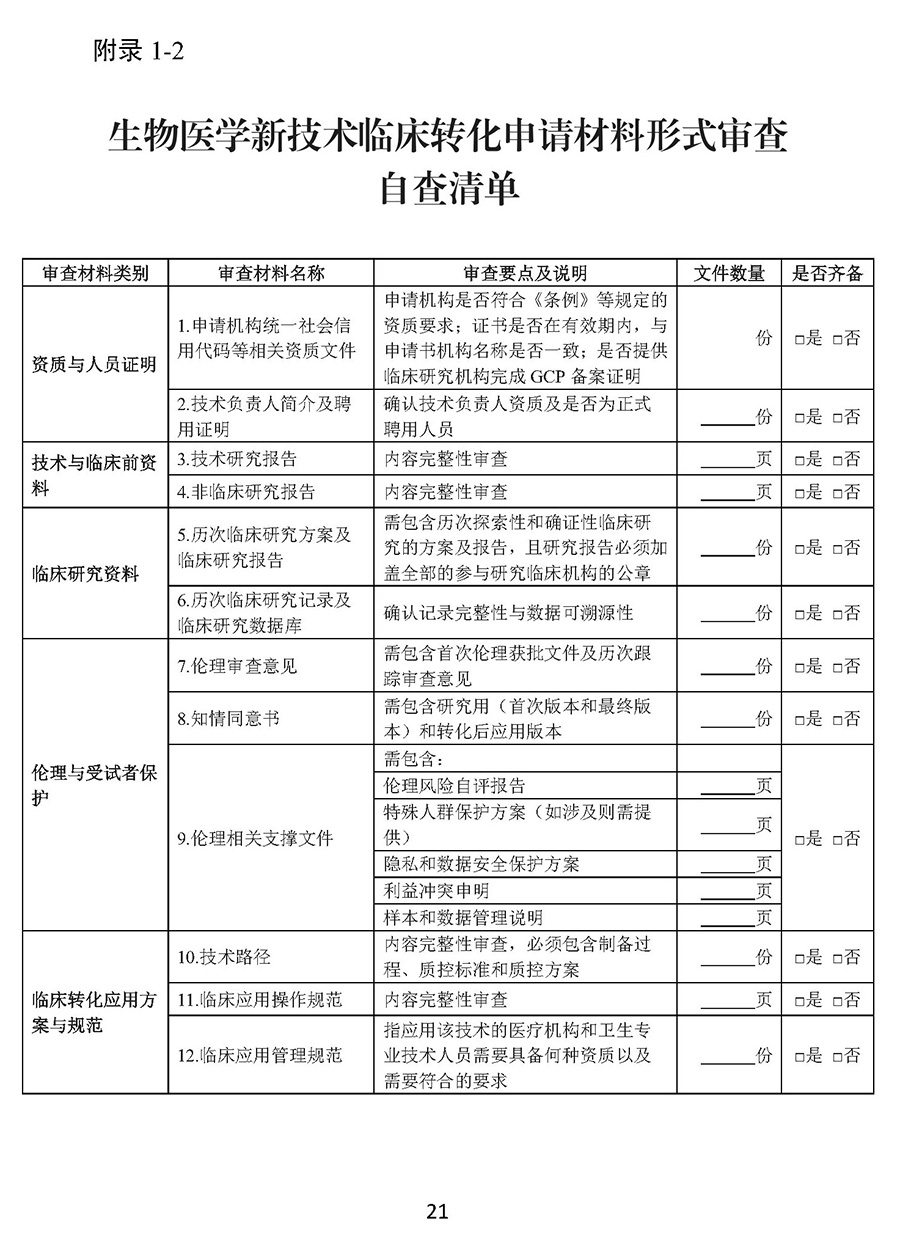
征求意见稿第六条明确生物医学新技术申请临床转化应用,应当同时具备:(一)经依法备案并完成生物医学新技术临床研究;(二)生物医学新技术临床研究证明该技术安全、有效,符合伦理原则;(三)多中心独立验证一致,即符合条件的其他医疗机构和卫生专业技术人员,遵守临床应用操作规范独立实施该技术,可以得到一致的安全性、有效性结论。
本次征求意见稿截止时间为2026年4月25日。
来源:医谷网
为你推荐
 资讯
资讯 国家药监局批准第四代BTK抑制剂洛布替尼片
近日,国家药品监督管理局通过优先审评审批程序,附条件批准广州麓鹏制药有限公司申报的1类创新药洛布替尼片(商品名:麓可达)上市,该药适用于既往接受过至少两种系统性治疗(...
2026-06-05 15:07
 资讯
资讯 开盘大涨 50.22%!抗过敏创新药企上市首日受热捧
6 月 5 日,天辰生物医药(苏州)股份有限公司(证券简称:天辰生物 - B,股票代码:01779 HK)正式于香港联合交易所挂牌上市,依托港股 18A 生物科技企业上市规则登陆资本市场。
2026-06-05 14:30
 资讯
资讯 百度健康AI智慧门诊落地中科大附一院,已规模覆盖近二十家三甲医院
6月5日,百度健康与中国科学技术大学附属第一医院(以下简称“中科大附一院”)正式达成战略合作。双方将围绕AI智慧门诊、医生IP打造、全病
2026-06-05 14:20
 资讯
资讯 出海BD宣布后落地的细节
自2024年以来,出海、BD已成为创新药企响亮的名片。相关数据现实,2025年中国创新药对外授权交易总金额超过1300亿美元,近期又有恒瑞医药与BMS、信达生物与辉瑞、云顶新耀与TVTX...
2026-06-05 09:28
 资讯
资讯 徕卡生物科技与 CellCarta 拓展伴随诊断合作开发模式,加速全球商业化进程
该合作模式旨在适应生物制药企业多样化的研发需求,通过紧密协作与并行推进,建立灵活的全球伴随诊断(CDx)开发框架,助力项目从早期检测开发到商业化诊断的更高效转化。
2026-06-04 19:39
 资讯
资讯 瀚森制药双靶点GLP-1减重产品上市申请获受理
瀚森制药今日发布公告,公司创新药奥莱泊肽注射液上市许可申请(NDA)获中国国家药品监督管理局(NMPA)受理,适用于肥胖或超重成人,奥莱泊肽是一款瀚森制药自主研发的每周一次给药...
2026-06-04 13:40
 资讯
资讯 中国生物技术发展中心:抗原特异性免疫细胞激活新技术临床研究备案指引(第1版)
本指引所指的抗原特异性免疫细胞激活新技术是指将不同类型的抗原或抗原载体注射到人体, 经过抗原递呈细胞识别、 吞噬、 加工处理等过程, 诱导机体内产生抗原特异性的免疫...
2026-06-04 10:54
 资讯
资讯 康方生物发布依沃西联合化疗一线治疗结直肠癌II期期中分析数据
近日,在2026年美国临床肿瘤学会年会(ASCO 2026)上,康方生物对外公布了PD-1 VEGF双特异性抗体新药依沃西联合mFOLFOX6化疗方案,一线治疗不可切除转移性结直肠癌(mCRC)的...
2026-06-04 10:21
 资讯
资讯 冲击港股穿刺消融手术机器人第一股!真健康医疗正式递表
总部扎根广东珠海横琴粤澳深度合作区的真健康医疗,2018 年注册成立,是国内聚焦肿瘤精准微创赛道的高新技术、专精特新小巨人企业,深耕经皮穿刺、消融手术机器人全链条研发生...
2026-06-04 09:48
 资讯
资讯 CDE:关于开发适宜药品包装规格的指导原则
药品适宜的包装规格通常应满足临床用药的功能性、方便性和经济性需要,基于批准的适应症或功能主治、用法用量、用药周期、用药场景等合理设计。
2026-06-03 18:40
 资讯
资讯 甘李药业周制剂胰岛素GZR4注射液第三项关键III期SUPER-3研究完成
6月1日,甘李药业宣布,公司自主创新 1 类生物新药、超长效周制剂胰岛素 GZR4 注射液第三项关键 III 期 SUPER-3 临床试验顺利达到预设主要疗效终点。
2026-06-03 16:00
 资讯
资讯 超11亿美元,云顶新耀新一代 BTK 抑制剂出海
6 月 2 日,云顶新耀发布公告,宣布公司与美国纳斯达克上市罕见病龙头企业 Travere Therapeutics(TVTX)签署独家授权合作协议,将自研管线核心品种希布替尼(EVER001,civ...
2026-06-03 15:22
 资讯
资讯 数因智科落地 Pre-A 轮融资,AI+RNA 双引擎发力,医药消费双赛道迈入商业化加速期
本轮融资由科创板上市生物科技企业嘉必优独家领投,中信建投资本、临港数科基金、闵行金投、康容药业、大零号湾创投等产业资本与国资基金联合跟投
2026-06-02 19:40
 资讯
资讯 EMERALD-3 III期临床试验中,英飞凡与英卓凡联合仑伐替尼和经动脉化疗栓塞术(TACE)将适于栓塞的不可切除肝细胞癌患者疾病进展或死亡风险降低30%
STRIDE方案联合仑伐替尼与TACE呈现积极总生存获益趋势
2026-06-02 19:11
 资讯
资讯 阿里达摩院急性主动脉综合征CT平扫AI诊断软件纳入创新医疗器械特别审查程序
近日,创新医疗器械特别审查申请审查结果公示(2026年第8号)显示,阿里达摩院研发的急性主动脉综合征CT平扫图像辅助分诊软件(DAMO iAorta)已被纳入进入国家药品监督管理局的...
2026-06-02 17:19
 资讯
资讯 众生药业昂拉地韦颗粒纳入优先审评品种名单
6月2日,众生药业发布公告,近日,根据国家药监局药品审评中心发布的公示信息,公司控股子公司广东众生睿创生物科技有限公司自主研发的创新药物昂拉地韦颗粒被CDE纳入优先审评品...
2026-06-02 17:01
 资讯
资讯 原则上每个街道办好1所社区卫生服务中心,国家卫生健康委办公厅发布《关于进一步健全城市社区卫生服务体系 提升服务能力的通知》
实现社区卫生服务中心全覆盖。原则上每个街道办好1所社区卫生服务中心。
2026-06-02 15:59
 资讯
资讯 国家药监局关于医疗器械分类调整有关工作的公告
为加强医疗器械分类管理,根据《医疗器械监督管理条例》《医疗器械注册与备案管理办法》《体外诊断试剂注册与备案管理办法》等相关要求,进一步明确调整医疗器械(含体外诊断试...
2026-06-02 15:45