近年来,癌症免疫治疗在医疗界大放异彩,受到广泛关注。免疫治疗就是通过重新启动并维持肿瘤-免疫循环,恢复机体正常的抗肿瘤免疫反应,从而控制与清除肿瘤的一种治疗方法。包括单克隆抗体类免疫检查点抑制剂、治疗性抗体、癌症疫苗、细胞治疗、小分子抑制剂等。
目前FDA已经批准11个癌症免疫疗法,其中最多的为单克隆抗体类免疫检查点抑制剂如CTLA-4单抗、PD-1/PD-L1单抗,较热的为细胞疗法CAR-T。此外据药智数据,这些获批的疗法中仅有1个在国内上市;6个进口申请已经批准临床,并且进入3期临床;4个没有申请记录,具体如下图所示。
Provenge(sipuleucel-T)
Provenge由总部位于西雅图的Dendreon公司研发而成,2010年4月29日,获得FDA批准了,成为首个用于治疗肿瘤的疫苗。Provenge不是一种预防性疫苗,它与防止感染病毒的麻疹、肝炎疫苗不同。Provenge是一种治疗性疫苗,用于已经被诊断出来的前列腺癌。能令罹患晚期前列腺癌的患者的平均存活时间延长了超过4个月。
Yervoy( Ipilimumab)
Ipilimumab由百时美施贵宝(Bristol-Myers Squibb,BMS)研发,于2011年3月25日获得美国食品药品管理局(FDA)批准, 2011年7月13日获得欧洲药物管理局(EMA)批准上市,并由百时美施贵宝在美国和欧洲市场销售,商品名为Yervoy。Ipilimumab是一种人细胞毒性T淋巴细胞相关抗原4(CTLA-4)阻断剂,能结合CTLA-4,以阻止CTLA-4与其配体(CD80和CD86)的结合。而阻断CTLA-4可以增加T细胞的活性和增殖能力。目前Ipilimumab已经获批7个适应症,其中三个是单独使用,4个为组合疗法,具体如下图所示:
Keytruda(Pembrolizumab)
Pembrolizumab由Merck研发,于2014年9月4日获得美国食品药品管理局(FDA)批准,2015年7月17日获得欧洲药物管理局(EMA)批准上市,并由默沙东在美国和欧洲市场销售,商品名Keytruda。Pembrolizumab是一种程序性死亡受体1(PD-1)阻断剂,能结合PD-1并解除PD-1对T细胞的抑制作用。该药目前批准的适应症共计13个,其中1个为组合疗法,具体如下图所示:
Blincyto(blinatumomab)
Blinatumomab由安进(Amgen)研发,于2014年12月3日获得美国食品药品管理局(FDA)批准,2015年11月23日获得欧洲药物管理局(EMA)批准上市,并由安进在美国市场销售,商品名为Blincyto。Blinatumomab是一种靶向于CD19和T细胞CD3的双特异衔接器,在CD3+T细胞和CD19+的B系淋巴细胞间形成突触,诱导CD19+细胞定向裂解。目前该药已经批准三个适应症,如下图所示。
Opdivo(Nivolumab)
Nivolumab由小野制药(Ono)和百时美施贵宝(Bristol Myers Squibb,BMS)联合研发,于2014年7月4日获得日本医药品医疗器械综合机构(PMDA)批准, 2014年12月22日获得美国食品药品管理局(FDA)批准上,2015年6月19日获得欧洲药物管理局(EMA)批准上市,并由小野制药和百时美施贵宝在美国、欧洲和日本共同销售,商品名为Opdivo。Nivolumab是一种程序性死亡受体1(PD-1)阻断剂,能结合PD-1并解除PD-1通路对T细胞的抑制作用。该药目前共计批准15个适应症,其中有4个为组合疗法,具体如下图所示。目前Opdivo已经于2018年6月15日在中国上市,成为国内第一个上市的PD-1疗法。
Imlygic(talimogene laherparepvec(T-Vec))
安进(Amgen)的Imlygic(Talimogene laherparepvec)于2015年10 月27 日由美国FDA 批准,用于皮肤及淋巴结黑色素瘤病变治疗,该药物也是FDA 批准的首个溶瘤病毒治疗药物,商品名Imlygic。黑色素瘤是一种严重的疾病,它可以进展及扩散到身体其它部位,然后变得难以治疗。
Tecentriq(Atezolizumab)
Atezolizumab由基因泰克(罗氏的子公司)研发,2016年5月18日首次获得FDA批准,商品名Tecentriq。Atezolizumab是一种程序性细胞死亡配体(PD-L1)抑制剂,是FDA批准的首个PD-L1抑制剂。目前共计已经批准3个适应症,具体如下图所示:
Bavencio(avelumab)
Avelumab是一种程序性细胞死亡配体(PD-L1)抑制剂,最初由默克雪兰诺(Merck Serono)开发,于2014年授权于辉瑞(Pfizer),共同进行该药物的研发和商业化。2015年,Avelumab被美国FDA认证为治疗默克尔细胞癌的孤儿药。2017年3月23日获批第一个适应症,紧接着在5月又获批另外一个适应症,商品名Bavencio。具体如下图所示:
Imfinzi(Durvalumab)
Durvalumab由MedImmune公司(阿斯利康的子公司)研发的PD-L1抗体,之后授权给新基公司,用于血液相关癌症的研究。2017年5月1日,美国食品药品监督管理局(FDA)批准了Durvalumab上市,商品名Imfinzi。目前该药共计批准2两个适应症,如下图所示:
Kymriah(tisagenlecleucel)
tisagenlecleucel是诺华公司研发的一种嵌合抗原受体T细胞(CAR -T)疗法,于2017年8月30日,美国FDA批准上市,用于治疗25 岁以下急性淋巴细胞白血病(ALL)的复发或难治性患者,商品名Kymriah。这是全球首个获得批准的CAR-T 疗法,也是美国市场的第一个基因治疗产品,具有里程碑式的意义。CAR-T治疗过程中可能发生的危及生命的副作用,包括细胞因子释放综合征(CRS)以及神经系统毒性。一次治疗费用为47.5万美元。目前该药已经获批2个适应症吗,如下图所示:
Yescarta(axicabtagene ciloleucel)
2017年12月18日,FDA宣布批准了吉利德制药公司(Gilead Science Inc)旗下凯特制药公司(Kite Pharma)的CAR-T疗法Yescarta(axicabtagene ciloleucel)上市,治疗罹患特定类型的大B细胞淋巴瘤成人患者。这些患者曾接受了至少两次其他治疗,但没有出现缓解,或是疾病出现复发。 Axicabtagene ciloleucel(KTE-C19)使患者自身T细胞被设计并表达嵌合抗原受体CAR,靶向CD19抗原,并重新定向T细胞进而杀死肿瘤细胞。值得一提的是,这是美国FDA批准的首款针对特定非霍奇金淋巴瘤的CAR-T疗法,也是第二款获批的CAR-T疗法。
注:部分信息来源于网络公开信息,相关申报信息来源于药智数据
来源:药智网
作者:绿萝
来源:药智网 作者:绿萝
为你推荐
 资讯
资讯 OpenAI 发布首款药物研发专用 AI 模型 GPT-Rosalind
不同于通用大模型,GPT-Rosalind 是 OpenAI 首个针对单一行业构建的前沿推理模型
2026-04-17 15:33
 资讯
资讯 创新泡沫剂型银屑病药物恩适达(卡泊三醇倍他米松泡沫剂)在华获批
是中国首个且目前唯一用于成人斑块状银屑病外用治疗的泡沫剂,专利的起泡装置可帮助患者轻松将药物均匀涂抹于皮肤,包括有毛发的部位。
2026-04-17 15:17
 资讯
资讯 安诺优达三闯港交所:NIPT 龙头转型 IVD 聚焦临床,亏损收窄仍承压
从强调 "一体化生命科学测序解决方案 ",转向 "聚焦临床 IVD、以营销拉动增长 ",并已开始剥离低毛利的检测服务业务,集中资源发展高附加值的 IVD 产品业务。
2026-04-17 12:43
 资讯
资讯 礼来口服小分子GLP-1RA药物orforglipron进一步证实其心血管及整体安全性
ACHIEVE-4: orforglipron迄今随访时间最长的3期研究显示可持续改善心血管代谢健康关键指标
2026-04-17 12:33
 资讯
资讯 国药控股原党委书记、董事长魏玉林以受贿罪判处有期徒刑12年
2026年4月14日,内蒙古自治区阿拉善左旗人民法院一审公开宣判国药控股股份有限公司原党委书记、董事长魏玉林受贿一案,对被告人魏玉林以受贿罪判处有期徒刑十二年,并处罚金人民...
2026-04-17 11:10
 资讯
资讯 国家中医药管理局原局长于文明被提起公诉
被告人于文明利用担任国家中医药管理局副局长职务上的便利以及职权或者地位形成的便利条件,为他人谋取利益,非法收受他人财物,数额特别巨大,依法应当以受贿罪追究其刑事责任。
2026-04-17 11:06
 资讯
资讯 黄果任国家药品监督管理局党组书记
2026年4月16日下午,中央组织部有关负责同志出席国家药品监督管理局领导干部会议,宣布中央决定:黄果同志任国家药品监督管理局党组书记,免去李利同志的国家药品监督管理局党组...
2026-04-16 22:10
 资讯
资讯 拜耳赫新诺(塞伐艾替尼片)治疗HER2突变非小细胞肺癌国内获批
用于治疗存在HER2(ERBB2)激活突变且既往接受过至少一种系统治疗的不可切除的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者
2026-04-16 18:27
 资讯
资讯 主动召回:一家药企的责任选择题
根据国家药监局发布的《药品召回管理办法》,持有人应当主动收集、记录药品的质量问题、药品不良反应 事件、其他安全风险信息,对可能存在的质量问题或者其他安全隐患进行调查...
2026-04-16 16:07
 资讯
资讯 《关于健全药品价格形成机制的若干意见》政策吹风会实录
所谓全周期就是根据药品上市后的不同环节,完善药品的价格政策,对于新上市的药品引入了药品首发价格机制,根据企业对临床价值和创新程度的自评结果,区分高水平创新药、改良新...
2026-04-16 14:18
 资讯
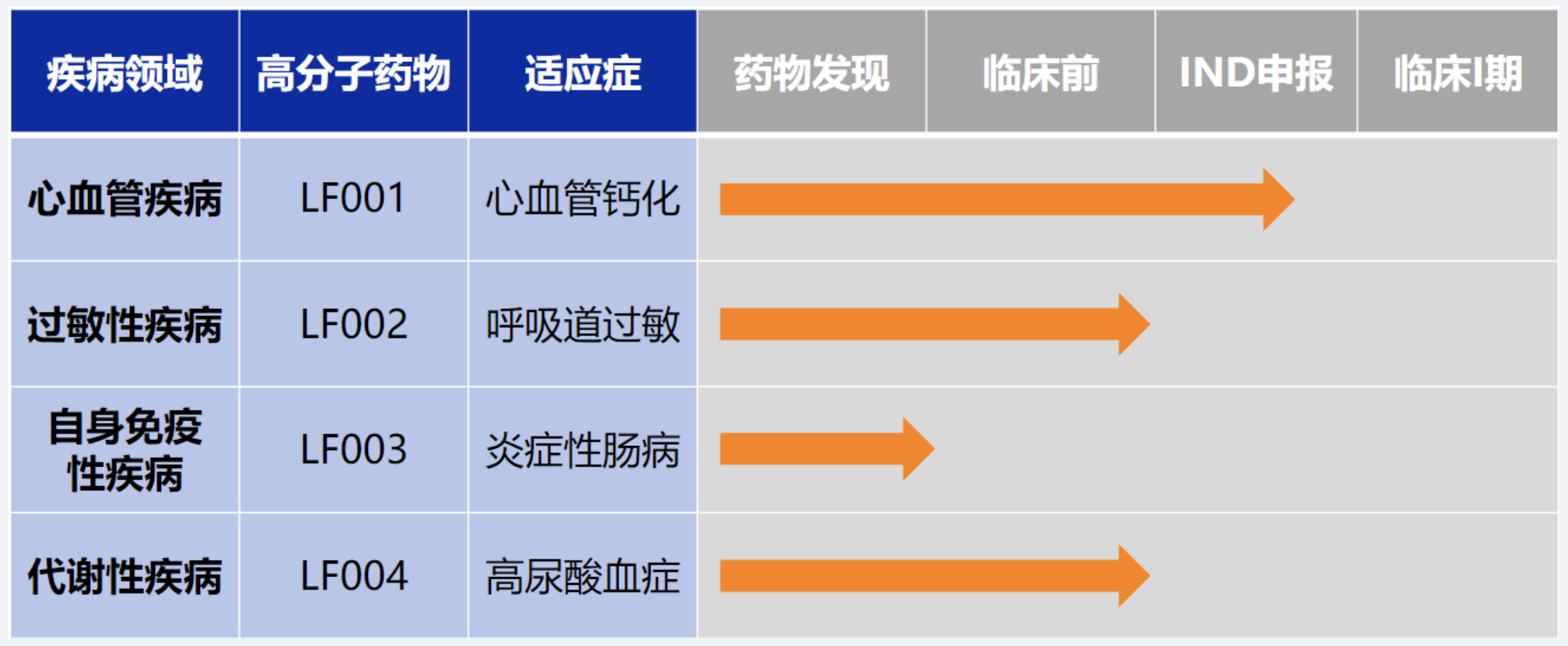
资讯 珞方生物获数千万种子轮融资,深耕高分子创新药开辟慢病治疗新路径
本轮融资由源来资本领投,飞镖创新种子基金跟投,募集资金将主要用于推进首个面向心血管钙化这一慢性疾病的高分子药物管线临床前研究与IND申报
2026-04-16 12:55
 资讯
资讯 创新药价格重磅文件,多部委将举办政策吹风会
4月14日,国办正式对外发布备受业内关注的《关于健全药品价格形成机制的若干意见》。该文件曾在去年2月份对外发布了征求意见稿,此后1年间,业内普遍关注该《意见》何时正式落地。
2026-04-14 22:37
 资讯
资讯 映恩生物拟登陆科创板,募资不超67.5亿元加码ADC研发
根据公告,映恩生物-B此次科创板IPO拟发行不超过1577 9190万股人民币股份,占发行后总股本的15%(不含超额配股权)
2026-04-14 19:26
 资讯
资讯 华东医药司美格鲁肽注射液减重适应症上市申请获受理,剑指GLP-1千亿蓝海
公司全资子公司杭州中美华东制药江东有限公司收到国家药品监督管理局(NMPA)签发的《受理通知书》,司美格鲁肽注射液上市许可申请获得受理,适用于在控制饮食和增加体力活动的...
2026-04-14 19:03
 资讯
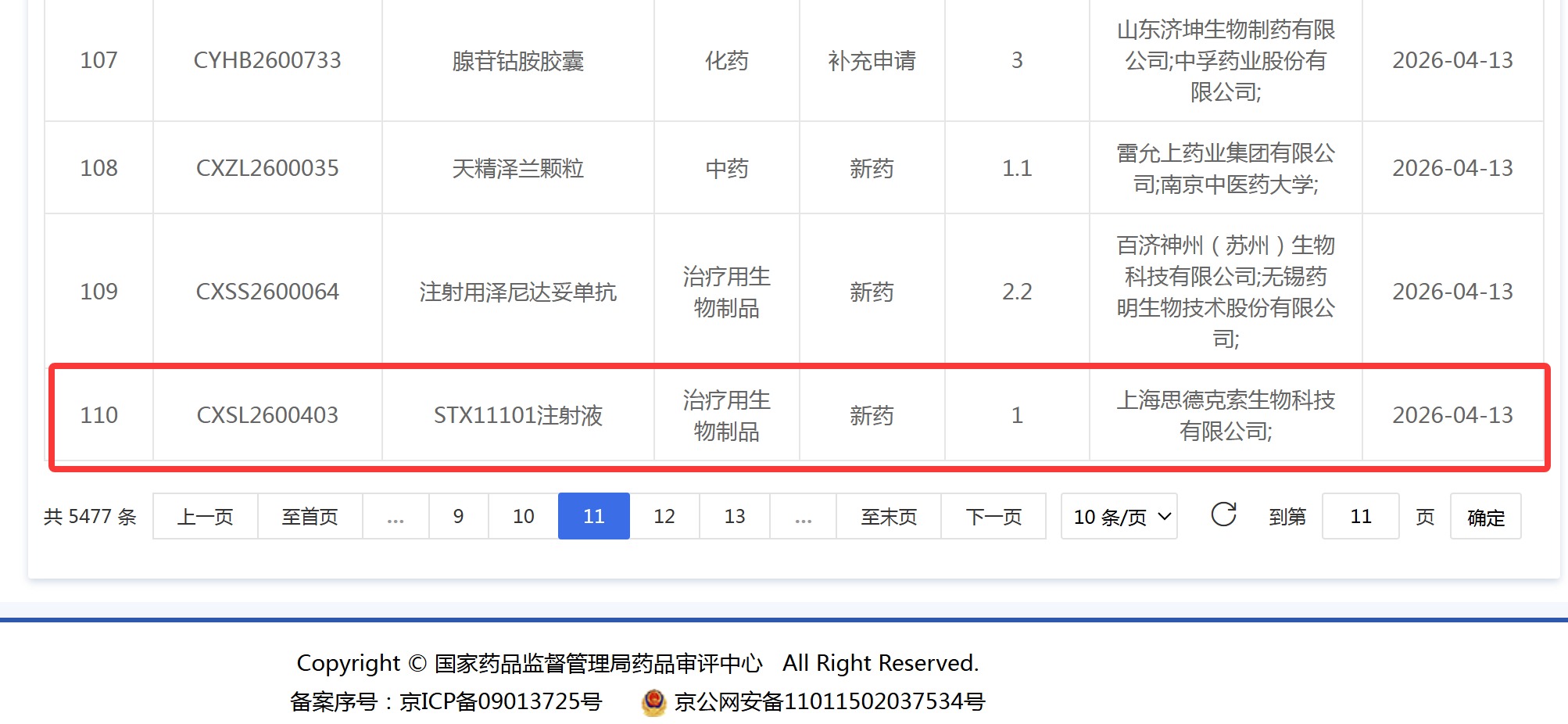
资讯 全国首款外泌体创新药申报IND
国家药监局药品审评中心(CDE)官网显示,4月13日,上海思德克索生物科技有限公司申报的STX11101注射液新药临床试验申请(IND)正式获得受理,受理号为CXSL2600403,药品类型为...
2026-04-14 18:11