完全理解PD-1/PD-L1通路机制还需要很长的路要走,目前关于如何最好地利用PD-L1表达作为免疫疗法预后目的的生物标志物已经引起了颇多争议,因为在不同的肿瘤中,临床试验呈现了不同的结果。
1.很晚起步
中国五种最常见的癌症(肝癌、肺癌、乳腺癌、结直肠癌和胃癌)都是免疫检查点阻断的目标。然而,五个全球上市的PD-1/PD-L1抑制剂并没有在中国开展任何临床研究,直到2014年10月,默沙东才首次在中国启动了一项名为KEYNOTE 042的试验,以评估pembrolizumab一线治疗非小细胞肺癌的疗效。跨国药企主要聚焦在把处于三期临床阶段的国际多中心临床试验(MRCT)扩展到中国大陆。
clinicaltrials.gov数据显示,截止到2018年4月9日,已有40个关于PD-1/PD-L1抑制剂的MRCTs将中国纳入了试验范围。除此之外,还有包括16项专门在中国开展的临床试验。在已经获批的五个PD-1/PD-L1抑制剂中,只有辉瑞/默克雪兰诺的avelumab没有公开登记在中国大陆的临床试验信息,不过GBI SOURCE数据显示,已经有三项与avelumab相关的临床试验获得了CFDA的批准。根据现有数据,跨国药企在中国研究最多的适应症是非小细胞肺癌,共有19项(见表1和表2)。
BMS一直致力于将nivolumab在中国进行本地化开发,该公司已在中国启动了14个临床试验。2017年11月,BMS已经在中国提交了nivolumab的上市申请,并被纳入优先审评程序,这也是第一个在中国提交的PD-1/PD-L1类抗体药上市申请。
BMS中国部门负责人Karl Lintel曾在2016年3月的一次新闻发布会上表示:像nivolumab这样的创新药物将会在中国市场的竞争中起到关键的作用。Lintel指出,无论是在适应症的选择,还是联合用药方面,nivolumab在中国的研发策略可能会不同于全球模式,这主要取决于具体的临床试验证据。
BMS在2017年9月举办的2017中国抗癌协会临床肿瘤学协作专业委员会(CSCO)上公布了CheckMate-077研究的初步结果,CheckMate-077是旨在评估nivolumab在中国经治晚期或复发实体瘤患者中使用情况的研究。结果显示,中国实体瘤患者在接受Nivolumab治疗后耐受性良好。
此外,BMS也在尽力探索nivolumab和其它疗法联合用药的效果,在已经开始招募的14个临床试验研究中,有7个是该药与CTLA-4抑制剂ipilimumab或化疗的联合用药。相比之下,默沙东主要将pembrolizumab作为单药疗法进行评估,pembrolizumab只有一项研究是与其它药物联合用药的,就是与化疗一起用于NSCLC的一线治疗。
中国药物审评审批的因素也使得阿斯利康和罗氏公司的PD-L1抑制剂durvalumab和atezolizumab追赶了上来。 阿斯利康正在充分利用其CTLA-4抑制剂tremelimumab的优势,在durvalumab的9项公开登记的临床试验中,有7项都有tremelimumab的参与。
与此同时,罗氏也在积极探索atezolizumab的联合疗法效果,除了与去势抵抗性前列腺癌治疗药物enzalutamide进行联合用药外,在16项试验中,有5项都是研究atezolizumab与化疗联合治疗效果。
2.民族特异性问题
跨国药企对临床研究本土化的承诺反映在了MRCT试验设计中。针对不同地区的病人采用相同的试验方案是行不通的。中国医学专家曾表示,中国患者人群的一些特殊性可能使他们在免疫检查点抑制剂的MRCTs招募中面临被排除在外的风险,例如肝炎高发,或者同时使用中药等等。
广东肺癌研究所的吴一龙教授建议:可以对中国患者进行更大范围的调查以研发针对中国患者的免疫疗法,例如可以把患者的基因谱、化疗治疗效果、毒性情况等因素考虑在内。
特别是对于肺癌,中国患者中的种族异质性和治疗反应是众所周知的。亚洲NSCLC人群中较高的表皮生长因子受体(EGFR)突变率(中国约为50%VS西方人群约为20%)正是开发易瑞沙(吉非替尼)等第一代靶向酪氨酸激酶抑制剂(TKI)的基础。
不幸的是,迄今为止,免疫疗法在EGFR阳性的肿瘤患者中治疗效果并不理想。从有限的公开数据中可以看出,前期开展的PD-1 / PD-L1在EGFR突变的NSCLC患者以及间变性淋巴瘤激酶(ALK)阳性转移性NSCLC患者中的研究并未取得令人满意的结果。因此,跨国药企在中国开展的PD-1/PD-L1临床试验大部分都集中在了EGFR/ALK野生型疾病上。
当然,也有一些探索免疫疗法和TKI疗法联合疗法的研究。阿斯利康正在开展一项评价durvalumab与其第三代EGFR TKI 泰瑞沙(奥希替尼)联合疗法效果的研究,该研究中也有中国患者参与(2014年8月开始; NCT02143466)。
虽然该试验的结果尚未公布,但从其他相关研究公开的有限数据得知,免疫检查点抑制剂与EGFR-TKI联用会对患者产生毒性作用,这样的结果也使针对该联合疗法的进一步临床研究陷入了争议之中。
3.EGFR和PD-L1紧密联系
科学家们对于EGFR和PD-L1在肿瘤微环境中表达之间复杂关系的研究从未停止,最近的一些研究进展揭示了免疫疗法的另一个潜在应用途径。研究已经发现,EGFR可以上调肺癌中的PD-L1表达水平,这开启了科学家们关于PD-L1表达可能是靶向疗法、化疗以及免疫疗法的预后因子的研究。
福建医科大学的一个研究小组发现EGFR-TKI对PD-L1表达阳性的EGFR突变型肺癌患者拥有更好的治疗效果,而且PD-L1表达水平在对吉非替尼产生耐药性的患者中显着增高。
一种假设认为肿瘤对EGFR-TKIs的抵抗性可能依赖于PD-1/PD-L1途径的免疫逃避机制,这表明免疫疗法很可能是接受过EGFR靶向治疗后的患者的最佳后续疗法。
BMS正在一项国际III期MRCT研究CheckMate722中评估nivolumab(联合伊匹单抗或化疗)对已经接受过TKI治疗的EGFR阳性NSCLC患者(限T790M阴性患者)的疗效。该研究包括中国大陆14个试验机构和香港的4家医院;在香港的患者招募工作已经在进行中,预计将在2019年10月得到初步数据。
完全理解PD-1/PD-L1通路机制还需要很长的路要走,目前关于如何最好地利用PD-L1表达作为免疫疗法预后目的的生物标志物已经引起了颇多争议,因为在不同的肿瘤中,临床试验呈现了不同的结果。
中国的研究人员也在这一领域做出了重大贡献,尤其是在调查种族特异性方面。复旦大学上海癌症研究中心的研究人员最近发表的一项研究表明,与西方患者相比,东亚肺癌患者的PD-L1表达水平非常低,这也可能是另外一个限制中国患者用免疫检查点抑制剂治疗的因素。
目前多家药物开发商正在致力于解决此问题,据报道,江苏恒瑞医药正在开展一项II期临床研究,以在中国NSCLC患者中确定可以用免疫检查点抑制剂治疗的PD-L1表达水平的最佳临界值。同时,罗氏正在用第二代测序技术(NGS)来确定NSCLC患者中T细胞抗原受体(TCR)的表达量,因为TCR可能成为指导atezolizumab临床应用的潜在生物标志物。
4.中国扫除MRCT申请障碍
目前正在开发的第一代PD-1/PD-L1抑制剂很可能是最后一批在中国上市时间落后于世界其它地方3~5年的例子。不过,对于政府而言,没有足够的病人能够用得起这种昂贵的疗法依然是一个敏感的问题。因为在美国,PD-1/PD-L1疗法每年约需要30万美元的花费,因此即便该种疗法推出市场,除了富人外,大部分人还是无法支付得起这么昂贵的疗法。
在过去的18个月里,虽然nivolumab和pembrolizumab已经在韩国、中国台湾、印度、澳大利亚、新西兰和新加坡等多个地区获批上市,但在中国,目前尚未有PD-1/L1类药物获批上市。
不过,2017年3月,CFDA批准海南博鳌勒城国际医疗旅游试验区内的海南省肿瘤医院成美国际医学中心可以进口包括Keytruda在内的抗癌药,以便中国患者可以在这些进口药上市之前提前用上国外的先进疗法。
自从2017年6月,CFDA正式加入国际人用药品注册技术协调会(ICH),成为其全球第8个监管机构成员以来,CFDA就一直在努力推动中国的药品注册技术标准早日与国际标准接轨。
以前,境外申请人在中国申请开展国际多中心药物临床试验(MRCT)的药物,必须是已在境外注册或者已经进入II期或III期临床试验。
而2017年10月,CFDA发布的新规表示,允许进口药(预防用生物制品除外)在中国境内外同步开展Ι期临床试验,取消开展MRCT的药品此前的“三报三批”流程和部分进口药品在境外上市的要求。此外,2018年1月底,CFDA还发布公告称,自2018年2月1日起,将逐步开始适用五个ICH二级指导原则。
PD-1/PD-L1抗体药物在中国患者中应用的复杂性也表明这种改革的必要性。随着改革的进行,中国缺乏Ⅰ期临床试验机构的历史难题将会被解决,不过,CFDA也已准备将临床试验机构资格认定改为备案管理,允许临床试验承办者自由选择场地,并培训当地的研究人员。
目前,中国领先的临床试验机构已具备世界级的研发能力,并广泛参与到全球型Ⅲ期临床试验研究中。例如,由31家顶级医院组成的中国胸部肿瘤研究协作组(CTONG)现在已经有能力开展与免疫治疗等高度相关的基因变异型疾病的篮子试验(Basket Trial)。在接下来的12个月,跨国药企将会陆陆续续地发布临床试验数据,随着这一尚在萌芽阶段的治疗方法的发展,免疫疗法这个市场必将越来越重要。
来源:E药经理人
作者:邓改芳
来源:E药经理人 作者:邓改芳
为你推荐
 资讯
资讯 创新药价格重磅文件,多部委将举办政策吹风会
4月14日,国办正式对外发布备受业内关注的《关于健全药品价格形成机制的若干意见》。该文件曾在去年2月份对外发布了征求意见稿,此后1年间,业内普遍关注该《意见》何时正式落地。
2026-04-14 22:37
 资讯
资讯 映恩生物拟登陆科创板,募资不超67.5亿元加码ADC研发
根据公告,映恩生物-B此次科创板IPO拟发行不超过1577 9190万股人民币股份,占发行后总股本的15%(不含超额配股权)
2026-04-14 19:26
 资讯
资讯 华东医药司美格鲁肽注射液减重适应症上市申请获受理,剑指GLP-1千亿蓝海
公司全资子公司杭州中美华东制药江东有限公司收到国家药品监督管理局(NMPA)签发的《受理通知书》,司美格鲁肽注射液上市许可申请获得受理,适用于在控制饮食和增加体力活动的...
2026-04-14 19:03
 资讯
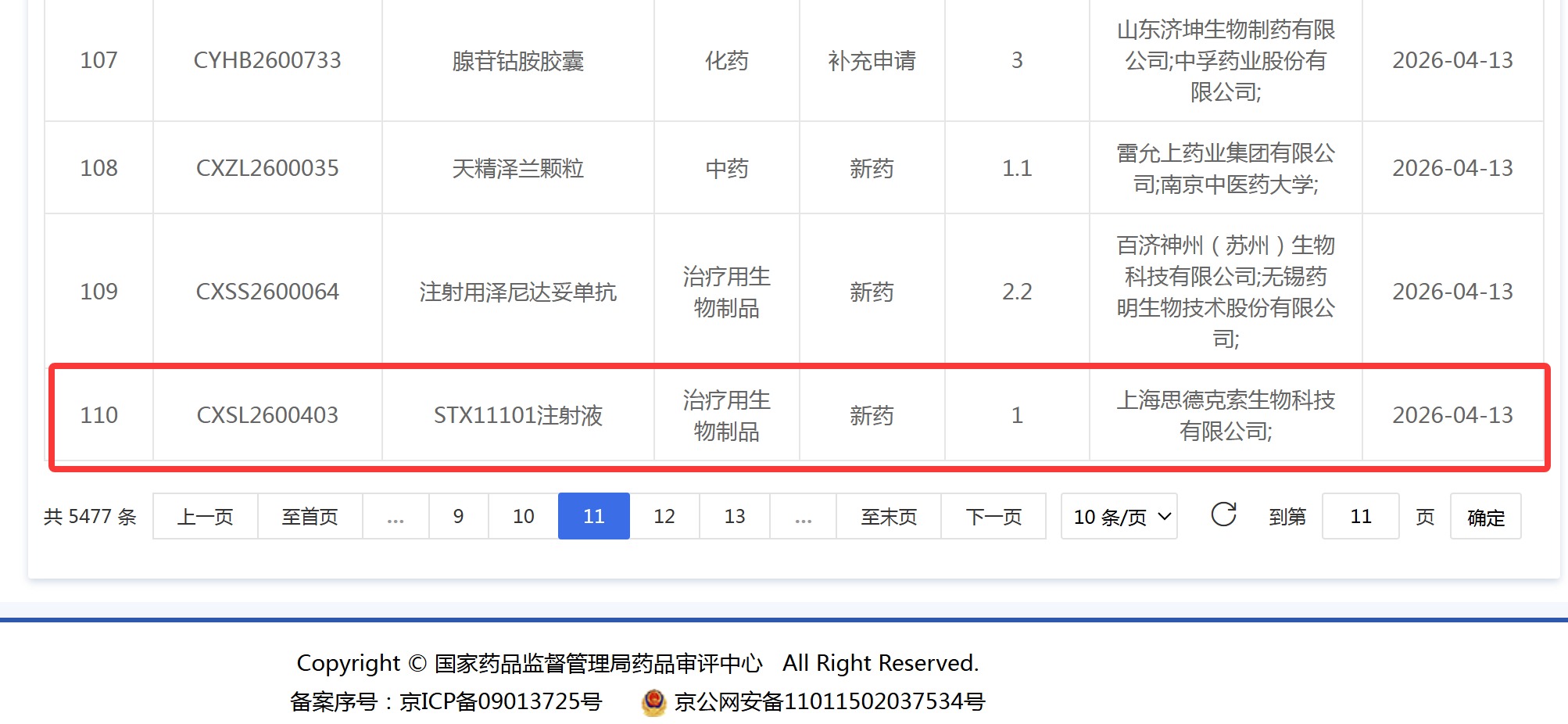
资讯 全国首款外泌体创新药申报IND
国家药监局药品审评中心(CDE)官网显示,4月13日,上海思德克索生物科技有限公司申报的STX11101注射液新药临床试验申请(IND)正式获得受理,受理号为CXSL2600403,药品类型为...
2026-04-14 18:11
 资讯
资讯 安永发布《“本土药企盈利引擎”模型1.0 ——供应链与财务篇》医药白皮书
安永大中华区(后简称:安永)重磅发布《穿越盈利的迷雾:安永“本土药企盈利引擎”模型1 0 ——供应链与财务篇》医药白皮书。
2026-04-14 17:50
 资讯
资讯 31款药品,第一批参照药预沟通药品信息公示
近日,国家医保局发布第一批参照药预沟通药品信息公示。根据公示信息,此次公布的药品信息为截至3月底收到的拟纳入首次预沟通工作范围的企业申请药品名单。
2026-04-14 15:36
 资讯
资讯 授权许可费最高至7.45亿美元,海思科与艾伯维达成一项BD交易
4月13日,海思科宣布日前与美国艾伯维(AbbVie Group Holdings Ltd )签订独占许可协议,授予AbbVie在除中国大陆、香港特别行政区及澳门特别行政区以外的全球范围开发、生产...
2026-04-13 16:09
 资讯
资讯 创业板新增第四套上市标准,无盈利要求
4月10日,中国证监会发布《关于深化创业板改革 更好服务新质生产力发展的意见》,旨在优化发行上市标准提高包容性和吸引力,更好服务实体经济高质量发展,助力高科技创新。
2026-04-12 16:36
 资讯
资讯 降低医疗医药行贿入罪门槛,两高《解释(二)》发布
4月10日,最高人民法院、最高人民检察院共同发布《关于办理贪污贿赂刑事案件适用法律若干问题的解释(二)》(以下简称“《解释(二)》”),这是对2016年发布《关于办理贪污贿...
2026-04-12 12:10
 资讯
资讯 百济神州DLL3/CD3双抗安泰适(注射用塔拉妥单抗)附条件批准上市
4月10日,百济神州公司宣布,安泰适(注射用塔拉妥单抗)经优先审评程序获得国家药品监督管理局(NMPA)附条件批准,用于既往接受过至少2种系统性(包括含铂化疗)失败的广泛期...
2026-04-10 19:28
 资讯
资讯 蔚程医药超额完成 5400 万美元 A 轮融资,全面加速肝外递送小核酸疗法临床转化
本轮融资由启明创投与一家知名产业基金联合领投,弘晖基金、一家知名投资基金、泰福资本共同参与投资,原有投资方杏泽资本持续追加投资
2026-04-10 13:06
 资讯
资讯 诠释重疾诊疗新范式,西门子医疗携创新成果亮相2026 CMEF
今日,西门子医疗以“创新境,为每一个生命”为主题,重磅亮相第93届中国国际医疗器械博览会(CMEF)。
2026-04-09 15:33
 资讯
资讯 磅策医疗完成亿元 B 轮战略融资,加速 AI 手术机器人与消费医疗全球化布局
本轮融资由一家国际 AI 科技公司领投,联想创投等老股东持续加码跟投,资金将重点用于核心技术迭代、新产品管线研发与临床注册、商业化渠道拓展及全球化商业布局
2026-04-09 12:38
 资讯
资讯 吉利德预防HIV感染新药拟纳入优先审评
4月7日,国家药品监督管理局药品审评中心(CDE)官网显示,吉利德科学(Gilead Sciences)来那帕韦钠片和来那帕韦钠注射液新适应症拟纳入优先审评。
2026-04-09 09:28
 资讯
资讯 因药品生产存在严重缺陷,一药品被取消国家药品集采中选资格
近日,国家组织药品联合采购办公室发布公告,取消广州合和医药有限公司美索巴莫注射液中选资格,同时将广州合和医药有限公司和委托生产企业成都天台山制药股份有限公司列入违规...
2026-04-07 13:23
 资讯
资讯 上海市药监局核发上海首张干细胞《药品生产许可证》
近日,上海市药监局核发上海地区的首张干细胞《药品生产许可证》,上海爱萨尔生物医药股份有限公司也因此成为今年首位获该证的企业。
2026-04-07 11:56
 资讯
资讯 甘李药业一款PROTAC药物完成临床试验I期首例入组
4月3日,甘李药业(603087 SH)发布公告称,其自主研发的GLR2037于近日成功完成Ⅰ期临床试验首例受试者给药。本次临床试验拟开展的适应症为晚期前列腺癌。
2026-04-05 19:55






![远大医药钇[90Y]微球注射液美国临床达终点,局部肿瘤控制率达100%](https://img.medvalley.cn/2026/0413/1776086367155426.png)
