报告来源:国家食品药品监督管理局
一、药品批准生产上市情况
2011年,共批准药品注册申请718件。其中批准境内药品注册申请644件,批准进口74件。在644件境内药品注册申请中,化学药品569件,占88.4%;中药50件,占7.8%;生物制品25件,占3.8%。
从注册分类看,境内药品注册申请中,新药149件,占22.9%;改剂型59件,占9.3%;仿制药436件,占67.7%。与2010年相比较,批准化学药品仿制药品的数量减少,批准新药的数量增加,其中,1.1类化学药品共批准10件,相比2009年及2010年有显著增长。
表1 2011年批准的药品情况
注:“其他”指按《药品注册管理办法》(2005年版)分类申报的一、二、三、四类药品。数量以受理号计。
表3 2011年批准的中药新药分布
注:“其他”指按《药品注册管理办法》(2005年版)分类申报的三类药品。数量以受理号计。
表4 2011年批准的1.1类新药
药品名称 注册类别 剂 型 生产企业 艾瑞昔布 化药1.1类 原料药 江苏恒瑞医药股份有限公司 艾瑞昔布片 化药1.1类 片剂 江苏恒瑞医药股份有限公司 盐酸埃克替尼 化药1.1类 原料药 浙江贝达药业有限公司 盐酸埃克替尼片 化药1.1类 片剂 浙江贝达药业有限公司 艾拉莫德 化药1.1类 原料药 先声药业有限公司 艾拉莫德片 化药1.1类 片剂 先声药业有限公司 吡非尼酮 化药1.1类 原料药 上海睿星基因技术有限公司 吡非尼酮胶囊 化药1.1类 胶囊剂 上海睿星基因技术有限公司 托伐普坦片 化药1.1类 片剂 浙江大冢制药有限公司 托伐普坦片 化药1.1类 片剂 浙江大冢制药有限公司
二、药物临床研究批准情况
2011年,共批准621个注册申请开展临床研究。其中39个为注册分类1类的化学药品注册申请,110件为国际多中心临床研究申请。批准进入临床试验的药物,既涵盖在我国疾病谱中占重要位置的常见疾病和多发疾病,如肿瘤、心血管病等的治疗药物,也包括了社会影响度高的一些罕见性疾病的治疗药物。对于符合《新药注册特殊审批管理规定》要求的,按照特殊审批程序开展审评审批,促进药物研究进程。
来源:国家食品药品监督管理局
为你推荐
 资讯
资讯 礼邦医药 AP306 出海
根据协议,礼邦医药已授予 R1 在大中华区以外地区独家开发、生产及商业化 AP306 的权利。协议项下的整体经济条款包括最高总计过亿美元的开发、注册及商业化里程碑付款;同时...
2026-03-18 15:59
 资讯
资讯 百度健康计划近期推出DoctorClaw
据悉这是一款面向医生的OpenClaw,定位是医生AI助理,可以帮医生自动整理研究资料、跟踪论文进度、设置随访提醒、定时追踪最新文献等。
2026-03-18 11:45
 资讯
资讯 传奇生物被传拟赴港上市
日前有媒体报道引述知情人士称,传奇生物拟赴港上市,最早将于今年(2026年)落地,募资规模约3亿至4亿美元(约折合港元23 4亿至31 2亿)。对此,3月17日,传奇生物方面表示,...
2026-03-17 13:20
 资讯
资讯 男子回家遭自家狗撕咬,伤口深可见骨!专家紧急提醒:暴露后规范处置是关键
狂犬病是由狂犬病病毒引起的一种以侵犯中枢神经系统为主的急性人兽共患传染病。其主要临床表现为特异性恐风、恐水、咽肌痉挛、进行性瘫痪等。
2026-03-17 12:42
 资讯
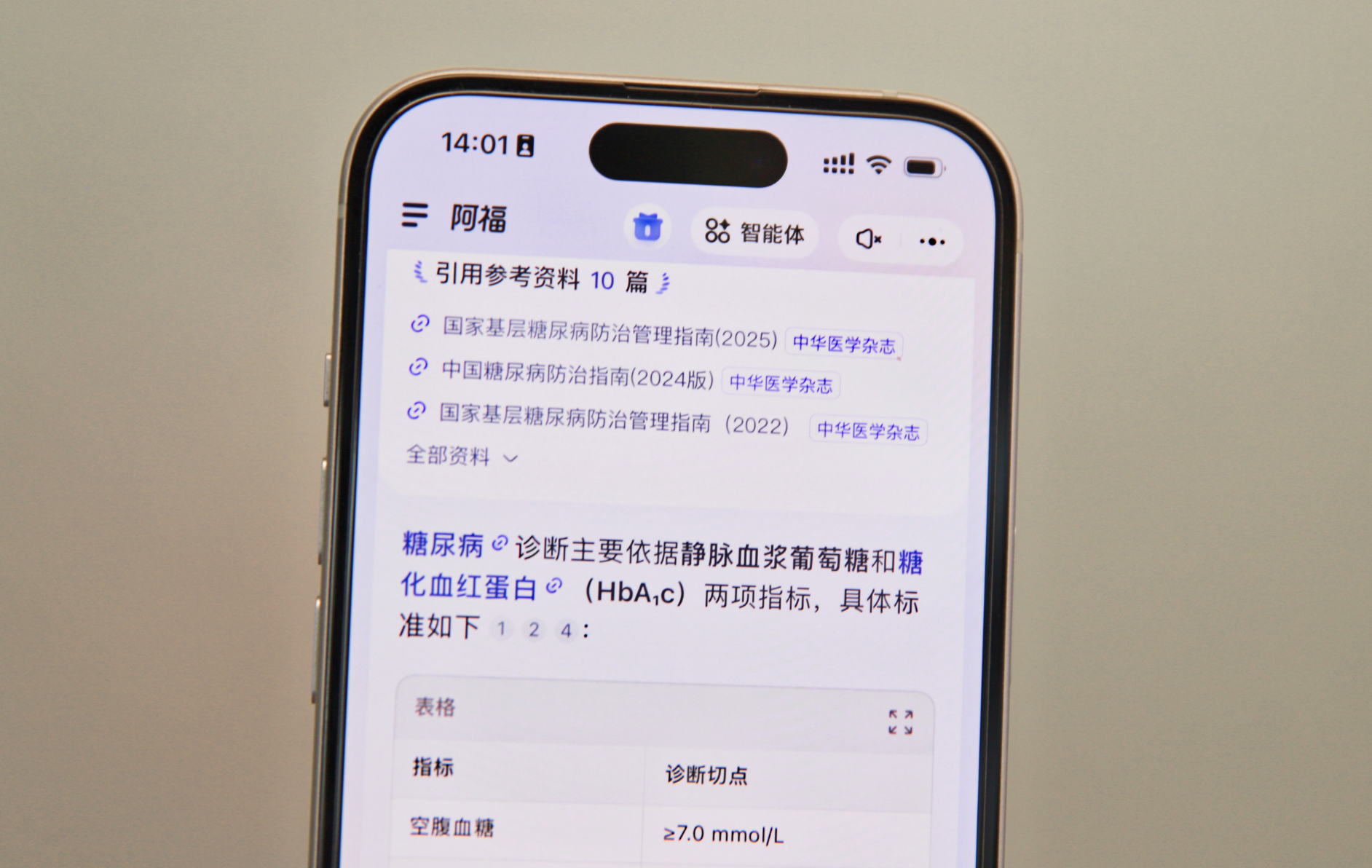
资讯 蚂蚁阿福全面接入中华医学会杂志社知识库
近日,中华医学会杂志社与蚂蚁健康战略合作迎来新进展:蚂蚁阿福已全面接入中华医学会杂志社的医学文献知识库,阿福问答功能可引用知识库内最新的临床指南、专家共识和医学文献。
2026-03-17 11:24
 资讯
资讯 佰特微医疗完成近亿元B轮融资,加速外周血管介入与心衰领域创新布局
本轮融资由天士力资本领投,勤智资本跟投,凯乘资本担任独家财务顾问,所募资金将主要用于新产品研发、生产基地建设及市场拓展,进一步加速公司在外周血
2026-03-16 19:46
 资讯
资讯 天鹜科技完成超2亿元A+轮融资,加速AI蛋白质设计产业化落地
本轮融资由中国石油昆仑资本、上海未来产业基金及老股东涌铧投资联合领投,国投招商、新供销基金、法默凯、孚腾资本等机构跟投,老股东启明创投、金沙江联合资本润璞医疗基金、...
2026-03-16 19:42
 资讯
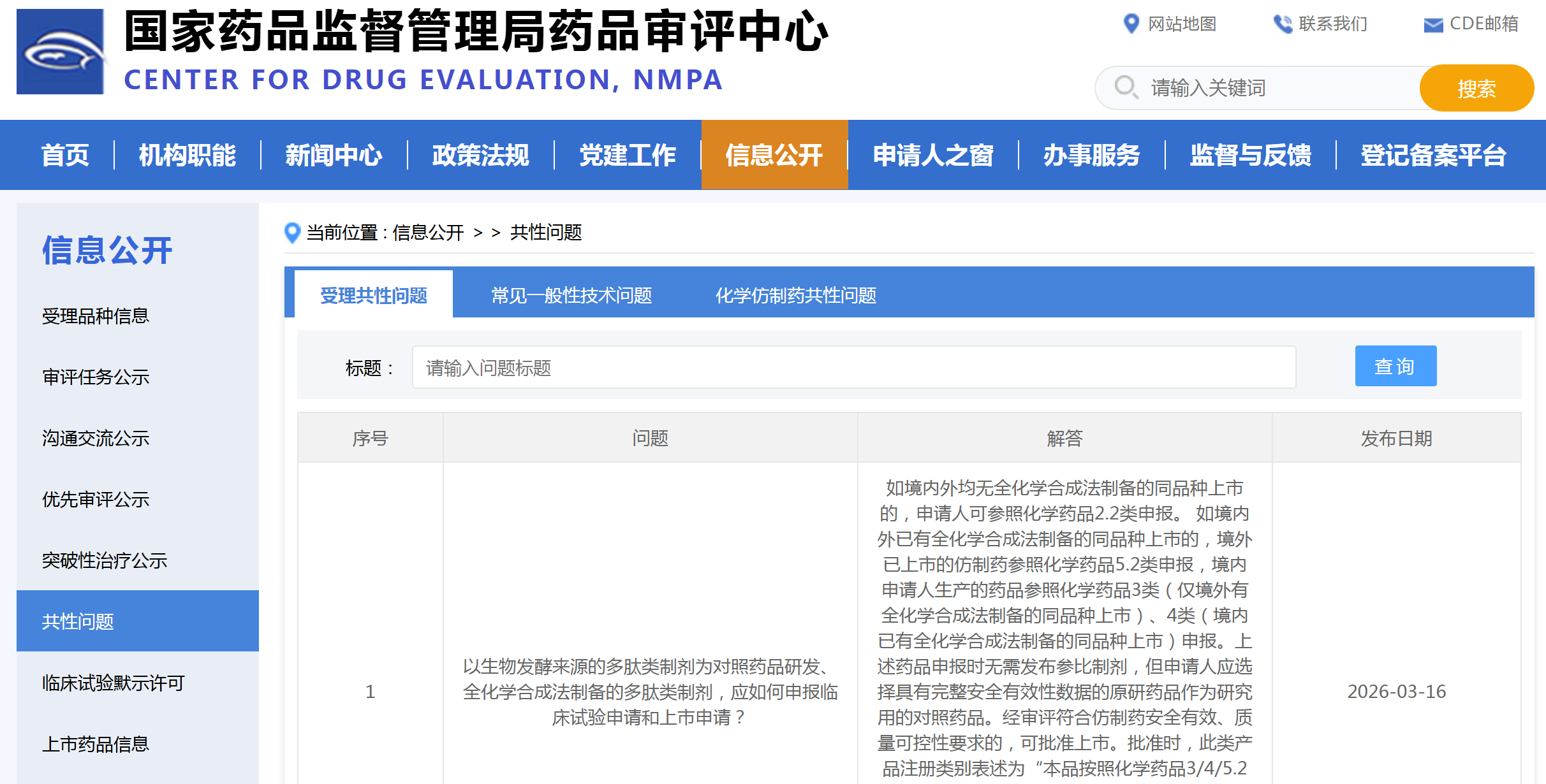
资讯 CDE:以生物发酵来源的多肽类制剂为对照药品研发、全化学合成法制备的多肽类制剂,应如何申报临床试验申请和上市申请?
如境内外均无全化学合成法制备的同品种上市的,申请人可参照化学药品2 2类申报。
2026-03-16 16:32
 资讯
资讯 Cytiva发布重磅新品及本土新品牌“瑞予”, 助推中国创新疗法实现全球引领与普惠可及
Cytiva在华发布三款重磅产品与创新解决方案,赋能体内细胞治疗、个性化肿瘤疫苗、新型抗体等创新疗法的研发与生产。
2026-03-16 13:26
 资讯
资讯 正式发布的“十五五”规划纲要中的“医药健康”
3月13日,《中华人民共和国国民经济和社会发展第十五个五年规划纲要》发布,明确了2026-2030年我国经济社会发展的战略方向,医谷网现将“医药健康”相关辑录如下。
2026-03-14 21:37
 资讯
资讯 成人阻塞性睡眠呼吸暂停诊治指南(2025)发布会暨OSA个体化治疗研讨会在京圆满召开
2026年3月13—14日,由《中华医学杂志》社有限责任公司、《中华结核和呼吸杂志》编委会主办的“成人阻塞性睡眠呼吸暂停诊治指南(2025)发布会暨OSA个体化治疗研讨会”在北京圆满召开。
2026-03-14 18:21
 资讯
资讯 全球首个侵入式脑机接口医疗器械获批上市
今日,国家药监局发布消息,国家药监局批准了博睿康医疗科技(上海)有限公司植入式脑机接口手部运动功能代偿系统创新产品注册申请,实现脑机接口医疗器械全球首发上市,标志着...
2026-03-13 17:39
 资讯
资讯 康龙化成与礼来达成口服GLP-1小分子药Orforglipron生产合作协议
3月11日晚间,康龙化成官方微信发布消息,康龙化成与礼来公司共同宣布,达成关于首个申报注册的口服小分子GLP-1受体激动剂Orforglipron的生产合作协议。
2026-03-12 21:56
 资讯
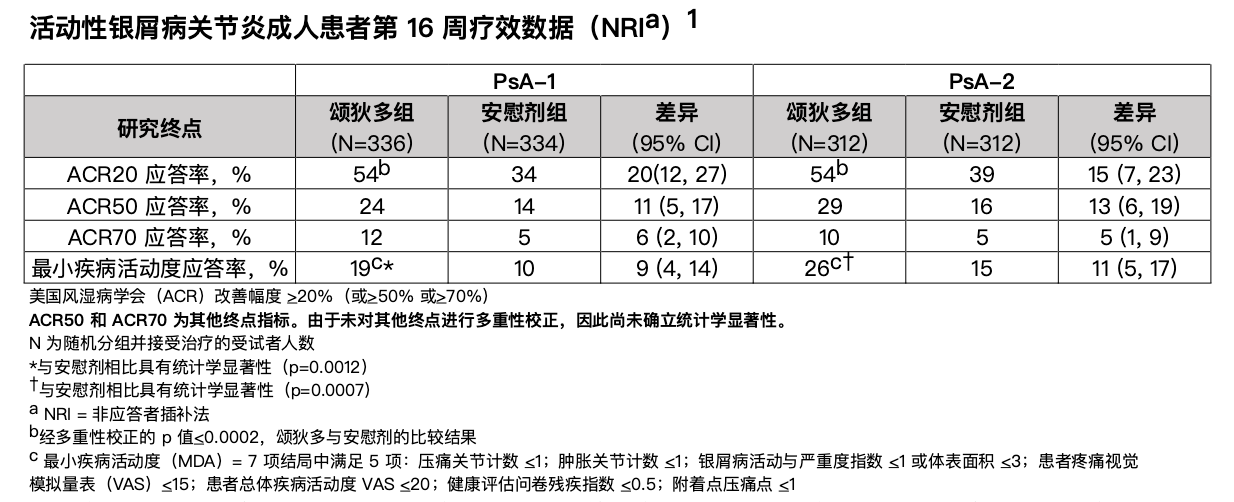
资讯 美国 FDA 批准颂狄多(氘可来昔替尼)用于治疗活动性银屑病关节炎成人患者
颂狄多是一种口服选择性酪氨酸激酶 2(TYK2)抑制剂,也是首个获批用于 PsA治疗 的 TYK2 抑制剂
2026-03-12 16:53