SERENA-6 III期临床试验的积极结果显示,阿斯利康的药物Camizestrant与细胞周期蛋白依赖性激酶(CDK)4/6抑制剂(哌柏西利、瑞博西利或阿贝西利)联合使用,对患者无进展生存期(PFS)这一主要终点显示出具有高度统计学和临床意义的改善。该试验评估了在晚期一线治疗中,对于激素受体(HR)阳性、人表皮生长因子受体2(HER2)阴性的乳腺癌患者,当其肿瘤出现ESR1突变时,从标准治疗方案(芳香化酶抑制剂[AI],如阿那曲唑或来曲唑,联合CDK4/6抑制剂)切换为Camizestrant联合CDK4/6抑制剂的治疗方案的疗效。
这项研究结果在伊利诺伊州芝加哥市举办的2025年美国临床肿瘤学会(ASCO)年会全体大会上公布(摘要:#LBA4),并将同步发表在《新英格兰医学杂志》上。
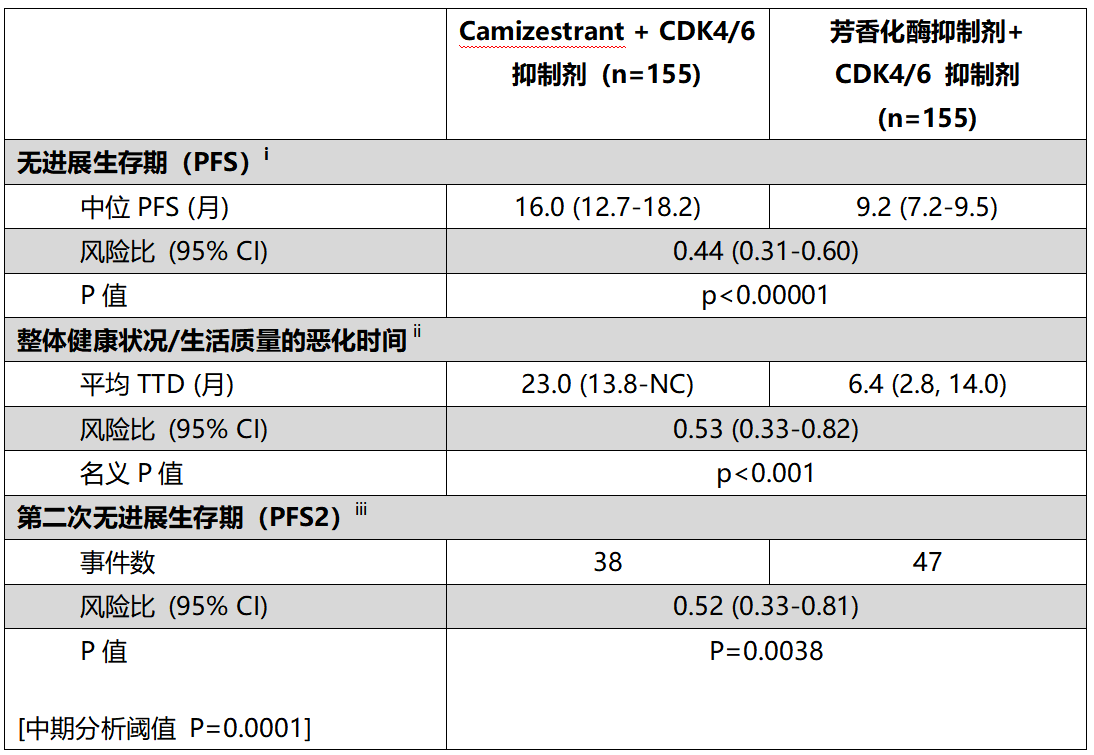
结果显示,与标准治疗相比,Camizestrant联合疗法可将疾病进展或死亡风险降低56%(基于风险比[HR] 0.44;95%置信区间[CI]:0.31–0.60;p<0.00001)。接受Camizestrant联合疗法的试验组中位PFS为16个月,而对照组为9.2个月。值得注意的是,在接受任意一种CDK4/6抑制剂治疗以及各种临床相关亚组,包括年龄、种族、地区、ESR1突变检出时间及ESR1突变类型的患者中,均观察到一致的PFS获益。
此外,Camizestrant联合治疗还延缓了生活质量下降的时间。在一项探索性终点中,与使用芳香化酶抑制剂(AI)联合治疗相比,Camizestrant联合治疗方案可使整体健康状况与生活质量恶化的风险降低47%(HR 0.53;95% CI:0.33-0.82;名义p值<0.001)。接受Camizestrant联合治疗的患者整体健康状况恶化的中位时间为23个月,而继续使用芳香化酶抑制剂(AI)联合治疗的患者为6.4个月(EORTC QLQ-C30)。相比于芳香化酶抑制剂(AI)联合治疗,Camizestrant组合还延缓了疼痛恶化时间。
在进行本次中期分析时,第二次无进展生存期(PFS2)和总生存期(OS)这两个关键次要终点尚未成熟。然而,Camizestrant联合治疗已经显示出PFS2改善的趋势(HR 0.52;95%CI:0.33–0.81;p=0.0038 [中期分析阈值p=0.0001])。该试验将继续评估OS、PFS2和其他关键次要终点。
伦敦癌症研究所(The Institute of Cancer Research)和英国皇家马斯登NHS基金会信托医院的分子肿瘤学教授、SERENA-6试验的联合首席研究者Nicholas Turner博士表示:“这一研究进展标志着乳腺癌治疗领域的又一重要里程碑,重新定义了我们对于这类乳腺癌药物耐药机制的认知。根据SERENA-6的创新试验结果,在患者肿瘤出现ESR1突变后,从芳香化酶抑制剂转换为Camizestrant联合任一CDK4/6抑制剂治疗,可将疾病进展或死亡风险降低一半以上,并将生活质量的恶化时间延迟近18个月。这种前瞻性的策略体现了肿瘤治疗的新思路:在耐药性引发疾病进展和生活质量恶化之前进行干预,有望延长一线治疗的获益,改善患者预后。”
阿斯利康全球执行副总裁、全球肿瘤研发负责人高书璨(Susan Galbraith)表示:“SERENA-6采用循环肿瘤DNA监测,以识别新出现的耐药性并尽早指导治疗方案切换,是首个证明其临床价值的关键性试验,正在重新定义乳腺癌的临床范式。Camizestrant是首个且唯一在一线治疗中,与广泛获批的CDK4/6 抑制剂联合使用时展示出治疗获益的新一代口服SERD和完全ER拮抗剂。这些研究结果进一步表明,Camizestrant有望成为HR阳性乳腺癌内分泌治疗的潜在标准治疗方案。”
SERENA-6临床试验结果摘要:
CI,置信区间;HR 风险比;NC,不可计算;TTD,恶化时间。
i PFS根据RECIST v1.1定义。HR由Cox比例风险模型估算,并根据分层因素进行调整。
ii在基线、第4周、第8周和第12周进行了评估,此后每8周评估一次,直到出现PFS2事件。分析对象为有基线评分且基线后至少完成一次基线后评估的患者。整体健康状况/生活质量恶化时间为一项探索性终点,定义为从随机分组到首次确认恶化之间的时间,恶化需在后续时间点再次确认,评估工具为欧洲癌症研究与治疗组织的30项生活质量问卷(EORTC QLQ-C30)。恶化定义为相较基线下降≥16.6。风险比(HR)通过Cox比例风险模型估算,并根据ESR1突变检出的时机(一次检测 vs 多次检测)以及从启动芳香化酶抑制剂(AI)+CDK4/6抑制剂治疗到随机分组的时间(<18个月 vs ≥18个月)进行分层分析。
iii风险比(HR)采用Cox比例风险模型估算,并根据分层因素进行调整。PFS2的最终分析将在发生158例PFS2事件时进行。
在SERENA-6研究中,Camizestrant 联合CDK4/6抑制剂(哌柏西利、瑞波西利或阿贝西利)的安全性与各药物已知的安全性一致。由于试验中Camizestrant与CDK4/6抑制剂的联合治疗暴露时间更长,Camizestrant试验组中由于各种原因导致的3级或更高级别的不良事件发生率为60%,AI(芳香化酶抑制剂)组则为46%,其中大多数为CDK4/6抑制剂治疗常见的血液不良反应,包括:中性粒细胞减少(45% vs. 34%)、贫血(5% vs. 5%)和白细胞减少(10% vs. 3%)。若发生闪光症(表现为外周视野出现短暂的闪光),并未对患者的日常活动造成影响,且该现象可逆。此外,未观察到眼部结构改变或视力变化。试验中未发现新的安全性信号,两组停药率均较低且相似:Camizestrant联合治疗组有1%的患者停药,AI(芳香化酶抑制剂)组有2%的患者停药,CDK4/6抑制剂的停药率在两组中均为1%。
SERENA-6是首个采用循环肿瘤DNA (ctDNA)检测内分泌耐药性的出现,并依据此在疾病进展前指导切换治疗的全球性、双盲、注册性III期临床试验。该项创新性试验设计在常规肿瘤影像检查时同步进行ctDNA监测,以识别患者是否有内分泌耐药的早期迹象和ESR1突变的出现。在检测到ESR1突变但尚未出现疾病进展前,患者的内分泌治疗将由当下的芳香化酶抑制剂(AI)治疗切换为 Camizestrant,同时继续联合使用原先的CDK4/6抑制剂。
基于SERENA-6 III期临床试验结果,Camizestrant联合CDK4/6抑制剂(哌柏西利、瑞波西利或阿贝西利)这一疗法已获得美国食品药品监督管理局(FDA)授予的“突破性疗法认定(BTD)“,用于治疗在一线内分泌治疗期间出现ESR1突变的HR阳性、HER2阴性局部晚期或转移性乳腺癌成人患者。
为你推荐
 资讯
资讯 百度智能云加码银发经济:大模型破解养老供需错配难题
当居家养老还停留在“人找服务”的传统模式时,以大模型与AI Agent为代表的智能技术,正在掀起一场全新变革,服务开始主动理解需求,并精准触达每一位老人。
2026-03-27 17:24
 资讯
资讯 优赫得®序贯THP方案在华获批用于HER2阳性早期乳腺癌新辅助治疗,实现该适应症“全球首发”
此次获批使优赫得®迈向早期乳腺癌,成为首个且唯一*获批HER2阳性乳腺癌新辅助治疗的ADC疗法
2026-03-27 17:16
 资讯
资讯 医疗服务价格项目立项指南解读辅导(第1期)
长期以来,医疗服务价格实行属地管理,由地方医药价格主管部门制定价格项目、确定价格水平,地区间价格项目数量、内涵、颗粒度差异较大,部分地区按操作流程、岗位分工等拆分价...
2026-03-27 11:21
 资讯
资讯 社保“第六险”,长期护理险全国落地
3月25日,中共中央办公厅、国务院办公厅发布《关于加快建立长期护理保险制度的意见》,标志着这项被称作社保“第六险”的制度正式结束10年试点,迈向全国建制新阶段。
2026-03-26 18:09
 资讯
资讯 国家药监局发布《药品现代物流规范化建设指导意见》,自发布之日起施行
本指导意见是对申请开办药品批发企业(以下简称批发企业)和接受委托储存运输药品业务的第三方药品现代物流企业(以下简称第三方物流企业),在药品现代物流设施设备等方面的基...
2026-03-26 10:14
 资讯
资讯 华东医药独家商业化VC005片Ⅲ期临床顶线数据积极,抢占自免口服疗法新高地
华东医药战略合作方江苏威凯尔医药科技股份有限公司(简称“江苏威凯尔”)宣布,其自主研发的Ⅱ代高选择性JAK1抑制剂VC005片在口服治疗中重度特应性皮炎(AD)的Ⅲ期临床研究中...
2026-03-25 18:52
 资讯
资讯 Cytiva携手上海临床研究中心与新叶生维, 加速先进细胞治疗临床应用转化与产业化发展
Cytiva与上海临床研究中心签署战略合作备忘录,共同设立先进细胞治疗技术临床应用示范平台,以产学研协同为牵引,带动区域产业升级。
2026-03-25 18:46
 资讯
资讯 国家药监局批准两款创新医疗器械
近日,国家药品监督管理局批准了两款创新医疗器械上市。分别为阿迈特医疗器械(北京)股份有限公司二氧化碳造影压力注射套装创新产品注册申请和应脉医疗科技(上海)有限公司经...
2026-03-25 14:53
 资讯
资讯 甘李药业博凡格鲁肽新适应症获批IND
近日,甘李药业股份有限公司及其全资子公司甘李药业山东有限公司宣布,其自主研发的博凡格鲁肽(研发代号:GZR18)注射液增加新适应症的临床试验申请获得国家药监局批准。拟用于...
2026-03-25 14:38
 资讯
资讯 茵菲多组学完成5100万元Pre-A轮融资,构建“硬件+AI+试剂”一体化技术壁垒
本轮融资由杭州新干世业、三泽资本、泰煜投资、德华创投共同参与,丰和资本担任独家财务顾问
2026-03-24 12:59
 资讯
资讯 赶早赴约,忆路守护 礼来携手清华大学阿尔茨海默病科普创意大赛圆满收官
今日,由礼来主办,清华大学承办的 “赶早赴约,忆路守护” 阿尔茨海默病(AD)科普创意大赛颁奖典礼在清华大学圆满落幕。
2026-03-23 17:48