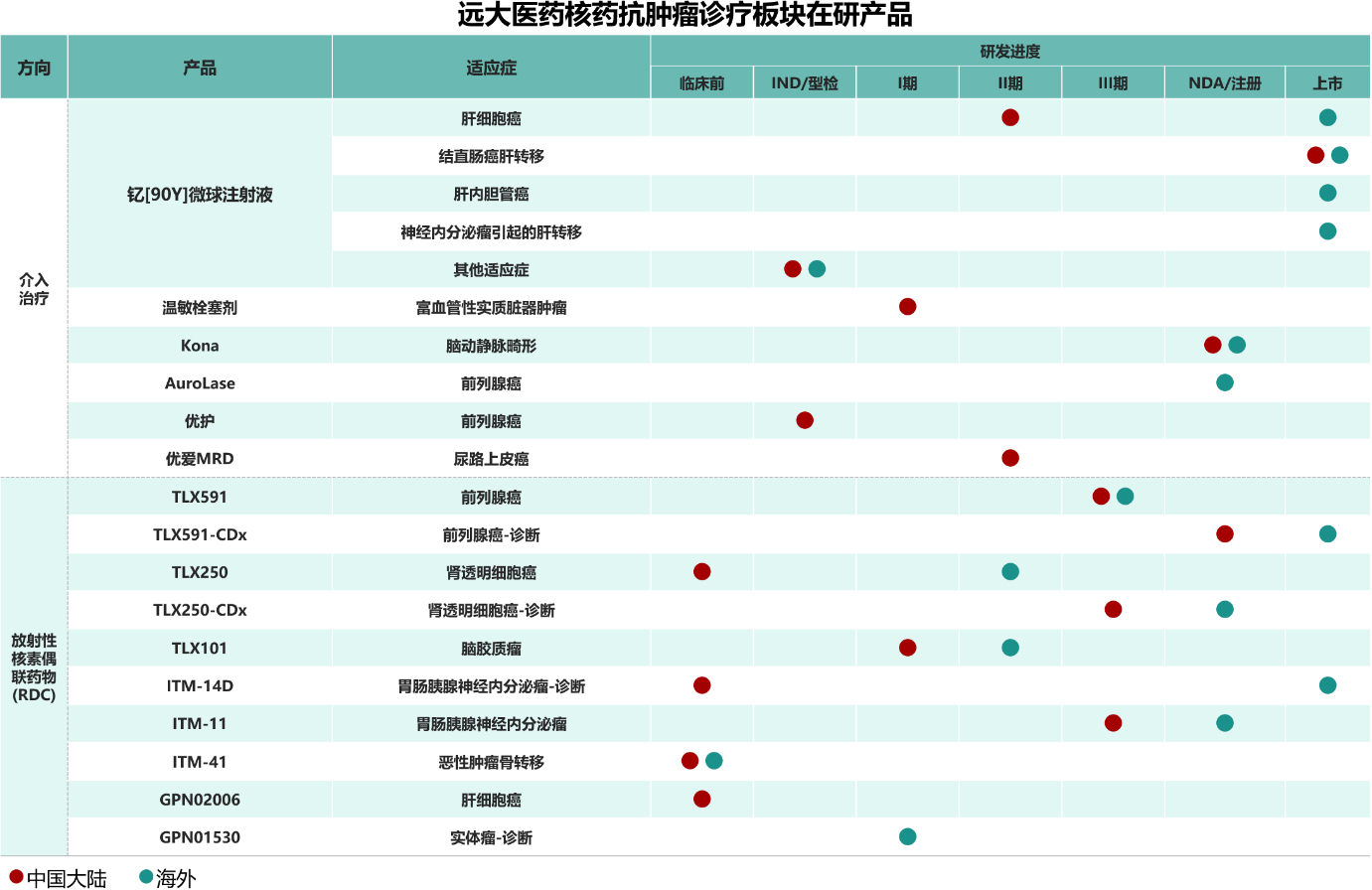
近日,位于张江科学城上海国际医学园区的细胞治疗企业易慕峰宣布,其自主研发的靶向EpCAM的自体CAR-T细胞注射液产品(IMC001)近期获得美国FDA的孤儿药资格,用于治疗胃癌患者。
资料显示,易慕峰是一家致力于突破实体瘤治疗的免疫细胞药物开发企业,基于“化实体瘤为血液瘤”的临床策略,目前已开发降低CAR-T中靶脱瘤毒性的创新平台Peri Cruiser,以及SNR、T-Booster等技术平台,旨在提高CAR-T产品的安全性、对抗肿瘤异质性以及提高扩增和浸润肿瘤的能力。
IMC001是靶向EpCAM的自体CAR-T产品。EpCAM是循环肿瘤细胞(CTC)的生物标志物,其在消化系统肿瘤的转移灶和原位灶中均表达高,而在正常组织中表达量较低;同时,EpCAM在正常组织中表达在免疫细胞不易接触到的细胞基底侧面,而在肿瘤恶性转化过程中EpCAM表达模式转变为在细胞膜上均匀分布。基于此,IMC001能够区分肿瘤组织和正常组织,具有良好的剂量窗口。
目前,IMC001已开展了两项IIT研究,以评估其在晚期EpCAM+消化系统肿瘤的安全性和初步有效性。在针对晚期胃癌的临床试验中,中低剂量组6名晚期胃癌患者中有2名患者被评定为部分缓解(PR),中剂量组三例患者的存活时间均已超过10个月,其中1例PR患者在IMC001单药单次输注后28周成功进行了胃癌根治手术,安全性良好。
除了IMC001,易慕峰还有多条管线在研。今年4月,易慕峰靶向CLDN18.2的自体CAR-T产品IMC002的IND申请获得中国CDE默示许可,适应症为CLDN18.2表达阳性的晚期消化系统恶性肿瘤,包括但不限于晚期胃癌/食管胃结合部腺癌、晚期胰腺癌等。同时,该产品已于今年3月获得FDA的IND批准,并获得FDA孤儿药资格认定。
今年9月,易慕峰基于合成性天然杀伤受体(Synthetic Natural killer Receptor,SNR)技术平台研发的自体CAR-T产品IMC008获得FDA孤儿药认定资格,用于治疗胰腺癌患者。这也是IMC008继2023年8月获得治疗胃癌孤儿药资格认定后的第二项认定。
为你推荐
 资讯
资讯 诺和诺德每周一次长效基础胰岛素Awiqli在美国获批
诺和诺德近日宣布,美国食品药品监督管理局(FDA)已批准Awiqli(insulin icodec-abae,国内通用名依柯胰岛素注射液、商品名诺和期)注射液700单位 mL。
2026-03-30 16:34
 资讯
资讯 “医学影像大模型第一股”德适登陆港交所,开盘大涨121%
上市首日,德适以每股99港元的发行价开盘,股价随即大幅飙升,盘中最高涨幅达121%,报219港元,市值迅速突破200亿港元
2026-03-30 12:39
 资讯
资讯 微元合成完成 3 亿元 A + 轮融资,联合全球顶尖机构发布 AI 生物计算开放平台 PoseX
本轮融资由河南投资集团汇融基金与复旦大学校董、化工行业资深投资人谭瑞清先生联合投资
2026-03-30 12:34
 资讯
资讯 华海药业与西班牙制药企业达成不超过3.4亿美元的BD交易
3月29日,华海药业发布公告称,下属控股子公司上海华奥泰生物药业股份有限公司与西班牙知名制药企业Almirall,S A 达成全球研究合作及许可协议,用于开发具有多种潜在适应症(...
2026-03-30 10:18
 资讯
资讯 礼来与英矽智能达成交易总价值最高约27.5亿美元的AI药物合作
3月29日电,英矽智能在港交所公告,已与Eli Lilly and Company(“礼来”)达成授权及药物研发合作,双方将利用英矽智能的AI制药能力,加速多个治疗领域中新型疗法的发现与开发。
2026-03-30 09:58
 资讯
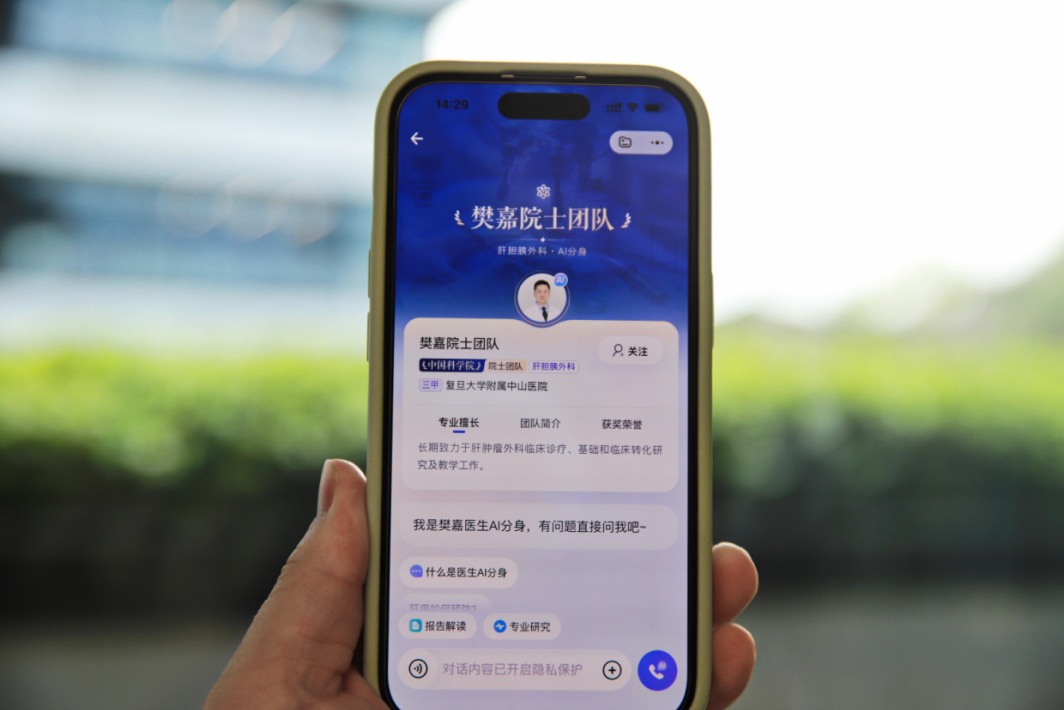
资讯 助力国家人工智能应用中试基地建设,蚂蚁阿福上线樊嘉院士肝病专科智能体
3月28日,国家人工智能应用中试基地(医疗领域)阶段性成果总结发布会在复旦大学附属中山医院举行。
2026-03-29 21:03
 资讯
资讯 贵州百灵的“平账”造假行为
3月28日,贵州百灵(ST百灵,002424 SZ)发布多则公告披露,公司及相关当事人已分别收到贵州证监局下发的《行政处罚决定书》,涉及连续四年年报虚假记载、相关人员违规履职等多...
2026-03-29 19:38
 资讯
资讯 李强主持召开国务院常务会议,研究加快建设分级诊疗体系有关政策措施
要统筹抓好分级诊疗体系建设和医疗卫生强基工程实施,以常见病、慢性病为重点引导群众基层首诊,以增强就医连续性为导向优化转诊服务管理,扎实做好家庭医生签约服务,推动医疗...
2026-03-28 22:18
 资讯
资讯 百度智能云加码银发经济:大模型破解养老供需错配难题
当居家养老还停留在“人找服务”的传统模式时,以大模型与AI Agent为代表的智能技术,正在掀起一场全新变革,服务开始主动理解需求,并精准触达每一位老人。
2026-03-27 17:24
 资讯
资讯 优赫得序贯THP方案在华获批用于HER2阳性早期乳腺癌新辅助治疗,实现该适应症“全球首发”
此次获批使优赫得®迈向早期乳腺癌,成为首个且唯一*获批HER2阳性乳腺癌新辅助治疗的ADC疗法
2026-03-27 17:16
 资讯
资讯 医疗服务价格项目立项指南解读辅导(第1期)
长期以来,医疗服务价格实行属地管理,由地方医药价格主管部门制定价格项目、确定价格水平,地区间价格项目数量、内涵、颗粒度差异较大,部分地区按操作流程、岗位分工等拆分价...
2026-03-27 11:21
 资讯
资讯 社保“第六险”,长期护理险全国落地
3月25日,中共中央办公厅、国务院办公厅发布《关于加快建立长期护理保险制度的意见》,标志着这项被称作社保“第六险”的制度正式结束10年试点,迈向全国建制新阶段。
2026-03-26 18:09
 资讯
资讯 国家药监局发布《药品现代物流规范化建设指导意见》,自发布之日起施行
本指导意见是对申请开办药品批发企业(以下简称批发企业)和接受委托储存运输药品业务的第三方药品现代物流企业(以下简称第三方物流企业),在药品现代物流设施设备等方面的基...
2026-03-26 10:14
 资讯
资讯 华东医药独家商业化VC005片Ⅲ期临床顶线数据积极,抢占自免口服疗法新高地
华东医药战略合作方江苏威凯尔医药科技股份有限公司(简称“江苏威凯尔”)宣布,其自主研发的Ⅱ代高选择性JAK1抑制剂VC005片在口服治疗中重度特应性皮炎(AD)的Ⅲ期临床研究中...
2026-03-25 18:52
 资讯
资讯 Cytiva携手上海临床研究中心与新叶生维, 加速先进细胞治疗临床应用转化与产业化发展
Cytiva与上海临床研究中心签署战略合作备忘录,共同设立先进细胞治疗技术临床应用示范平台,以产学研协同为牵引,带动区域产业升级。
2026-03-25 18:46