近日,一则《关于加强药物临床试验机构日常监管的函》在网上流传,落款是国家药监局。
函件指出,上海市东方医院等13家临床试验机构在数据完整可靠方面存在问题,要求在6个月内完成整改,并由相关省局加强日常监管。
“这13家中心,所有的项目都暂停了,而且至少停半年,对在研的项目影响非常大。”在临床类CRO工作多年的李瑜(化名)介绍,“而且,如果整改之后,药监局再去检查,还是不能符合要求的话,可能这些医院在研的新药临床项目全部都会作废。”
李瑜分析,这次13家机构被发现有问题,较大可能是常规核查发现,也不排除是对之前已申报药物的核查。
如果是后者,在报批阶段被查出临床试验有问题的话,按照《药物临床试验质量管理规范》(GCP)要求,药品申办方是最终责任人。这款药可能会无法获批、平均10年的付出打了水漂,而且药企会上黑名单,三年不能再申报。
临床试验机构被查出数据问题,后果可能严重到什么程度?可以从近年其他类似事件中找到参照。
2021年1月,国家药监局发布公告称,对在审的10个医疗器械注册申请项目开展了临床试验监督抽查,涉及27家临床试验机构。抽查中发现,安旭生物的一款检测试剂盒产品在浙江大学医学院附属第一医院开展临床试验过程中,存在医疗机构留档的电子照片拍摄时间、地点与临床试验实际时间、地点不一致等问题,其临床试验数据无法溯源,使数据可靠性大打折扣。
安旭生物当时对公众辩解说,这主要是医疗机构的问题,“这次抽查发现的问题,主要指向的是医疗机构,公司也是受害者。”
不过,板子主要还是打在它这个申办方身上。
当时,国家药监局公告宣布,“对该注册申请项目不予注册,并自不予注册之日起一年内不予再次受理该项目的注册申请。”此外,国家药监局还责成浙江省药品监督管理局对安旭生物依法依规调查处理。
当时,安旭生物正寻求科创板上市,这一事件为其带来了浓重的阴影。
行业高速发展伴生的问题
药企或CRO会向临床研究机构委派CRA(临床监察员)、CRC(临床研究协调员),对日常临床试验的开展进行协调与监管,并核查最终数据。
李瑜在CRO行业工作多年,亲身经历了“7·22核查”风暴,也见证了医药河道翻滚起来后,每个相关环节都应声涨水,因此伴生的新问题。
她回忆,2015年的“7·22核查”,是中国临床试验真实、完整度的一个分水岭。
在那之前,临床试验造假颇为普遍。在那之后,主动造假变得十分罕见,中国创新药产业也随之蒸蒸日上。
不过,如今,中国的药物临床试验仍存在一些问题,有待规范及改善。最常见的问题,包括数据转录过程中不可避免的误差,也包括相关资料缺失等。
首先是不可避免的误差。行外人也许很难相信,临床试验数据这种精确性至关重要的信息,竟然是人工搬运的。
在中国,临床试验往往由公立医院承担执行。公立医院的HIS系统不直接向CRO敞开,甚至外部机构的移动硬盘都不可以接入到医院的电脑上,临床试验数据就只能靠人的眼和手,从医院的HIS系统搬运到临床试验机构的EDC系统。
李瑜解释,临床试验数据规模很大,人在录入时难免有错漏,“此外,由于录入者本身专业度的区别,录入的数据也会有差异。”
数据录入是CRC的工作。CRC,即临床协调员,负责协助研究者进行非医学判断的相关事务性工作。他们的工作事无巨细,基本上是“哪里需要哪里搬”,包括让患者签知情同意书、陪他们做检查、电话随访,让医生在各种文件上签字,还有患者病历、领药单、发药记录、医院质控文件等大量文件的搜集和录入等。
理想状态下,CRC最好由懂临床医学的人担任。不过,这个职位目前很难招到临床医学背景的员工,绝大多数都是药学背景的。为保证录入工作的质量,大部分新入职的员工都需要接受临床医学知识培训。
此外,CRO负责监督一个临床试验项目的,还有CRA、项目经理等。
CRA(临床试验监察员)负责临床项目的监察工作,定期去不同医院收集数据,是申办方和临床试验机构的沟通枢纽。项目经理则负责整体的把控。
李瑜指出,近年一些CRO常遇到临床试验资料中途丢失的问题,这通常是由于不少项目的CRC、CRA甚至项目经理离职都过于频繁,有时甚至缺少交接。
她提到,这几年创新药赛道大热,大量资金涌入,创新药企层出不穷,这让CRC等成为紧俏工种,导致从业者流动性很高。
“我看到网上报道说,整个行业的人员流动率达到了80%-90%。”李瑜以CRC为例,这一职位的新人在工作一年后,就开始成为业界高薪挖角的对象,开始频繁跳槽。她曾任职的CRO,也因此不愿意再招没经验的人从头培养。
李瑜了解到,一些临床试验的研究者(即医生)一开始还会培训CRC、CRA怎么看病历、怎么录入,还会审核录入的数据。“可是培训之后,过了一个月这人就离职了。你想想,当CRO派来的人换到第三个、第五个的时候,研究者还会培训吗?”她说,“如果你每个月甚至每一周都在给他换他的助理(即CRC),他是不是也觉得你对这个项目不负责任?”
高度流动性有时会导致更大的麻烦。比如,前一个员工辞职之后,如果一时招不到新人,甚至有项目三个月、半年都没有CRC。这种情况下,工作交接变得几乎不可能。
“新的人来了之后,可能连相关文件有多少个都不知道,再去找可能已经找不到了。”李瑜表示。
等试验结束,CRO派人去稽查,或CRA、项目经理去看的时候,才发现大量文件缺失。“知情同意书、领药单、病例、各种资料都可能丢失。”她介绍。
可能导致哪些后果?
发现有资料丢失的时候,CRC会怎么办?
一种常见的情况是,重新找相关人签字,补上资料。在合规性严格的公司,资料回签是坚决不被允许的,它视同造假。不过,许多公司选择睁一只眼闭一只眼。
据多位CRO从业者介绍,资料回签是行业普遍现象。一位从业者举例道,一份本应该在8月10日被签的文件,因为医生出差、开会、疏忽,没能及时被签署,一周之后,医生才发现这份文件,签了8月10日的日期。他认为这样的情况并不属于造假。
但如果文件缺失过多,可能有另一种情况。“如果这个项目换了5个CRC,你是第五个,你需要补的东西是不是可能很多?”李瑜举例,职位空缺几个月后新招来的CRC,可能不知道该补哪些东西,也可能知道但没有动力去做。因为补件会大大增加工作量,还可能挨医生和患者的骂,而公司并不会为这种额外工作支付工时费。
发现缺件严重的时候,新接手的CRC通常会告诉公司这个烂摊子的实情。根据2017年6月最高人民法院、最高人民检察院发布的《关于办理药品、医疗器械注册申请材料造假刑事案件适用法律若干问题的解释》,临床试验数据造假行为属于刑事犯罪。因此,遇到这种情况,项目经理等人往往并不敢在相关文件上签字,他们很可能选择在临床项目揭盲前离职。
如果真到了这一步,CRO公司也无力回天。据李瑜介绍,有的CRO就选择了“拖”字诀:一直出不了组,或者出组后拖着不做统计,甚至还有的直接宣布试验失败。另外,也有的试验结束以后,临床试验机构认为质控不通过不给盖章,于是这款药品就无法去报批。
“而药企,因为资料都在CRO公司手里,也不能换公司,还得去求着见面。”李瑜回忆,她曾见过一个药企老板,因为CRO一直不给他们临床结果,最后老板就到CRO公司门口去堵人。
“这几年Biotech大热,很多创新药企开了很多临床,现在都快到出二三期结果的时候了。”李瑜推测,过后几年,可能出现大量临床试验烂尾的情形,“反正不是说新药研发99%都是失败的么?”新药研发本身高企的失败率,也许将成为一些临床试验管理水平低下的遮羞布。
研究者缺位何解?
多名CRO从业者分析,临床试验中的这些问题,一定程度是临床研究者缺位所导致。
当小医院苦于没有临床试验时,大三甲医生们的案头已经堆满了试验项目。由于患者多、名气大的天然优势,前来递交临床试验合作的药企不在少数。
一位从业者提及:“有的医生接了太多试验。但医生的时间是有限的,本身临床工作就非常忙,分配到试验上的时间少得可怜。”
在他看来,利益分配的问题更是加剧了这一情况。每一年,CRO公司会通过医院的药物临床试验机构来达成合作。药企支付的钱,被写在合同里,也会按时支付到医院。但医院是否把钱给了医生,如何给,药企无权过问。
“大部分医院不能及时有效把临床试验的这一笔钱发给医生。这样带来一个很大问题,医生没有主观能动性去做项目。”他透露,这就导致需要额外花时间和精力去和医生打交道、做客情。
本应该是医生跟企业之间纽带和桥梁的药物临床试验机构,一旦成为了药企临床试验进度推进的阻力时,进一步加剧了CRO公司另辟蹊径。
一位行业人士透露,进度对药企来说是抢占先机的关键。但如果医院这一层面有阻力,就会导致一些立项时间超过半年,甚至超过一年。好一点的可能就两三个月立项完成,时间成本背后的差距特别大,CRO公司也只能在不合规的边缘无奈试探。
此外,还有一位熟悉临床试验过程的肿瘤患者表示,部分外资药企对临床试验的把控能力相对好,“审核、评估和用药都很严格”,这从一定程度上能消除一定范围内的误差。
这几年,疫情也加重了临床数据录入和追溯的困难。尤其在今年,不少临床研究机构所在地都受到了较大影响,CRA无法定期出差到现场核查,这也影响了临床数据记录的时效性和真实性。李瑜举了一个例子,她的团队在做一个临床试验的稽查时发现,多名受试者需要每隔数小时量一次体温,但在报告表上,所有受试者在不同时段的体温,都是同一个数字。
“7·22”至今,中国的临床试验规范性有了极大提高,这也促进了创新药行业的发展。不过,这一领域的进一步规范化,仍需药企、CRO、临床研究机构和监管部门的继续努力。
来源:深蓝观 作者:郑洁 丛丛 卓曌
为你推荐
 资讯
资讯 诺华泰菲乐®联合迈吉宁®新适应症获批,为BRAF V600E突变阳性RAIR-DTC患者带来精准治疗新选择
用于治疗BRAF V600E突变阳性、放射性碘难治或不适用、且血管内皮生长因子酪氨酸激酶抑制剂(VEGFR-TKI)治疗失败的局部晚期或转移性分化型甲状腺癌成人患者。
2026-06-10 18:08
 资讯
资讯 3个项目完成首批生物医学新技术临床研究备案
6月8日,中国生物技术发展中心发布生物医学新技术临床研究备案完成项目清单(第1批),自5月1日《生物医学新技术临床研究和临床转化应用管理条例》正式生效以来,5月1日至5月22...
2026-06-10 17:51
 资讯
资讯 35.7亿元!来凯医药PI3Kα抑制剂达成达成海外BD
来凯医药将授予Vasque Bio LAE118在全球范围内(不含中国大陆、中国香港、中国澳门、中国台湾地区)的独家开发、生产制造及商业化权益,全权负责该药物海外市场的全流程研发与...
2026-06-10 14:28
 资讯
资讯 腾讯、阿里等入股脑机接口企业阶梯医疗,博睿康完成上市辅导
公开资料显示,近日上海阶梯医疗科技有限公司发生工商变更,新增阿里巴巴关联公司杭州灏月企业管理有限公司、腾讯关联公司上海启善投资有限公司等为股东,同时注册资本由100万元...
2026-06-10 10:06
 资讯
资讯 药明康德、诺禾致源等被美国列入“中国军工企业”名单
今日,药明康德发布公告称,公司注意到,2026年6月8日(美国时间),美国国防部错误地将药明康德列入其根据1260H条款认定的“中国军工企业”正式更新版名单中。
2026-06-09 21:24
 资讯
资讯 微眸医疗完成近亿元A轮融资,全国首个眼科手术机器人多中心随机对照注册临床试验同期收官
本轮A轮融资由元航资本领投,老牌投资机构明桂资本持续加码追投,多家行业知名投资机构联合参与投资,伊嘉资本担任本次融资财务战略合作伙伴。
2026-06-09 20:20
 资讯
资讯 礼来公布口服小分子GLP-1 药物关键研究完整数据,潜在T2D新口服方案表现亮眼
礼来公司在美国糖尿病协会(ADA)第86届科学年会上公布了口服小分子GLP-1受体激动剂orforglipron在ACHIEVE系列三项3期临床研究中的详细数据。
2026-06-09 19:57
 资讯
资讯 因美纳发布StrataMap Spatial Solution:高性能的端到端空间全转录组研究解决方案
StrataMap Spatial支持研究人员以真正的单细胞分辨率开展空间生物学研究,拓展科学发现的边界
2026-06-09 19:52
 资讯
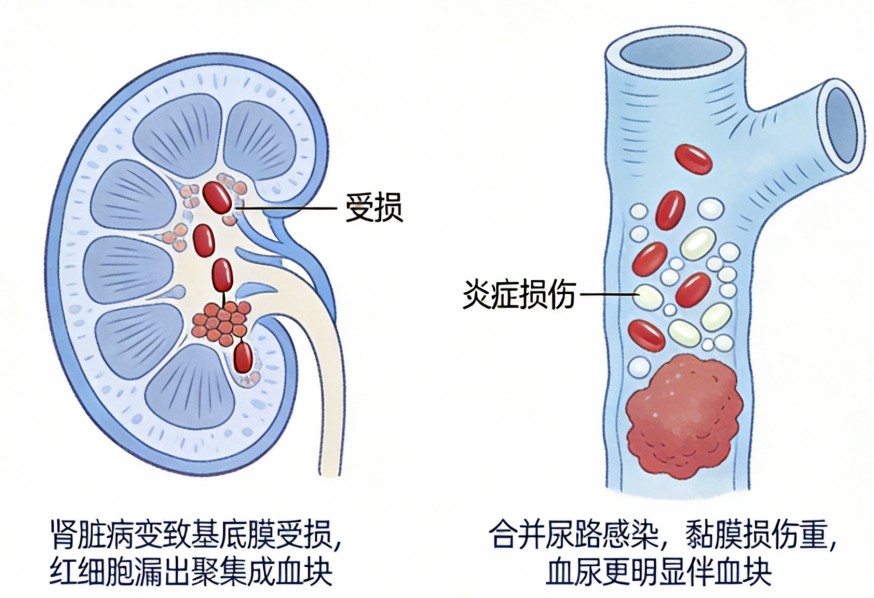
资讯 两款IgA肾病新药获批
6月9日,荣昌生物发布公告称,近日,荣昌生物制药(烟台)股份有限公司收到国家药品监督管理局(NMPA)核准签发的《药品注册证书》,泰它西普注射液(代号:RC18)治疗免疫球蛋...
2026-06-09 11:33
 资讯
资讯 第五年,2026年纠正医药购销领域和医疗服务中不正之风工作要点
《通知》围绕年度重点任务和既往工作中发现的突出问题,聚焦重点领域和关键环节,在坚持党建引领行风、强化医德医风建设、加强正向宣传引导、防范化解风险隐患、严守医疗数据安...
2026-06-09 09:14
 资讯
资讯 华超神控完成亿元天使系列融资,自研 AI 超声脑机平台开辟无创深脑调控新赛道
本轮融资分为天使轮与天使 + 轮两期,天使轮由经纬创投独家领投,天使 + 轮由德联资本、道远资本联合领投,行业知名机构持续加注,循光资本担任本次系列融资独家财务顾问。
2026-06-08 17:05
 资讯
资讯 Cytiva与鼎康生物合作GMP-2扩建项目投产, 共筑“中国速度,全球交付”新标杆
GMP-2生产基地专为临床后期及商业化生产打造,可为全球生物药合作伙伴提供灵活且可扩展的生产解决方案,助力加速产品商业化进程并保障全球稳定供应。
2026-06-08 16:41
 资讯
资讯 默沙东欣瑞来(注射用索特西普)重磅上市,引领肺动脉高压(PAH)迈向“治本” 新里程碑
用于治疗世界卫生组织功能分级(WHO FC)Ⅱ-Ⅲ级的肺动脉高压(PAH,WHO第1组)成年患者
2026-06-08 16:36
 资讯
资讯 GCP2026修订版发布,2020版废止
6月8日,国家药监局、国家卫生健康委、国家中医药局、国家疾控局联合发布《药物临床试验质量管理规范(2026年修订)》,自2026年9月1日起施行。国家药监局、国家卫生健康委《关...
2026-06-08 16:21
 资讯
资讯 博腾股份终止斯洛文尼亚研发生产基地建设,保留对诺华子公司主张索赔的权利
近日,博腾股份公告称,鉴于诺华斯洛文尼亚子公司已向博腾股份全资子公司PSI发出解除通知,PSI在该场地内的投资和建设已面临重大不确定性,公司决定终止投资建设斯洛文尼亚研发...
2026-06-08 13:10
 资讯
资讯 全球首款CD7 CAR-T儿童适应症一期临床启动
据安科生物和博生吉医药消息,安科生物参股公司博生吉医药自主研发的全球首款进入临床阶段的靶向CD7自体CAR-T产品PA3-17儿童适应证临床试验启动会在组长单位中国医学科学院血液...
2026-06-08 10:57
 资讯
资讯 一家医疗器械企业被调入港股通
6月5日收市,上海证券交易所官网发布最新港股通标的调整通知,共6家企业调入,包括广受关注的大模型企业智谱(02513 HK)、GPU企业壁仞科技(06082 HK)等,其中生物医药、医...
2026-06-07 21:20




