3月29日,国家卫健委会同国家药监局就《临床急需药品临时进口工作方案》和《氯巴占临时进口工作方案》公开征求意见,意见反馈截止时间为2022年4月28日。
《临床急需药品临时进口工作方案》适用于国内无注册上市、无企业生产或短时期内无法恢复生产的境外已上市临床急需少量药品。其中,临床急需少量药品为符合下列情形之一的药品:
(一)用于治疗罕见病的药品;
(二)用于防治严重危及生命疾病,且尚无有效治疗或预防手段的药品;
(三)用于防治严重危及生命疾病,且具有明显临床优势的药品。
方案指出,由医疗机构向国家药监局或国务院授权的省、自治区、直辖市人民政府提出临时进口申请,并按要求提供材料,包括医疗机构的机构合法登记文件复印件、申请报告及承诺书、拟进口药品清单。同时,医疗机构、经营企业依法对临时进口药品承担风险责任。
对于《氯巴占临时进口工作方案》,资料显示,氯巴占是一款治疗罕见癫痫疾病的广谱抗癫痫发作药物,在超过100个国家被用作抗癫痫药物,在我国属于第二类精神管制药物。早在2017年5月,氯巴占就作为“中国大陆境内尚未注册上市且临床急需的儿童用药”,被列入《第二批鼓励研发申报儿童药品建议清单》,但截至目前,尚无国内药企生产的氯巴占上市,患儿家属只能从国外代购正规上市的氯巴占。2021年6月,一名母亲为给孩子治病,给一名代购者代收了海外购买的氯巴占,结果因为涉嫌“走私、运输、贩卖毒品罪”受到刑事追究,此案已经做出不起诉处理。近期,随着海关对氯巴占药物查处力度的加大,众多患儿已经面临断药风险。
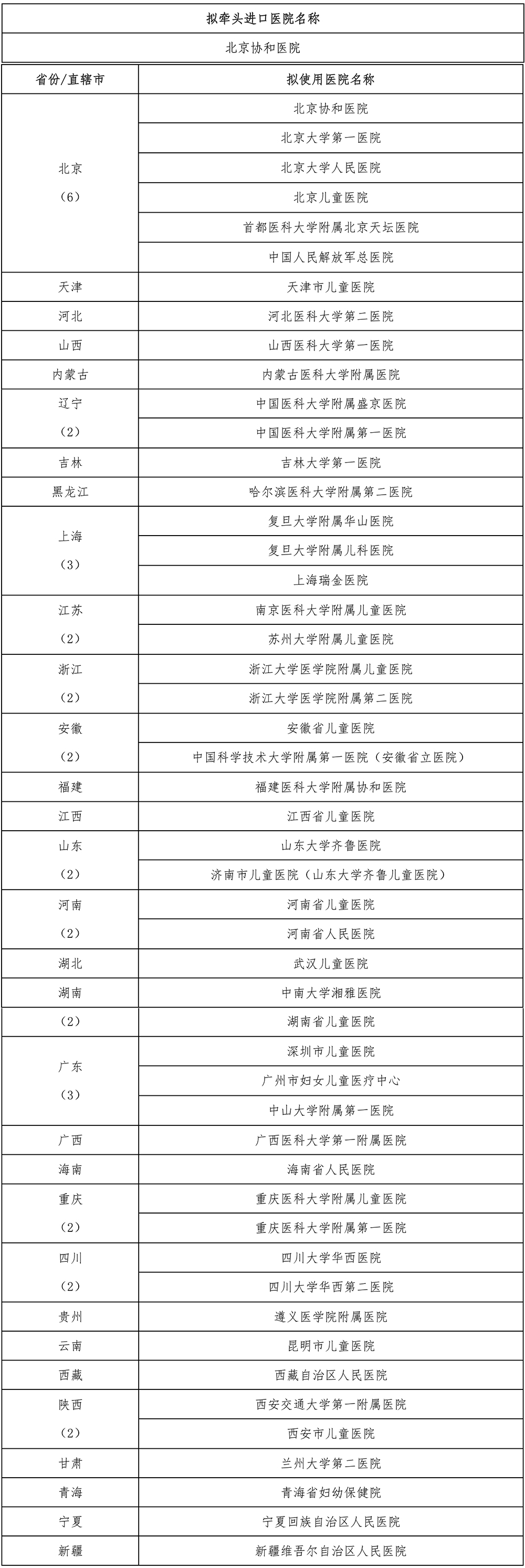
针对患儿的用药需求,目前国家卫健委在方案中提出拟牵头进口和使用氯巴占的50家医疗机构名单,此次选定的医疗机构条件包括:1.三级医院;2.具有癫痫亚专科或相关专业医生,从事癫痫或儿童癫痫诊治10年以上;3.具有氯巴占临床安全使用规范及应急预案,建立临床、药学、医务多学科诊疗团队。
拟牵头进口和使用氯巴占的医疗机构名单
临床急需药品临时进口工作方案(征求意见稿)
为进一步完善药品供应保障政策,满足人民群众特定临床急需用药需求,现依据《中华人民共和国药品管理法》有关规定,制定本方案。
一、工作目标
明确各部门职责,各负其责,加强组织保障和监管力度,规范、高效地开展临床急需药品临时进口工作。
二、药品范围
适用于国内无注册上市、无企业生产或短时期内无法恢复生产的境外已上市临床急需少量药品。其中,临床急需少量药品为符合下列情形之一的药品:
(一)用于治疗罕见病的药品;
(二)用于防治严重危及生命疾病,且尚无有效治疗或预防手段的药品;
(三)用于防治严重危及生命疾病,且具有明显临床优势的药品。
三、申请工作流程
(一)医疗机构应向国家药监局或国务院授权的省、自治区、直辖市人民政府提出临时进口申请,并按要求提供以下材料:
1.医疗机构的机构合法登记文件复印件(如医疗机构执业许可证、营业执照(如有)、组织机构代码证等)。
2.申请报告及承诺书。内容应包括:拟申请进口药品的具体用途、进口的必要性说明,申请医疗机构的名称、地址及联系人信息。医疗机构书面承诺拟进口药品在指定医疗机构内用于特定医疗目的,不得用于申请用途以外的其他用途。
3.拟进口药品清单。内容应包括:药品名称、剂型、规格、进口数量、境外持有人名称地址、生产企业名称地址、药品产地、拟申报通关的口岸名称。
上述材料须加盖医疗机构公章。
(二)国家药监局收到医疗机构申请后,可就申请医疗机构是否具备使用管理能力、药品是否临床急需、药品需求量是否合理等征求国家卫生健康委意见。国家卫生健康委可视情况征求医疗机构所在地省级卫生健康主管部门意见。国家药监局在接到国家卫生健康委书面反馈意见后3个工作日内,对符合要求的申请,以局综合司函形式作出同意进口的复函,复函抄送国家卫生健康委、各省级药品监督管理部门及口岸药品监督管理部门,国家卫生健康委抄送各省级卫生健康主管部门。
(三)医疗机构依据复函向口岸药品监督管理部门申请办理《进口药品通关单》。此类进口药品,无需进行口岸检验。
(四)进口药品若属于麻醉药品和国家规定范围内的精神药品,还需要向国家药监局申请进口准许证。医疗机构可以委托进口单位办理进口准许证。进口单位按照国家药监局网上办事大厅公布的供临床使用麻醉药品和精神药品的进口审批办事指南提出申请。
具体材料包括:麻醉(精神)药品进口申请表;购货合同或订单复印件;医疗机构委托代理协议复印件;进口单位的《营业执照》《对外贸易经营者备案登记表》复印件;出口单位如为该药品的销售代理公司,还需提供委托代理协议和出口单位合法资质证明文件、公证文本以及认证文本;申报资料真实性自我保证声明。符合规定的,国家药监局在3个工作日内出具进口准许证。
该项申请可与(一)医疗机构申请临时进口同步提交申报材料,国家药监局予同步审批。申请人因自身原因无法同步提交申报材料的,也可将(一)与(四)分别提交申请。
(五)进口麻醉药品、国家规定范围内的精神药品的,凭进口准许证办理报关验放手续。
(六)进口药品属于治疗罕见病的,原则上由全国罕见病诊疗协作网的1家医疗机构作为牵头进口机构,汇总全国范围内用药需求、使用该药的医疗机构名单和承诺书,按照本方案要求牵头提出临时进口申请并组织做好使用管理工作。
四、药品使用管理
使用临时进口药品的医疗机构应按照《医疗机构药事管理规定》,重点做好以下工作:
(一)制定临床技术规范,明确药品的临床诊治用途、患者群体、使用科室及医生名单;建立专项管理制度,对医师处方、用药医嘱的适宜性进行审核,严格规范医师用药行为。
(二)监测记录临时进口药品使用相关的临床诊疗病历及药品安全性、有效性、价格、依从性、不良反应等信息数据,并应当长期保存。若发生严重不良反应时,及时通报医疗机构所在省份的药品监督管理部门、卫生健康主管部门、国内药品经营企业。省级药品监督管理部门与省级卫生健康主管部门共同研判临床用药风险,必要时采取停止使用等紧急控制措施,并分别报告上级主管部门。
(三)制定完善的安全防范措施和风险监控处置预案。
(四)应按规定对临时进口药品合理储存。
(五)应按年度对临时进口药品进行评估,并报告省级卫生健康主管部门。
(六)按规定选取药品经营企业开展采购、进口和配送临时进口药品等相关工作。
(七)属于罕见病用药的,原则上应当依托《中国罕见病诊疗服务信息系统》和全国罕见病诊疗协作网加强药品使用的科学化管理。
五、相关方权责
医疗机构、经营企业依法对临时进口药品承担风险责任。医疗机构应当与经营企业签订协议,经营企业应当与境外生产企业签订协议,明确双方责任,保证药品质量。
制定责任风险分担和免责相关规定。在用药前,医生应向患者明确说明病情、用药风险和其他需要告知的事项,并取得书面知情同意;不能或者不宜向患者说明的,应当向患者的近亲属说明,并取得其书面知情同意。
六、国务院授权的省、自治区、直辖市人民政府可参照本工作方案结合自身工作实际制定相应工作程序及要求。
氯巴占临时进口工作方案(征求意见稿)
为满足氯巴占临床用药急需,根据《临床急需药品临时进口工作方案》有关规定,制定氯巴占临时进口工作方案。
一、申请工作流程
(一)国家卫生健康委组织提出氯巴占临床需求量,确定使用医疗机构名单,选定牵头进口的医疗机构,组织拟订药品使用规范和处方资质要求,明确患者知情同意和医生免责要求。
(二)牵头进口的医疗机构应向国家药监局提出临时进口申请,并按要求提供以下材料:
1.医疗机构的机构合法登记文件复印件(如医疗机构执业许可证、营业执照(如有)、组织机构代码证等)。
2.申请报告及承诺书。内容应包括:申请医疗机构的名称、地址及联系人信息。医疗机构书面承诺拟进口药品在指定医疗机构内用于特定医疗目的,不得用于申请用途以外的其他用途。
3.拟进口药品清单。内容应包括:药品名称、剂型、规格、进口数量、境外持有人名称地址、生产企业名称地址、药品产地、拟申报通关的口岸名称。
上述材料须加盖医疗机构公章。
同时,牵头进口的医疗机构可委托进口单位办理进口准许证。进口单位应按照国家药监局网上办事大厅公布的供临床使用麻醉药品和精神药品的进口审批办事指南,提出进口准许证申请,具体材料包括:
4.精神药品进口申请表。
5.购货合同或订单复印件。
6.医疗机构委托代理协议复印件。
7.进口单位的《营业执照》《对外贸易经营者备案登记表》复印件。
8.出口单位如为该药品的销售代理公司,还需提供委托代理协议和出口单位合法资质证明文件、公证文本以及认证文本。
9.申报资料真实性自我保证声明。
上述1-9项材料可同步提交,因申请单位自身原因无法同步提交的,也可将1-3部分及4-9部分分别提交。
(三)国家药监局收到医疗机构相关申请后,对符合要求的,在3个工作日内以局综合司函形式作出同意进口的复函,复函抄送国家卫生健康委、各省级药品监督管理部门及口岸药品监督管理部门,国家卫生健康委抄送各省级卫生健康主管部门。同时,出具进口准许证。
(四)进口单位持进口准许证直接向海关办理通关手续。此类进口药品,无需进行口岸检验。
二、药品使用管理
使用临时进口药品的医疗机构应按照《医疗机构药事管理规定》,重点做好以下工作:
(一)制定临床技术规范,明确药品的临床诊治用途、患者群体、使用科室及医生名单;建立专项管理制度,对医师处方、用药医嘱的适宜性进行审核,严格规范医师用药行为。
(二)监测记录临时进口药品使用相关的临床诊疗病历及药品安全性、有效性、价格、依从性、不良反应等信息数据,并应当长期保存。若发生严重不良反应,及时通报医疗机构所在省份的药品监督管理部门、卫生健康主管部门、国内药品经营企业。省级药品监督管理部门与省级卫生健康主管部门共同研判临床用药风险,必要时采取停止使用等紧急控制措施,并分别报告上级主管部门。
(三)制定完善的安全防范措施和风险监控处置预案。
(四)应按规定对临时进口药品合理储存。
(五)应按年度对临时进口药品进行评估,并报告省级卫生健康主管部门。
(六)按规定选取药品经营企业开展采购、进口和配送临时进口药品等相关工作。
(七)依托《中国罕见病诊疗服务信息系统》和全国罕见病诊疗协作网加强药品使用的科学化管理。
三、处方医师的资质条件和管理要求
(一)从事癫痫或儿童癫痫诊治10年以上,副主任医师或主任医师;
(二)具有麻醉药品和精神药品处方权;
(三)有使用苯二氮䓬类治疗癫痫的临床使用经验;
(四)能够严格掌握氯巴占的适应证(限癫痫);
(五)熟悉氯巴占的用法用量、治疗效果评估、不良反应监测与处理;
(六)按照目前各自所在医院苯二氮䓬类药品使用要求,且每张处方最多不得超过1个月用量。
四、相关方权责
牵头的医疗机构、经营企业依法对临时进口药品承担风险责任。医疗机构应当与经营企业签订协议,经营企业应当与境外生产企业签订协议,明确双方责任,保证药品质量。
制定责任风险分担和免责相关规定。在用药前,医生应向患者明确说明病情、用药风险和其他需要告知的事项,并取得书面知情同意;不能或者不宜向患者说明的,应当向患者的近亲属说明,并取得其书面知情同意。
来源:医谷网
为你推荐
 资讯
资讯 欧洲肥胖大会:诺和诺德Wegovy在所有绝经阶段的女性中均实现了显著减重
丹麦当地时间5月12日,诺和诺德公布数据显示,Wegovy(诺和盈)在女性肥胖症患者不同生育生命阶段中均达成了显著且一致的减重效果,涵盖绝经前阶段、绝经期和绝经后阶段[1]。绝...
2026-05-13 12:59
 资讯
资讯 伊米诺康完成 2.5 亿元 A 轮融资 加速打造全球领先全人源抗体发现平台
本轮融资由维梧资本领投,高脉元航跟投,老股东熙诚金睿、泰煜投资大比例超额追加投资,资金将重点用于核心技术迭代、平台商业化落地与创新能力升级。
2026-05-13 09:58
 资讯
资讯 减重之后怎么办?礼来ECO最新数据将行业视线推向“长期维持”
2026年5月13日,礼来公布SURMOUNT-MAINTAIN和ATTAIN-MAINTAIN两项后期临床研究详细结果。
2026-05-13 09:53
 资讯
资讯 147亿,A股医药板块有史以来最大的年度亏损
147亿,A股医药板块有史以来最大的年度亏损。近日,A股疫苗明星企业智飞生物(300122 SZ)发布的2025年年报公布了这一“成绩”。这也是智飞生物上市以来首个亏损。
2026-05-12 20:21
 资讯
资讯 恒瑞医药与BMS达成总交易额可达约152亿美元的战略与许可合作
本次合作协议共包含 4 项恒瑞肿瘤学及血液学项目、4 项 BMS 免疫学项目,以及双方依托恒瑞研发引擎与多元创新技术平台共同研发的 5 项创新项目,值得注意的是,这13在研...
2026-05-12 13:40
 资讯
资讯 徐和平教授荣膺国际视觉与眼科研究协会(ARVO)金质会士(FARVO Gold)荣誉称号
近日,国际视觉与眼科研究协会(The Association for Research in Vision and Ophthalmology, ARVO)在美国丹佛召开的2026年年会上正式公布了本年度金质会士(ARVO Gold Fellow,FARVO)评选结果。
2026-05-12 13:35
 资讯
资讯 中国生物技术发展中心:细胞组分及衍生物治疗新技术临床研究备案指引(第1版)
本指引适用于在我国境内开展的非以药品注册为目的的细胞组分及衍生物治疗新技术临床研究,本指引所指的细胞组分及衍生物治疗新技术不依赖完整活细胞,是指利用人自体或异体干细...
2026-05-12 10:05
 资讯
资讯 迈瑞遭证监会监管六问
5月8日,中国证监会对外公布最新一期《境外发行上市备案补充材料要求》(2026年4月27日—2026年5月8日),国际司共对7家企业出具补充材料要求,其中包括已于2025年11月10日向港交...
2026-05-10 19:21
 资讯
资讯 复星医药至多10.15亿元取得两款FAK抑制剂中国大陆区域独家商业化权利
5月8日,应世生物宣布与复星医药达成战略合作。根据协议约定,应世生物将授予复星医药其自主开发的两款创新 FAK 抑制剂IN10018(Ifebemtinib)、IN10028在中国(不含港澳台地...
2026-05-09 16:14
 资讯
资讯 河南省药监局局长正接受纪律审查和监察调查
据河南省纪委监委消息:河南省市场监督管理局党组成员,省药品监督管理局党组书记、局长田文才涉嫌严重违纪违法,目前正接受河南省纪委监委纪律审查和监察调查。
2026-05-09 12:55
 资讯
资讯 这家市值仅23亿的科创板上市公司要筹划控制权变更
5月7日晚间,仁度生物(688193 SH)发布公告于2026年5月8日(星期五)开市起停牌。停牌原因,公告显示为公司控股股东、实际控制人居金良正在筹划可能导致公司控制权发生变更的重大事项。
2026-05-09 10:30
 资讯
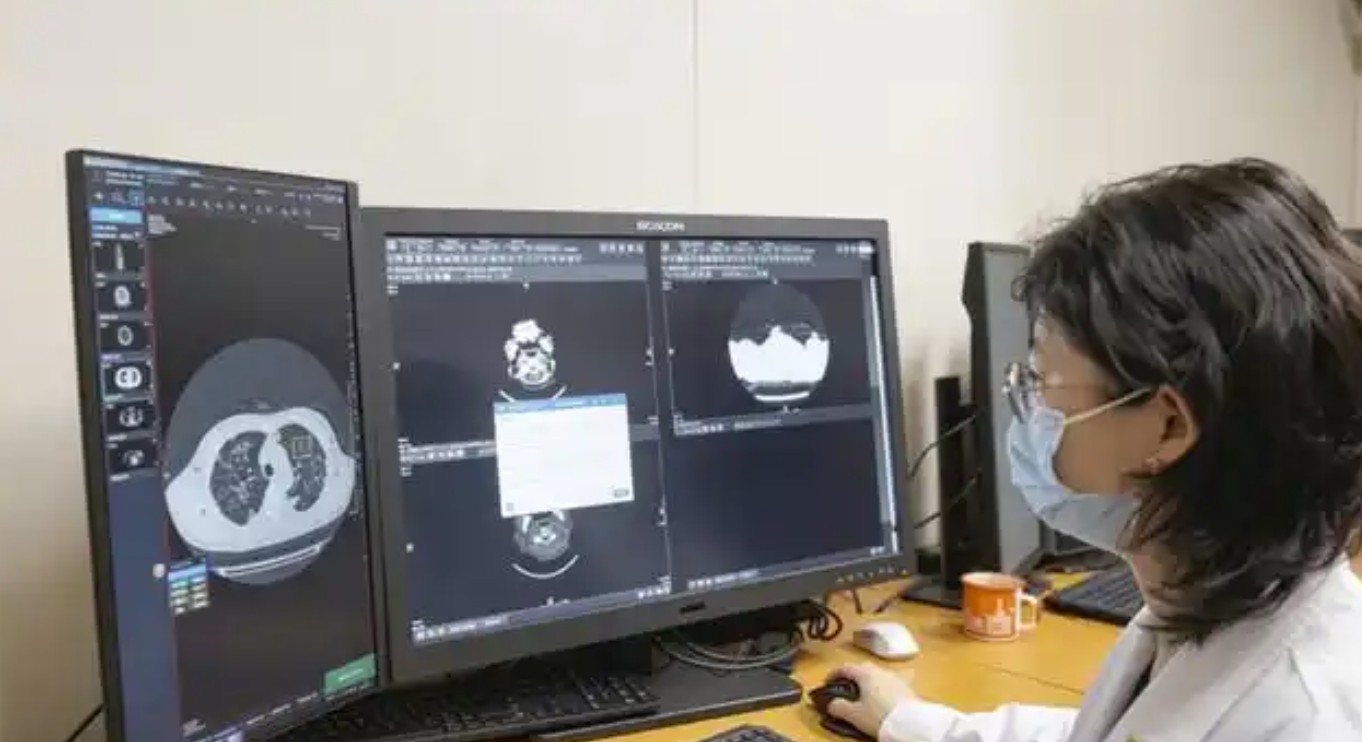
资讯 全国首款大模型多病种AI医疗产品进入国家药监局创新医疗器械特别审查程序
近日,国家人工智能应用中试基地(医疗领域)中试推广的智能应用——胸部CT图像辅助诊断软件,成功进入国家药监局创新医疗器械特别审查程序。这是全国首款进入该审查通道的大模...
2026-05-08 13:57
 资讯
资讯 国家集采,儿童专用药与成人用药将分组采购
5月7日,国家卫健委官网发布《关于改革完善儿童用药供应保障机制的实施意见》,明确提出在国家组织药品集中带量采购中,对儿童专用药与成人用药分组采购。
2026-05-08 11:19