在11月20日-22日召开的2020年欧洲肿瘤内科学会亚洲年会(ESMO ASIA 2020)上,多款PD-1/PD-L1单抗治疗非小细胞肺癌(NSCLC)的最新临床研究数据公布,包括基石药业GEMSTONE-302 III期研究(舒格利单抗+化疗一线治疗IV期NSCLC),罗氏IMpower132 III期研究(T药+化疗一线治疗IV期非鳞状NSCLC)、默沙东KEYNOTE-042 III期研究(K药一线治疗PD-L1阳性NSCLC)。
非小细胞肺癌(NSCLC)约占所有肺癌病例的85%,绝大部分肺癌患者诊断时已是晚期,这些病人可能会在1到2年内死亡。目前晚期NSCLC的主要治疗手段包括放疗、化疗、靶向治疗、免疫治疗等。众所周知,化疗单药治疗的副作用很大,治疗效果未尽如人意,患者依从性和生活质量不高。含铂双药化疗方案相比更早期的化疗方案带来了疗效的改善,安全性更佳,已成为NSCLC的一线标准治疗方案。另一方面,对于具有驱动基因突变/变异(EGFR、ALK、ROS1、BRAF等)的人群,相比化疗,靶向治疗药物为患者带来更长的生存时间,同时药物安全性更好,口服给药更为方便。但并未解决所有问题,靶向治疗对驱动基因突变阴性的患者无效,存在巨大的未被满足的医疗需求。
近些年来,以PD-1/PD-L1抑制剂为代表的免疫治疗因为有效时间长、副作用小而受到广泛关注,成为了目前研究最火热的治疗方式。无论是单药治疗还是联合治疗,都取得了不错的结果。相对化疗的毒副作用,免疫治疗相关不良反应要降低了很多,特别是为无驱动基因突变的患者带来了更好的治疗选择。今年,中国临床肿瘤学会(CSCO)在线发布《非小细胞肺癌诊疗指南2020》,最大亮点之一莫过于几款PD-1/PD-L1抑制剂被推荐为NSCLC一线和二线治疗。
目前,国内已经批准上市约8款PD-1/PD-L1单抗药物,4款PD-1/PD-L1单抗获批了NSCLC相关适应症。下一款获批上市的药物可能很快就会出现,本月初,国家药监局受理了此次亮相ESMO ASIA 2020大会的舒格利单抗(基石药业, PD-L1抗体)联合化疗一线治疗NSCLC的上市申请。
在ESMO ASIA 2020上,上海市肺科医院肿瘤科主任周彩存教授首次公布了III期研究(GEMSTONE-302)的详细数据。在官方早前的报道可以看出,该药在最早临床方案设计的时候,是全球首个抗PD-L1单抗联合化疗作为一线治疗在IV期鳞状和非鳞状NSCLC患者中的随机双盲III期临床试验。
创新临床设计
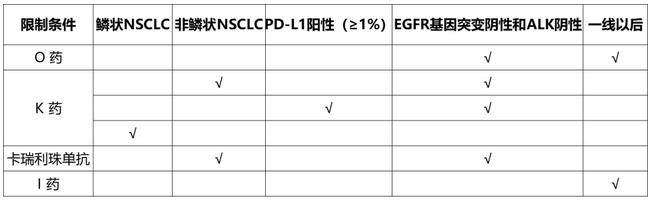
根据临床试验的设计不同,几款已上市的PD-1/PD-L1药物获批的适应症也有所差异,这些限制因素是由于疾病分期、病理亚型、肿瘤标记物的不同而异的。部分PD-1/PD-L1单抗治疗被限制用于化疗、靶向治疗药物治疗失败的患者,而非用于一线治疗。通常,为了提高临床试验的成功率,EGFR基因突变阴性和ALK阴性、PD-L1阳性(≥1%)等被设置为患者入组的筛选条件。
NSCLC可分为非鳞癌和鳞癌,根据病理组织而异,这两种类型的治疗方案也是截然不同的。两者常见的驱动基因突变/变异(EGFR、ALK、ROS1、BRAF等)不同,使用的主要标准化疗方案和靶向药物也不尽相同。根据国外的临床入组经验,国内PD-1/PD-L1单抗临床试验设计中,常常将两种类型的NSCLC分为两个研究来进行患者的入组。
国内几款PD-1/PD-L1单抗获批的NSCLC具体适应症
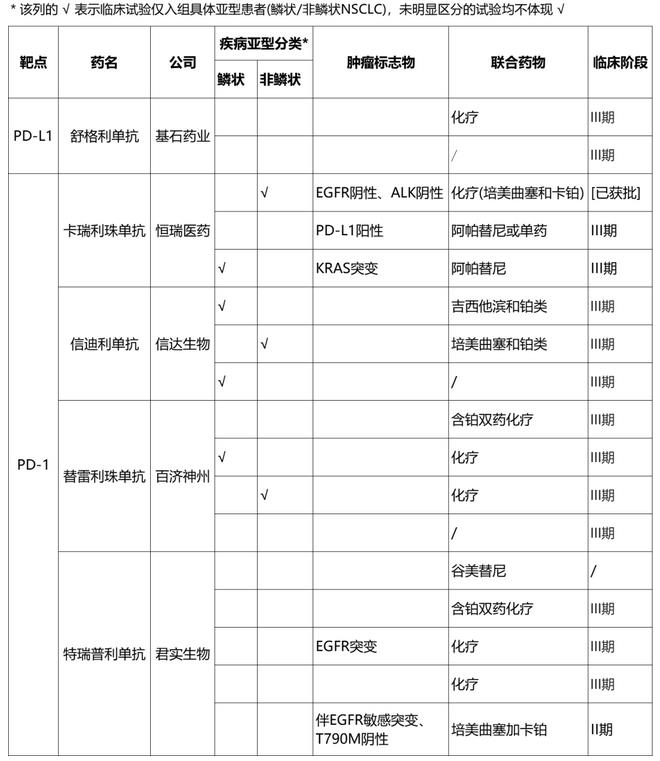
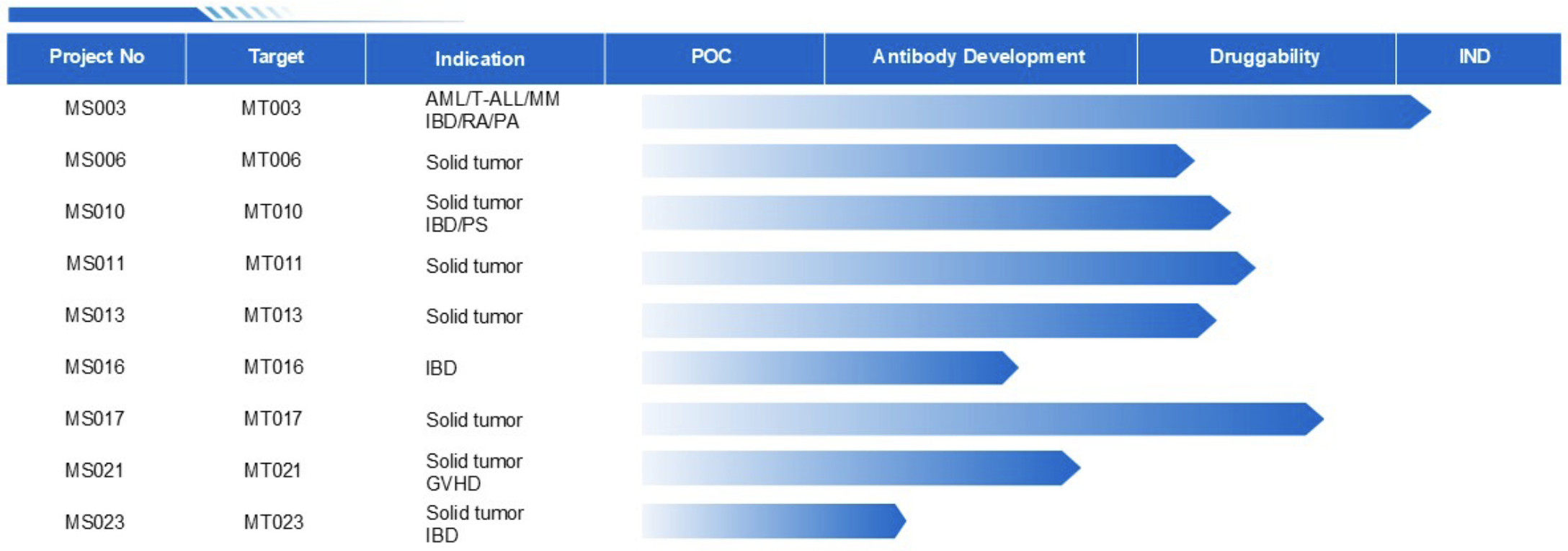
部分PD-1/PD-L1单抗治疗NSCLC的国内临床试验进展
相比一线单纯化疗治疗方案,多项研究证实免疫联合化疗作为一线治疗晚期NSCLC能够降低疾病进展风险,因此整体来看,以上大部分NSCLC临床试验都采用了联合治疗模式,但多数针对一种类型的肺癌患者,非鳞癌或鳞癌,或者有肿瘤标志物表达的限制。
更广泛的适用人群
那么,有没有一种PD-1/PD-L1的联合治疗方案可以同时涵盖更多类型的NSCLC患者?
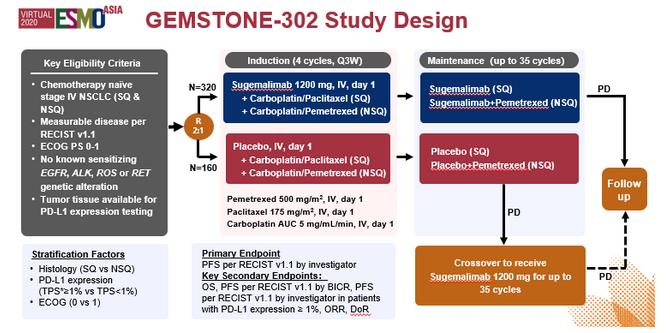
周彩存教授之前也在采访中提到,GEMSTONE-302 III期研究创新性地将鳞癌和非鳞癌一同研究,采用免疫联合化疗,对照安慰剂联合化疗的研究设计,用一个临床研究攻克所有NSCLC,并且最大程度地贴近国内患者临床情况,入组的鳞癌患者不超过40%,剔掉PD-L1阴性的病人不能超过40%。
GEMSTONE-302研究设计
综合判断,该药可以覆盖大部分IV期NSCLC患者的一线治疗,包括鳞癌和非鳞癌,且不管PD-L1表达水平如何。临床试验的巧妙设计也将为舒格利单抗的上市铺路,临床数据具有代表性,尽可能地模拟真实世界的情况。
临床效果和安全性如何?
根据ESMO ASIA 2020上公布的最新数据,治疗IV期NSCLC,这款联合疗法显著延长患者的无进展生存期(PFS),降低患者疾病进展或死亡风险(HR)50%!
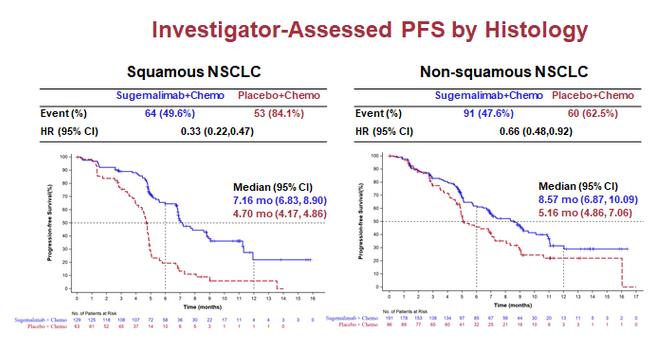
截至2020年6月8日,入组的479例患者分别接受舒格利单抗联合化疗对比安慰剂联合化疗,在包含鳞状和非鳞状NSCLC的所有患者中,研究者评估的中位PFS由对照组的4.9月提高到7.8月,风险比HR =0.5 (95% CI: 0.39, 0.64),p<0.0001;盲态独立中心审查委员会(BICR)评估的中位PFS由对照组的4.9月提高到8.9月,风险比HR=0.54(95%CI:0.41,0.70), p<0.0001。其中:<>
鳞癌患者中,中位PFS分别为7.16月 vs 4.70月,HR=0.33;
非鳞癌患者中,中位PFS分别为8.57月 vs 5.16月,HR=0.66。
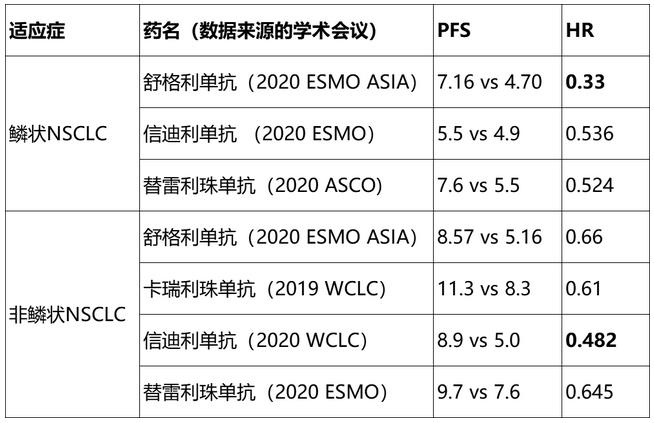
对比几款PD-1/PD-L1单抗在近期大型学术会议上公布的数据,这款PD-L1抗体同样值得期待。尤其是在鳞癌患者中,这款降低患者疾病进展或死亡风险(HR=0.33)67%,与对照组化疗相比疗效显著,并且在国产PD-1/PD-L1单抗中表现出色。
近期国产PD-1/PD-L1治疗NSCLC的临床数据
GEMSTONE-302研究结果也显示出良好的安全性,未发现新的安全性信号。
未来可期
目前已有2个PD-L1抗体在中国获批,均为进口药物,用于晚期小细胞肺癌(SCLC)的一线治疗和III期NSCLC的巩固治疗,尚无治疗晚期NSCLC的适应证获批。据悉,不久前,国家药监局已基于这项III期临床研究结果受理舒格利单抗的新药上市申请(NDA),基于以上出色的临床试验结果,中国自主原创新药舒格利单抗有望填补这一空白,成为最早在国内获批用于一线治疗晚期NSCLC的PD-L1抑制剂。最近,基石药业先后与制药巨头辉瑞和EQRx达成的两项有关舒格利单抗的战略合作,足以看出其治疗潜力和市场前景。
非小细胞肺癌进入免疫治疗时代,但是针对特定人群的治疗受益还有很多未解决的问题,我们希望更多类似舒格利单抗的新药能够早日上市,为患者带来更多的治疗选择,为国内肺癌的一线免疫治疗格局带来突破。
参考出处:
[1] ESMO ASIA 2020 | 基石药业公布GEMSTONE-302研究结果,舒格利单抗可为晚期非小细胞肺癌患者提供新治疗选择
[2] 张盼, 张俊萍. 晚期非小细胞肺癌PD-1/PD-L1单抗治疗临床转化现状[J], 中国肿瘤生物治疗杂志,2018,25(4).
[3] 各大学术会议公开数据
来源:医麦客 作者:陈婉仪
为你推荐
 资讯
资讯 甘李药业一款PROTAC药物完成临床试验I期首例入组
4月3日,甘李药业(603087 SH)发布公告称,其自主研发的GLR2037于近日成功完成Ⅰ期临床试验首例受试者给药。本次临床试验拟开展的适应症为晚期前列腺癌。
2026-04-05 19:55
 资讯
资讯 人工智能公司 Anthropic 4亿美元收购生物科技初创公司Coefficient Bio
据国外多家媒体消息,人工智能公司Anthropic已以4亿美元收购了生物科技初创公司Coefficient Bio。
2026-04-05 19:30
 资讯
资讯 众多行业顶级机构参与,益生菌千亿市场将迎大洗牌
近日,国家市场监管总局就《保健食品原料 益生菌》国家标准向社会公开征求意见,意见反馈截至5月29日。该标准的制定填补了我国保健食品原料益生菌质量标准的空白,将从源头规范...
2026-04-05 18:56
 资讯
资讯 无法保供,两家企业被取消国家集采药品中选资格并被列入违规名单
4月3日,国家组织药品联合采购办公室发布公告,取消2个国家组织药品集采中选药品中选资格并将相关企业列入违规名单。
2026-04-04 17:13
 资讯
资讯 自4月起,国家医保局开展医保药品领域违法违规问题专项行动
专项行动开始时间为自2026年4月起,分为两个阶段,第一阶段为2026年4月至7月,第二阶段为2026年9月至11月。国家医保局将于2026年4月初和9月初分别下发一批药品追溯码重复结算疑点线索。
2026-04-03 13:24
 资讯
资讯 上海交大携手蚂蚁健康,发起成立“AI4HealthCare联合实验室”
近日,上海交通大学人工智能学院与蚂蚁健康在上海签署合作协议,将共同发起“AI4HealthCare联合实验室”,围绕医疗领域专科智能体的研发、临床适配应用等开展联合攻坚。
2026-04-03 12:45
 资讯
资讯 美赛生物完成超 1.5 亿人民币 A 轮融资,巨噬细胞靶向药物研发加速推进
本轮融资由康君资本领投,宏沣投资、瑞华资本、行业头部投资机构和知名产业基金共同参与,舟渡资本担任独家财务顾问。
2026-04-03 11:22
 资讯
资讯 耀速科技完成超2亿元A轮融资,AI+器官芯片赋能新药研发新范式
本轮融资由国寿股权独家领投,老股东晶泰科技、雅亿资本、君联资本持续加码,资金将重点投入下一代生物智能基础设施构建,加速技术产业化落地,推动新药研发范式革新。
2026-04-03 11:15
 资讯
资讯 Orforglipron获批背后:FDA“优先审评券”首迎新分子实体
根据FDA发布的信息,Orforglipron是在“局长国家优先审评券(Commissioner s National Priority Voucher,CNPV)”试点项目下获得批准的第五款药物,也是该项目下首个获批的新分子实体。
2026-04-03 11:04
 资讯
资讯 加速增长:拜耳处方药史上最强的产品组合和前景广阔的研发管线
2025年创下纪录,获得五项首次获批(三项新产品获批、两项新适应症获批),以及六项积极III期临床试验结果,预计2026年将在重点治疗领域取得多项关键研发管线里程碑
2026-04-02 13:03
 资讯
资讯 国家卫健委:基层医疗卫生机构医疗质量改善三年行动方案(2026—2028年)
紧密型县域医共体牵头医院负总责,乡镇卫生院(社区卫生服务中心)主要负责人是第一责任人;“区社一体”牵头医院负总责,社区卫生服务中心主要负责人是第一责任人。
2026-04-01 21:49
 资讯
资讯 傍云医疗完成近亿元天使轮融资,加速高端伤口缝合国产替代与全球创新
本轮融资由道彤投资领投,金鼎资本跟投,所募资金将全面用于高端伤口闭合耗材的产能扩建、核心原料国产化攻关、全球首创创新产品研发及商业化推进,加速推动中国高端伤口缝合产...
2026-03-31 12:48
 资讯
资讯 诺和诺德每周一次长效基础胰岛素Awiqli在美国获批
诺和诺德近日宣布,美国食品药品监督管理局(FDA)已批准Awiqli(insulin icodec-abae,国内通用名依柯胰岛素注射液、商品名诺和期)注射液700单位 mL。
2026-03-30 16:34
 资讯
资讯 “医学影像大模型第一股”德适登陆港交所,开盘大涨121%
上市首日,德适以每股99港元的发行价开盘,股价随即大幅飙升,盘中最高涨幅达121%,报219港元,市值迅速突破200亿港元
2026-03-30 12:39