乳腺癌是女性中最常见的癌症类型之一,在过去50年里,随着科学和医学的不断发展,我们在诊断和治疗乳腺癌方面取得了显着进展,将这一疾病的死亡率降低了40%。对于乳腺癌患者来说,不但有包括放疗和手术治疗在内的局部疗法,还有化疗和多种靶向疗法作为全身性治疗选择。科学家和药物研发人员还在不断开发创新疗法,旨在进一步消除肿瘤复发的风险,延长患者的生命。
新药研发是一个耗时而且耗力的过程,一款新药经常需要10来年才能够来到患者身边。而在人体中进行的临床试验通常是新药研发过程中耗时最长,成本最高的部分。如果能够对临床试验过程进行精简,不但可能降低新药研发的成本,还可能加速把新药送到患者手中。
近日,美国FDA肿瘤卓越中心主任,FDA药物评估和研究中心血液学和肿瘤学产品办公室代理主任Richard Pazdur博士带领的团队在《新英格兰医学杂志》上发表评论,探讨了如何从临床试验的设计角度,加快乳腺癌新药的开发,造福“高危早期”患者。
传统临床试验的设计局限
乳腺癌创新全身性疗法的开发通常从治疗转移性乳腺癌患者开始,这种类型的患者的乳腺癌已经扩散到全身其它组织,她们的中位总生存期不到两年。获得批准治疗这些患者之后,研发过程的下一步是检测这些创新疗法能否用于治疗早期乳腺癌患者。毕竟,大部分乳腺癌患者在最初确诊时肿瘤尚未转移到全身,这些患者通常接受的疗法是通过手术切除肿瘤或者乳房,然后使用辅助疗法(adjuvant therapy)控制乳腺癌的复发。根据乳腺癌类型的不同,辅助疗法可能是化疗,内分泌疗法或者靶向疗法,例如基因泰克公司着名的靶向HER2+乳腺癌的赫赛汀(Herceptin)。
然而,当创新疗法需要通过临床试验证明在早期乳腺癌患者中也能够产生疗效时往往会遇到在临床试验方面的挑战。因为以前的临床试验设计是先对早期乳腺癌患者进行手术,然后在手术后的患者群中检验创新疗法的疗效。而目前已有的辅助疗法,在接受过手术疗法的早期乳腺癌患者中已经能够达到非常好的疗效,防止超过90%的患者的癌症复发。想要证明创新疗法比已有疗法更好,需要募集几千名患者,才能达到足够的样本数目,从统计学上分辨出疗效的差异。而且,由于大多数患者的癌症不会复发,以传统的无进展生存期(PFS)或者总生存期(OS)为临床终点的试验需要等待很长时间,才可能观察到创新疗法和已有疗法在临床终点上的区别。这意味着,传统的临床试验设计可能导致一项获批治疗转移性乳腺癌的创新疗法,需要等上10多年的时间,才能获批治疗早期乳腺癌患者。这严重推迟了创新疗法在早期乳腺癌患者身上的应用。特别是有些患者的肿瘤侵袭性很强,复发风险很高,对于这些患者来说,一款有效的新疗法可能挽救她们的生命。那么,有没有什么办法在临床试验方面加快针对早期乳腺癌患者的创新疗法的开发速度呢?
新辅助疗法和病理学完全缓解
美国FDA也认识到了传统临床试验设计以及试验终点对治疗早期乳腺癌患者的创新疗法的研发可能产生的阻碍。在2012年,FDA推出病理学完全缓解(Pathological Complete Response, pCR)作为获得FDA加速批准的替代终点。那么什么是病理学完全缓解呢?这要从近年来应用越来越广的新辅助疗法(neoadjuvant therapy)说起。
传统的辅助疗法是在乳腺癌患者接受手术切除肿瘤或者乳腺之后,使用全身性疗法防止癌症复发。而新辅助疗法是在患者接受手术之前就接受全身性化疗、内分泌疗法或靶向疗法的治疗,在接受全身性疗法一段时间后再进行手术。与辅助疗法相比,新辅助疗法可以提供几个优点:一,在进行手术之前使用全身性疗法可能减小肿瘤的大小,从而保存乳腺组织或者避免乳房切除手术。二,手术前进行药物治疗可以实时监控肿瘤对药物的反应,从而尽早停止无效疗法。三,患者对手术前新辅助疗法的反应可能为预后表现提供更多线索。最后,新辅助疗法给研究人员独特的机会分析肿瘤从最初组织活检到手术切除时这段时间的演变,为采用个体化的最佳疗法提供了更多信息。
接受新辅助疗法的患者最终还是需要接受手术切除肿瘤,pCR是描述乳腺癌患者在完成新辅助疗法之后的病情指标。根据FDA的指南,pCR的定义是,在完成新辅助疗法之后,在切除的乳房和周围取样的淋巴结中不存在残余的侵袭性(和原位)肿瘤。以往的研究表明,pCR与早期乳腺癌患者的预后状况相关。在接受新辅助疗法后达到pCR的患者乳腺癌复发的风险较小,而未达到pCR的患者乳腺癌复发的风险显着提高。这本身也是很容易理解的事,因为如果全身性疗法在手术前就可以消灭侵袭性肿瘤,那么意味着肿瘤对全身性疗法敏感,因此在手术之后继续使用全身性疗法有更大可能控制疾病不再复发。
基于pCR作为替代终点,美国FDA在2013年加速批准了帕妥珠单抗(pertuzumab)作为新辅助疗法治疗HER2+早期乳腺癌患者。在名为NeoSphere的临床试验中,在标准治疗方案中加入帕妥珠单抗将pCR比例从21%提高到39%。在帕妥珠单抗获批上市之后,随后名为APHINITY的上市后临床试验使用传统临床试验设计验证了帕妥珠单抗作为辅助疗法的疗效。然而,这一临床试验招募了4804名早期乳腺癌患者,中位随访时间达到45.4个月,获得的数据支持帕妥珠单抗获批作为辅助疗法时已经是2017年12月。这意味着以pCR作为替代终点做出的加速批准让早期乳腺癌患者提前4年获得了最新疗法。
筛选高危早期乳腺癌患者
pCR不但可以作为替代终点加速创新疗法的批准,它还可以作为筛选标准找出乳腺癌复发风险更高的早期乳腺癌患者。未达到pCR的患者因为癌症复发风险更高,更需要尽早获得创新疗法的治疗。一方面,这些患者更倾向于加入检验创新疗法的临床试验,因为她们知道已有疗法可能不能有效阻止癌症的复发。另一方面,这些患者在临床试验期间,身上出现肿瘤复发和其它与癌症恶化相关事件的几率升高。因此,针对这些高危早期乳腺癌患者的临床试验不但可能更早完成患者注册,而且与传统的辅助疗法临床试验相比,更早得出试验结果。
这种使用pCR筛选高风险早期乳腺癌患者进行临床试验的试验设计已经得到了应用。日前,基因泰克公司开发的Kadcyla(ado-trastuzumab emtansine)作为辅助疗法治疗接收过新辅助(neoadjuvant)疗法的高危早期HER2+乳腺癌患者的临床试验结果在《新英格兰医学杂志》上发表。在名为KATHERINE的临床试验中,只有接受新辅助疗法后未达到pCR的患者被纳入下一步的临床试验,接受了Kadcyla或赫赛汀的辅助治疗。中期试验结果分析表明,Kadcyla与赫赛汀相比,能够将患者癌症复发或死亡风险降低50%。基于这一结果,FDA授予Kadcyla突破性疗法认定,并且将使用实时肿瘤学审评(RTOR)机制审评Kadcyla的补充生物制剂许可申请。这意味着Kadcyla可能不久就可以用于治疗高危早期乳腺癌患者。
结语
美国每年有26万妇女被诊断出患有乳腺癌。在即便接受传统疗法,癌症复发风险仍然偏高的患者群中检验创新疗法不但能够降低她们的经济负担,而且能够加快开发和批准具有潜在治愈效果的新疗法的速度。
未来,我们需要预测预后结果的生物标志物来找出高危患者,以便及时进行干预,从而改善她们的治疗后果。在新辅助疗法过程中切除的残余疾病组织提供了一个机会,让研究人员可以探索那些能够预测肿瘤对新疗法反应的生物标志物。这些生物标志物的信息可能让研究人员在随后的临床试验中,更好地划分患者群。与此同时,接受新辅助疗法后的残留疾病应该被作为一个重要的生物标志物,帮助在治疗早期乳腺癌患者的临床试验中选择患者。这不但将提高试验效率,而且将帮助为具有最大未满足医疗需求的患者开发创新疗法。
参考资料:
[1] Guidance for Industry: Pathological Complete Response in Neoadjuvant Treatment of High-Risk Early-Stage Breast Cancer: Use as an Endpoint to Support Accelerated Approval. Retrieved February 14, 2019, from https://www.fda.gov/downloads/Drugs/GuidanceComplianceRegulatoryInformation/Guidances/UCM305501.pdf
[2] Powell et al., (2019). Residual Disease after Neoadjuvant Therapy — Developing Drugs for High-Risk Early Breast Cancer. NEJM, DOI: 10.1056/NEJMp1900079
[3] Roche submits supplemental biologics license application to US FDA for Kadcyla for adjuvant treatment of people with HER2-positive early breast cancer with residual disease after neoadjuvant treatment. Retrieved February 15, 2019, from https://globenewswire.com/news-release/2019/02/05/1710281/0/en/Roche-submits-supplemental-biologics-license-application-to-US-FDA-for-Kadcyla-for-adjuvant-treatment-of-people-with-HER2-positive-early-breast-cancer-with-residual-disease-after-n.html
[4] If You Have Breast Cancer. Retrieved February 15, 2019, from https://www.cancer.org/cancer/breast-cancer/if-you-have-breast-cancer.html
来源:药明康德
来源:药明康德
为你推荐
 资讯
资讯 刚果(金)与乌干达埃博拉疫情:国际SOS发布企业员工支持建议
近日,世界卫生组织(WHO)宣布,当前影响刚果民主共和国和乌干达的埃博拉疫情构成“国际关注的突发公共卫生事件”(PHEIC)。
2026-05-22 13:47
 资讯
资讯 早筛 戒烟 筑牢膀胱癌第一道防线
每年的5月是“膀胱关爱月”,根据国家癌症中心发布的《2024年全国癌症报告》显示,膀胱癌位居我国恶性肿瘤发病第 11 位。2022年中国膀胱癌发病率为7 3 10万人,死亡率为4...
文/刘思 2026-05-22 13:31
 资讯
资讯 再鼎医药总裁兼首席运营官离职
5月22日早间,再鼎医药发布公告称,公司董事会已于5月18日决定,Josh Smiley不再担任公司总裁兼首席运营官,相关决定自当日起生效,其在公司的最后任职日期为5月22日。
2026-05-22 11:45
 资讯
资讯 共建多元支付,加速创新可及:镁信健康与辉瑞中国达成战略合作
双方将依托长期合作基础,以多元支付为基石,以数据洞察和AI技术为引擎,加速前沿创新药落地中国,全方位提升患者用药可及性与健康服务体验,助力构建多层次医疗保障体系。
2026-05-21 17:57
 资讯
资讯 拜耳可申达(非奈利酮片)在中国获批用于LVEF≥40%的心力衰竭成人患者
拜耳宣布中国国家药品监督管理局(NMPA)批准高选择性非甾体类盐皮质激素受体拮抗剂可申达(非奈利酮片)用于射血分数(LVEF)≥40%的心力衰竭成人患者,以降低心血管死亡、因心...
2026-05-21 17:51
 资讯
资讯 冯慧宇教授:从“活下去”到“活得好”,重症肌无力迈入精准治疗时代
作为深耕重症肌无力领域数十年的临床专家,她用一个个真实的患者故事,揭示了这个有着 300 多年历史的古老疾病在当代诊疗中的核心痛点,并分享了对创新药发展和患者全程管理的...
文/张蓉蓉 2026-05-21 15:48
 资讯
资讯 2026年“家庭健康促进计划-健康同行1+1公益项目” 在西安医学院正式启动
5月18日,由中国妇女发展基金会主办,陕西省妇联、陕西妇女儿童发展基金会、西安医学院协办,默沙东公益支持的“家庭健康促进计划-健康同行1+1公益项目西安高校健康跑暨2026启动...
2026-05-21 15:37
 资讯
资讯 爱尔眼科补交税款及滞纳金5.24亿元
5月20日,爱尔眼科(300015 SZ)发布公告称,其根据国家税收法律法规相关要求进行自查后,需补缴税款3 48亿元,并支付滞纳金1 76亿元,合计金额达5 24亿元。目前,上述税款...
2026-05-21 15:36
 资讯
资讯 复宏汉霖引进第三代口服EGFR-TKI产品
近日,复宏汉霖宣布与江苏正大丰海制药有限公司及其旗下江苏创特医药科技有限公司达成战略合作。根据约定,复宏汉霖将获得由江苏创特自主研发的口服小分子三代表皮生长因子受体...
2026-05-21 11:28
 资讯
资讯 冠脉支架国家集采第二轮接续采购在天津开标,27个产品拟中选
5月20日,国家组织冠脉支架集中带量采购第二轮接续采购在天津开标。共15家企业的30个产品参与投标,投标企业全部中选,27个产品获拟中选资格。
2026-05-20 21:05
 资讯
资讯 因美纳发布年度企业责任报告,持续提升基因组学可及性,加速拓展全球影响力
报告重点介绍了公司在推动基因组学公平可及方面取得的持续进展,以及为全球患者、社区和医疗系统带来可衡量的影响
2026-05-20 18:14
 资讯
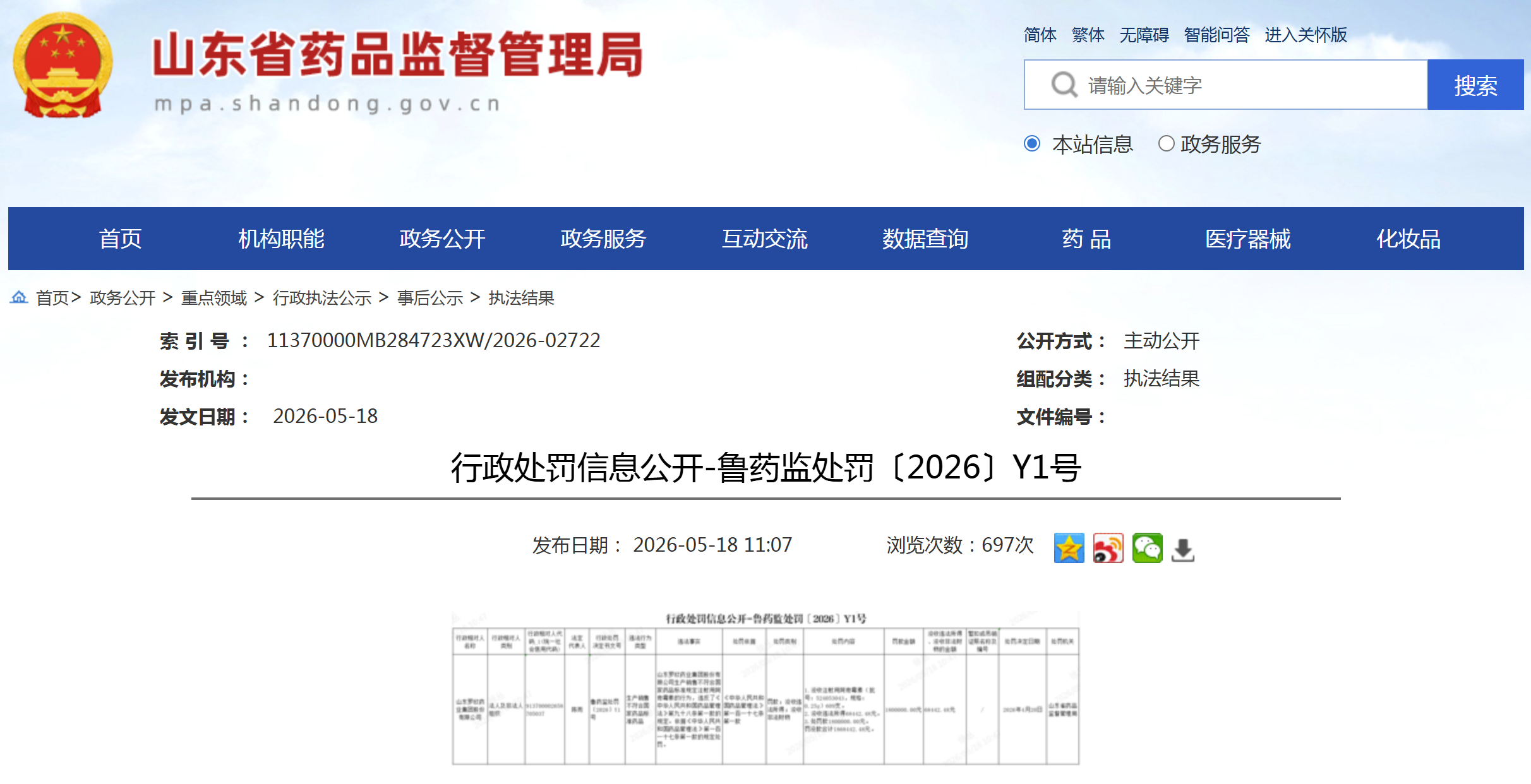
资讯 罗欣药业因生产劣药被处罚186万元
5月18日,山东省药监局发布的行政处罚信息显示,罗欣药业因生产销售不符合国家药品标准的注射用阿奇霉素,被处以没收药品609支、没收违法所得6 8万元并处罚款180万元,罚没款合...
2026-05-20 16:01
 资讯
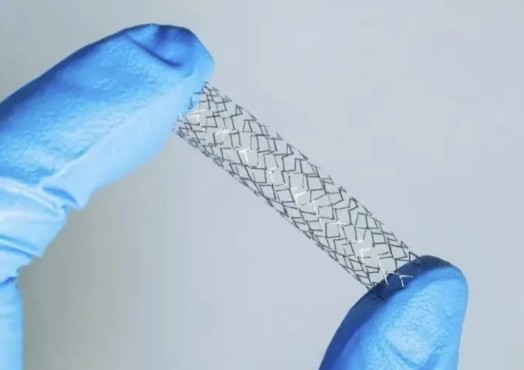
资讯 集采心脏支架临床使用超千万
2020年,心脏支架成为首批国家组织高值医用耗材集中带量采购品种,国内外企业的10个临床主流产品中选,普遍降至1000元以下,我国心脏支架基本告别“万元时代”。
2026-05-20 13:46
 资讯
资讯 我国启动首个128通道全植入式脑机接口系统多中心临床试验
5月18日,我国正式启动首个128通道全植入式脑机接口系统多中心临床试验,这项试验由首都医科大学附属北京天坛医院担任组长单位。
2026-05-19 21:08
 资讯
资讯 国产口服小分子GLP-1减重适应症完成III临床试验,即将申报NDA
5月18日,成都闻泰医药科技股份有限公司宣布,公司自主研发的每日一次口服小分子GLP-1受体激动剂VCT220片,在中国超重或肥胖受试者中的关键Ⅲ期临床试验取得积极顶线结果,计划...
2026-05-19 18:07
 资讯
资讯 辐联科技完成超 10 亿人民币融资,加速核药临床开发与全球同位素产能布局
本轮融资由全球医疗健康投资机构维梧资本领投,辐联科技战略合作伙伴 SK Biopharmaceuticals 以及成为资本、红杉中国、佳辰资本、楹联健康基金、Plaisance、Sky9、TSG 资本等多家优质机构跟投。
2026-05-19 18:02
 资讯
资讯 重磅,哪些药械产品纳入白名单,各省要在2026年9月底前统一建立定点零售药店职工医保个人账户支付白名单制度
5月19日,国家医保局官网发布《国家医保局办公室 财政部办公厅关于进一步加强定点零售药店职工基本医疗保险个人账户使用监督管理的通知》,提出要建立定点零售药店职工医保个...
2026-05-19 10:52




