近日,诺华在2022年第二季度业绩报中披露,基于FDA的反馈,诺华及其合作伙伴百济神州已经取消了在美递交替雷利珠单抗单药治疗非小细胞肺癌的上市申请。
至于放弃的原因,有外媒报道称,诺华首席执行官Vas Narasimhan透露,FDA已指出,百济神州开展的一项临床试验中,未能在患者人数以及使用的标准治疗方面充分突出美国群体。根据E药经理人的报道,亦有分析师认为,导致取消申请的主要原因是支持该适应症上市的Rationale-303这一随机、开放性、多中心的全球3期临床试验主要在中美洲和南美,中国和东欧进行。
据相关披露信息显示,该试验覆盖的国家有中国、巴西、保加利亚、立陶宛、墨西哥、新西兰、波兰、俄罗斯、斯洛伐克、土耳其10个国家,共86个临床站点,入组了805例患者,以2:1的比例随机至替雷利珠单抗试验臂或多西他赛试验臂。Rationale-303试验的主要终点为在全部患者(意向治疗患者人群)中以及在PD-L1高表达患者中的OS;关键次要终点包括客观缓解率(ORR)、缓解持续时间(DoR)、无进展生存期(PFS)及安全性。
虽然非小细胞肺癌适应症申请被搁置,但针对二线食管鳞癌的在美上市申请仍然在正常进行中。
7月14日,百济神州发布公告称,美国FDA因新冠肺炎疫情相关的旅行限制,无法如期在中国完成所需的现场核查工作,因此将延长替雷利珠单抗针对二线食管鳞癌新药上市许可申请(BLA)的目标审评完成时间,目前该项BLA仍在审评进程中(原本的BLA时间为7月12日),百济神州方面表示,FDA正在持续关注相关公共卫生状况和旅行限制,因此尚未提供更新的预期决议日期。
另悉,除了美国市场外,百济神州和诺华还在把目光市场机会投向欧洲市场,今年4月,百济神州宣布欧洲药品管理局(EMA)已受理替雷利珠单抗针对食管鳞状细胞癌和非小细胞肺癌的新药上市申请,对于非小细胞肺癌的上市申请既包括单药治疗也包括联合用药,主要是基于百济神州的3项临床试验(NCT03358875、NCT03594747、NCT03663205)的结果,这三项试验共纳入了1499例患者,其中包括一项RATIONALE 303试验。这是一项随机、开放性、全球3期临床试验,旨在对比替雷利珠单抗和多西他赛用于针对既往经含铂化疗后出现疾病进展的二线或三线局部晚期或转移性NSCLC患者。该试验在美洲、欧洲、亚洲和大洋洲的10个国家共入组了805例患者,患者以2:1的比例随机分配至替雷利珠单抗组或多西他赛组。百济神州已于2020年11月宣布,经独立数据监查委员会(IDMC)评估判断,该试验在计划的期中分析中达到了总生存期(OS)这一主要终点。替雷利珠单抗的总体耐受性良好,安全性特征与在各肿瘤类型中既往报告的已知风险一致,未出现新的安全性警示。
来源:医谷网
为你推荐
 资讯
资讯 这家药企停牌,ST,面临退市风险
6月10日晚间,湖南南新制药(688189 SH)发布公告,公司于6月9日收到中国证监会湖南监管局出具的《行政处罚事先告知书》(〔2026〕6号)。公司涉嫌信息披露违法违规行为被依法...
2026-06-10 22:27
 资讯
资讯 凯思凯迪完成 3.18 亿元 D 轮融资,加码胆汁酸代谢赛道,加速全球首创肝病创新药临床落地
本轮融资由太平医疗健康基金、上海科创集团联合领投,粤开资本、昭德投资、涟邦基金等多家专业医疗投资机构跟投
2026-06-10 18:56
 资讯
资讯 诺华泰菲乐联合迈吉宁新适应症获批,为BRAF V600E突变阳性RAIR-DTC患者带来精准治疗新选择
用于治疗BRAF V600E突变阳性、放射性碘难治或不适用、且血管内皮生长因子酪氨酸激酶抑制剂(VEGFR-TKI)治疗失败的局部晚期或转移性分化型甲状腺癌成人患者。
2026-06-10 18:08
 资讯
资讯 3个项目完成首批生物医学新技术临床研究备案
6月8日,中国生物技术发展中心发布生物医学新技术临床研究备案完成项目清单(第1批),自5月1日《生物医学新技术临床研究和临床转化应用管理条例》正式生效以来,5月1日至5月22...
2026-06-10 17:51
 资讯
资讯 35.7亿元!来凯医药PI3Kα抑制剂达成达成海外BD
来凯医药将授予Vasque Bio LAE118在全球范围内(不含中国大陆、中国香港、中国澳门、中国台湾地区)的独家开发、生产制造及商业化权益,全权负责该药物海外市场的全流程研发与...
2026-06-10 14:28
 资讯
资讯 腾讯、阿里等入股脑机接口企业阶梯医疗,博睿康完成上市辅导
公开资料显示,近日上海阶梯医疗科技有限公司发生工商变更,新增阿里巴巴关联公司杭州灏月企业管理有限公司、腾讯关联公司上海启善投资有限公司等为股东,同时注册资本由100万元...
2026-06-10 10:06
 资讯
资讯 药明康德、诺禾致源等被美国列入“中国军工企业”名单
今日,药明康德发布公告称,公司注意到,2026年6月8日(美国时间),美国国防部错误地将药明康德列入其根据1260H条款认定的“中国军工企业”正式更新版名单中。
2026-06-09 21:24
 资讯
资讯 微眸医疗完成近亿元A轮融资,全国首个眼科手术机器人多中心随机对照注册临床试验同期收官
本轮A轮融资由元航资本领投,老牌投资机构明桂资本持续加码追投,多家行业知名投资机构联合参与投资,伊嘉资本担任本次融资财务战略合作伙伴。
2026-06-09 20:20
 资讯
资讯 礼来公布口服小分子GLP-1 药物关键研究完整数据,潜在T2D新口服方案表现亮眼
礼来公司在美国糖尿病协会(ADA)第86届科学年会上公布了口服小分子GLP-1受体激动剂orforglipron在ACHIEVE系列三项3期临床研究中的详细数据。
2026-06-09 19:57
 资讯
资讯 因美纳发布StrataMap Spatial Solution:高性能的端到端空间全转录组研究解决方案
StrataMap Spatial支持研究人员以真正的单细胞分辨率开展空间生物学研究,拓展科学发现的边界
2026-06-09 19:52
 资讯
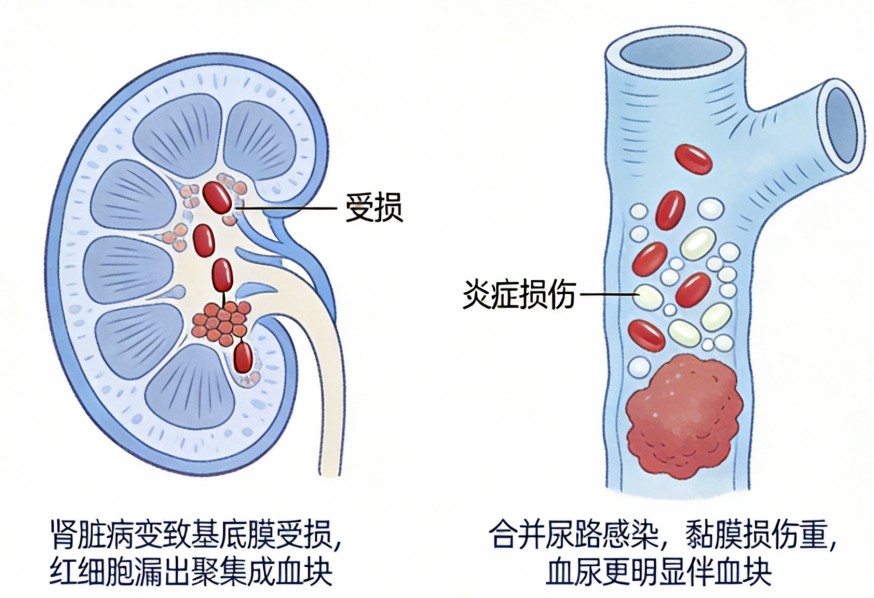
资讯 两款IgA肾病新药获批
6月9日,荣昌生物发布公告称,近日,荣昌生物制药(烟台)股份有限公司收到国家药品监督管理局(NMPA)核准签发的《药品注册证书》,泰它西普注射液(代号:RC18)治疗免疫球蛋...
2026-06-09 11:33
 资讯
资讯 第五年,2026年纠正医药购销领域和医疗服务中不正之风工作要点
《通知》围绕年度重点任务和既往工作中发现的突出问题,聚焦重点领域和关键环节,在坚持党建引领行风、强化医德医风建设、加强正向宣传引导、防范化解风险隐患、严守医疗数据安...
2026-06-09 09:14
 资讯
资讯 华超神控完成亿元天使系列融资,自研 AI 超声脑机平台开辟无创深脑调控新赛道
本轮融资分为天使轮与天使 + 轮两期,天使轮由经纬创投独家领投,天使 + 轮由德联资本、道远资本联合领投,行业知名机构持续加注,循光资本担任本次系列融资独家财务顾问。
2026-06-08 17:05
 资讯
资讯 Cytiva与鼎康生物合作GMP-2扩建项目投产, 共筑“中国速度,全球交付”新标杆
GMP-2生产基地专为临床后期及商业化生产打造,可为全球生物药合作伙伴提供灵活且可扩展的生产解决方案,助力加速产品商业化进程并保障全球稳定供应。
2026-06-08 16:41
 资讯
资讯 默沙东欣瑞来(注射用索特西普)重磅上市,引领肺动脉高压(PAH)迈向“治本” 新里程碑
用于治疗世界卫生组织功能分级(WHO FC)Ⅱ-Ⅲ级的肺动脉高压(PAH,WHO第1组)成年患者
2026-06-08 16:36
 资讯
资讯 GCP2026修订版发布,2020版废止
6月8日,国家药监局、国家卫生健康委、国家中医药局、国家疾控局联合发布《药物临床试验质量管理规范(2026年修订)》,自2026年9月1日起施行。国家药监局、国家卫生健康委《关...
2026-06-08 16:21
 资讯
资讯 博腾股份终止斯洛文尼亚研发生产基地建设,保留对诺华子公司主张索赔的权利
近日,博腾股份公告称,鉴于诺华斯洛文尼亚子公司已向博腾股份全资子公司PSI发出解除通知,PSI在该场地内的投资和建设已面临重大不确定性,公司决定终止投资建设斯洛文尼亚研发...
2026-06-08 13:10
 资讯
资讯 全球首款CD7 CAR-T儿童适应症一期临床启动
据安科生物和博生吉医药消息,安科生物参股公司博生吉医药自主研发的全球首款进入临床阶段的靶向CD7自体CAR-T产品PA3-17儿童适应证临床试验启动会在组长单位中国医学科学院血液...
2026-06-08 10:57



