公元前2500年左右,古埃及医生印和阗在行医笔记中记录了一位患者的症状:乳房上鼓起的肿块,又硬又凉,且密实如河曼果,潜伏在皮肤下蔓延。印和阗是个伟大的医生,他的手稿里对多种病例注明了详细的治疗方法,然而在癌症这一案例里,他只写了短短的一行字:“没有治疗方法”,这也是人类最早关于乳腺癌的记载。
千百年来,癌症一直是人类生命健康的最大威胁。据《2017年中国肿瘤登记年报》统计,我国每年有约1万人确诊为癌症,平均每分钟就有7个人确诊。
免疫疗法为肿瘤治疗带来新的希望,反应率成瓶颈
肿瘤免疫疗法(Immuno-Oncology Therapy,I-O)首次出现于 19世纪末期,经过130多年的漫长探索,终于开始被人们视为最有希望攻克癌症的手段。2014年9月,在日本上市的全球首个PD-1抗体药物纳武利尤单抗,将晚期非小细胞肺癌的五年生存期从不到5%提高到了16%。
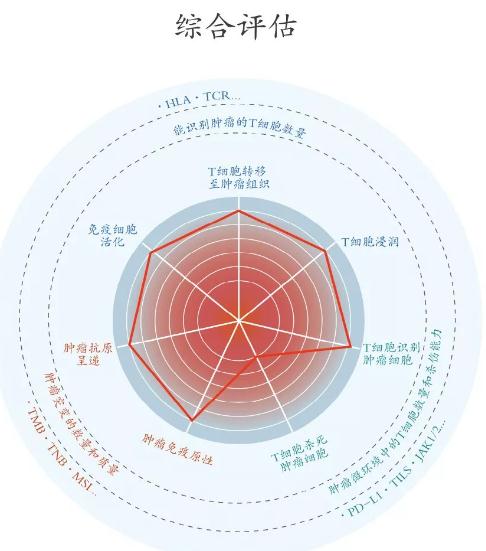
肿瘤免疫治疗是指通过激活机体免疫系统实现对肿瘤细胞的杀伤的一种疗法,其基本思路是解除肿瘤微环境的免疫抑制、提高抗原呈递细胞的抗原呈递功能及促进机体产生T 淋巴细胞等方式激活人体自身的免疫系统,从而达到识别和杀伤癌细胞的目的。
在21世纪的第二个10年,是免疫疗法发展最迅猛的10年,免疫调节剂PD-1、CAR-T细胞治疗等新型肿瘤治疗方案,纷纷完成了从科研成果到临床应用的转化。
自2014年以来,全球共批准上市了9款PD-1/PD-L1药物。据Evaluate Pharma数据显示,2016年全球肿瘤免疫疗法的市场规模达619亿美元,预计到2021年将增长至1200亿美元。
在国内,免疫疗法拥有着同样的爆发力。据米内网数据显示,2018年中国公立医疗机构终端抗肿瘤单抗的市场规模首次突破百亿,增速达到41.36%,为抗肿瘤药9个小类中最快。
2018年至今,随着特瑞普利单抗注射液、信迪利单抗注射液、注射用卡瑞利珠单抗等多个抗肿瘤单抗新品获批上市,另有20余款PD-1抑制剂正在国内开展临床试验。
从研发到临床的肿瘤免疫治疗领域热浪之下,异常激烈的市场竞争已经不可避免。现阶段,扩增适应症和降低价格是肿瘤免疫药厂争夺市场份额的常规手段。
例如,帕博利珠单抗自首次获批用于黑色素瘤治疗以来,已经覆盖了15个癌种的23个以上适应症。再如,目前国内陆续上市的6款PD-1/PD-L1单抗药物,价格呈现明显的下降趋势。
不过,纵然市场端竞争愈演愈烈,免疫疗法在肿瘤治疗中也取得过巨大的成功,各种类型免疫疗法呈现一致的患者响应率底下却是不可回避的事实。
肿瘤免疫疗法作为个性化精准治疗的重要组成部分,基于组学数据筛选最合适的潜在患者以优化临床效果,是提高药物响应率的主流思路。FDA将用于免疫治疗有效性判断的诊断方法分为"伴随诊断"和"补充诊断"两种。
伴随诊断对于接受相应药物治疗是必须进行的检测,能够为治疗用品的安全性和有效性提供必要信息。
伴随诊断的优点在于可基于预先设定的cut-off值将患者严格分为两部分,即生物标志物阳性和阴性患者,生物标志物阳性患者才能用药,以保证患者在安全用药的基础上获得最大的临床获益机会。
补充诊断对于接受相应药物治疗不是必须的检测,但可以提供个体治疗相关的信息,辅助医生或者患者做决策。
免疫疗法在临床实践中逐渐普及开来后,肿瘤精准免疫伴随诊断成为了肿瘤相关基因检测新的兵家必争之地。目前,FDA已经批准了PD-L1表达阳性、MSI-H等指标指导PD-1/PD-L1抑制剂的临床用药。
找到并合理设置肿瘤免疫诊断生物标志物(Biomarker),是肿瘤精准免疫诊断的关键。现阶段,基因检测服务商主要围绕PD-L1表达水平(TPS/CPS)、MMR/MSI检测、TMB等热门生物标志物提供检测产品,他们会根据适应症、标本类型、临床证据等不同而构建不同的测序组合。
主流生物标志物产品纷纷走向合规化
PD-L1表达
PD-L1表达是目前预测多种实体瘤患者是否适合使用PD-1/PD-L1抑制剂的三大预测指标之一,临床主要检测方法是免疫组化(IHC)。PD-L1表达越高,表明肿瘤越有可能是通过PD-1/PD-L1信号通路而非其它信号通路发生免疫逃逸。
早期研究显示:随着PD-L1表达升高,PD-1/PD-L1抑制剂疗效增加,疾病控制时间延长,并且患者预后改善。
2017年5月,罗氏研发的肿瘤学试剂盒VENTANA PD-L1(SP263)获得FDA批准上市。这个试剂盒首先用于阿斯利康的德瓦鲁单抗治疗局部晚期或转移性尿路上皮癌患者,功能是提供患者肿瘤程序性死亡配体-1(PD-L1)表达状态的相关信息。
一年后,安捷伦科技Dako PD-L1 IHC 22C3 pharmDx试剂盒获得FDA批准上市,作为用于治疗宫颈癌的帕博利珠单抗伴随诊断试剂。
目前,PD-L1免疫组化检测试剂有五种:22C3、28-8、SP263、SP142和73-10。五种免疫组化检测抗体分别在两个免疫组化平台DAKO和Ventana进行检测。
蓝印计划结果显示,22C3、28-8、SP263检测肿瘤细胞具有染色一致性,SP142检出阳性细胞较少,因此22C3抗体在评估其他免疫用药上面具有通用性。
国际肺癌研究协会对多款PD-L1检测试剂盒进行对比发现,DAKO 22C3检测试剂盒在检出率、准确率和整体可靠性方面均优于其他产品。
不过,PD-L1表达纵有千般好,也并非预测免疫疗效真正可靠的指标。临床证据在为PD-L1表达背书的同时,也提供了相反的证据。上也有不同癌种的患者PD-L1不表达但使用免疫检查点抑制剂仍然有效的情况。
例如,在肾癌中,PD-L1表达不具有预测作用。此外,PD-L1表达的预测作用与患者的吸烟史也有一定关系。
PD-L1表达预测作用好坏因PD-L1表达机制、检测方法、阈值确定及评估标准等而有所差异。
MMR及MSI
MMR(Mismatch-repair),即错配修复,是 DNA 复制后的一种修复机制,可以维持 DNA 复制的准确度,控制基因变异;MSI(Microsatellite Instability),即微卫星不稳定性,指与正常组织相比,在肿瘤中某一微卫星由于重复单位的插入或缺失而造成的微卫星长度的任何改变,出现新的微卫星等位基因现象。代表肿瘤基因组突变水平,间接反映肿瘤免疫原性。
2015 年,《新英格兰医学杂志》发表了一项由约翰霍普金斯大学 Luis Diaz 博士和 Bert Vogelstein 博士团队领导的研究。研究证明,免疫检查点抑制剂对结直肠癌患者的一个亚型有疗效。
在这项研究中,研究者招募了 41 位 dMMR(错配修复缺失)和pMMR(无错配修复缺失)的结直肠癌患者,以及一些 dMMR 的其它癌种患者,并对患者进行每两周一次帕博利珠单抗治疗。
结果显示,与 pMMR 结直肠癌患者相比,dMMR 患者的无进展生存期(PFS)和总生存期(OS)相对较长,对治疗的响应率较高。
2017年5月,FDA加速批准了PD-1抑制剂帕博利珠单抗(pembrolizumab,Keytruda)用于治疗携带微卫星不稳定性高(MSI-H)分子特征,且不可切除或转移性实体瘤的成人和儿童癌症患者——FDA批准的首款不依照肿瘤来源,而是依照生物标志物进行区分的抗肿瘤疗法。
同年8月1日,FDA又加速批准了纳武利尤单抗用于MSI-H或dMMR的结直肠癌患者中。从这两个例子也可以清楚的看到MMR及MSI在肿瘤预测中的关键作用。
不过,MSI-H在不同癌种中的分布差异较大,子宫内膜癌、消化道癌中可达到25%左右,而在肺癌和其他癌种中甚至不足5%。
且基于10万肿瘤患者数据分析,绝大多数MSI-H(83%)的患者,都落在了TMB-H的区域,就是存在很多微卫星稳定的患者,使用免疫药物疗效也很好,所以单一使用这个biomarker会漏掉很多合适用药的人群。
TMB
肿瘤突变负荷(TMB)是指,每百万碱基中被检测出的基因突变个数。在不同的癌症中体细胞突变数量从0.01突变/Mb~超过400突变/Mb不等,这些突变中有些会转录表达多肽抗原表位或肿瘤新生抗原。
理论上,携带基因突变越多的癌症患者,癌细胞产生的新生抗原越多,就与正常细胞越不一样,被免疫细胞识别的可能性更高,更有可能从中获益。
2014年,科学家分析了CTLA-4抗体治疗患者的全外显子测序(WES)数据,发现了TMB与治疗效果之间的关系,这是TMB首次被应用于免疫治疗中。
2015年,科学家再次通过WES分析了PD-1抗体治疗的肺癌患者,发现高TMB与临床效果呈正相关,其结果发表于顶级杂志《科学》上。
2016年,回顾分析CheckMate026临床试验的WES数据,发现高TMB患者,接受PD-1抑制剂治疗后,临床获益显着优于化疗。由此,TMB开始引发引全世界关注。
而TMB真正开始走红,是在多基因(Panel)测序出现之后。早期TMB研究采用WES测序方法,成本高昂,于是人们尝试Panel测序替代WES测序。
2018年,Panel检测TMB的前瞻性研究数据出炉,CheckMate227与CheckMate568同时证明TMB≥10muts/Mb的晚期非小细胞肺癌患者接受免疫疗法效果更佳。
随后,欧洲临床肿瘤学会(ESMO)和美国国立综合癌症网络(NCCN)分别基于CheckMate227和CheckMate568的数据,在其指南中纳入了TMB作为可能的生物标志物,由此引发基因公司开发Panel检测产品的热潮,其中不乏国内基因检测公司的身影。
不过,一路高歌猛进的TMB最近遭遇了折戟风波。
首先是BMS(百时美施贵宝)的纳武利尤单抗联合伊匹单抗(Yervoy)在生存结果上与TMB无关。近年来,BMS积极探索包括 PD-L1,TMB,MSI 和 TIL 等分子标记物。
然而,在2019年3月,新的临床试验数据显示,肿瘤TMB水平高或低的患者的生存结果没有差异,BMS与FDA讨论后已撤回了其补充生物制品许可申请。
几乎同时,在生物标志物临床应用上驾轻就熟的默沙东将TMB作为生物标志物加入多个临床研究中后,也遭遇了挫败。此外,10月初刚刚结束的2019ESMO中,来自美国的Corey Jay Langer教授宣告了在Keynote-021中,TMB在帕博利珠单抗联合化疗的患者中与生存结果无关联。
实际上,TMB是一个研究中的指标,尚无相应的行业标准和共识出台,Panel设计、算法、评判TMB高低的cut-off值都缺乏标准,不同临床试验采取不同检测机构提供的TMB检测结果不具有可比性,临床应用必须基于临床性能验证和前瞻性研究结果数据。
冷门生物标志物或推动免疫伴随诊断走向精准
围绕单一生物标志物做测序研究并试图预测免疫治疗效果,是主流生物标志物产品普遍采用的设计思路。诚然,经过持续迭代的单一生物标志物测序产品能够在一定程度上区分获益人群,但是无论是使用哪个生物标志物都存在较高假阳性率和假阴性率的缺陷。
换言之,现有免疫治疗预测方式存在挑选出的高水平患者对免疫治疗不响应,而有些低水平的患者反而对免疫治疗有响应的困境。
因此,已经有研究人员陆续把焦点集中在采用多个生物标记物对患者进行分层。
研究人员发现,人类白细胞抗原杂合性丢失(HLA-LOH)、肿瘤新生抗原负荷(TNB)等此前关注较少的指标可以作为前述主流指标的辅助,进一步提高疗效预测的特异性,动脉网就这类冷门生物标记物的预测原理采访了相关业内人士。
实际上,TNB的肿瘤免疫响应预测原理与TMB具有相似性,但存在本质差异。在肿瘤微环境中,基因突变经过转录、翻译,最终以肽段的形式被MHC呈递到细胞表面,T 细胞通过识别肿瘤特异的肽段来辨别肿瘤。这些特异的肽段也被称为肿瘤新生抗原,肿瘤突变越多,产生新生抗原的概率越大,越可能引发T细胞的免疫反应。
“目前,利用TMB对肿瘤突变进行了量化,与之对应的新生抗原的量化指标为TNB,即肿瘤基因组编码区中平均每百万碱基区域中检测到的新生抗原数量。”相关业内人士向动脉网解释道,“所以可以说TMB是间接反映肿瘤的免疫原性,而TNB是直接反映肿瘤的免疫原性。”
不过,从基因突变到产生新生抗原设计一系列复杂步骤。“肿瘤突变负荷高(TMB-H)不一定会表现出肿瘤新生抗原负荷高(TNB-H)。”该相关人士强调。真实世界研究数据显示,临床上存在TMB-H,但TNB-L的患者,这部分患者该概率不会对免疫药物响应。因此,所以使用TMB+TNB双元模型进行评估可以提高预测的准确性。
有趣的是,另一个生物标志物HLA预测免疫治疗响应率与特定患者的TNB状况也存在相关性。HLA是存在于抗原呈递细胞表面负责抗原呈递的蛋白分子,其等位基因数量异常庞大,目前发现的已达17331个,每种HLA等位基因可表现出对同一新生抗原不同的亲和呈递能力。
如果其杂合性缺失将导致HLA识别新生抗原介导的免疫监视功能削弱,以致携带突变的肿瘤克隆易于免疫逃逸,表现出高TMB的情况。
HLA作为生物标记物预测免疫响应率的准确率也于肿瘤微环境下其他生物标记物水平强相关。
在2019年9月结束的ASCO会议上,有研究人员汇报HLA I类基因 LOH是TMB-H的中国癌症患者对PD-1/PD-L1产生耐药的一个潜在因素。所以只进行患者胚系HLA分型,会遗漏肿瘤细胞HLA的实际情况,无法准确指导免疫用药。检测TMB的同时再检测肿瘤细胞的HLA LOH,可以更加有效地筛选免疫用药有效人群。
小结
免疫疗法是近几年肿瘤治疗研究领域的热点,其中PD-1/PD-L1检查点抑制剂在癌症治疗中取得了令人瞩目的成果。为了使更多接受PD-1/PD-L1抑制剂治疗的患者获益,寻找有效的预测性生物标志物刻不容缓。
从目前结果来看,似乎很难有一个单一的指标来预测免疫治疗的疗效。实际上,无论是主流的PD-L1、MMR、TMB还是现阶段关注度较低的HLA、TNB,其免疫响应预测原理都存在相关性,提高免疫响应预测准确性,整合不同生物标记物,设计合理的大Panel检测产品似乎是必由之路。
在未来的研究中,通过多维度的检测结果(包括但不限于基因测序、免疫组化、蛋白质组等数据),基于人群用药疗效数据,构建恰当的预测模型,综合评估药物靶点基因、TMB、TNB、HLA 分型及杂合缺失、免疫通路基因、免疫耐药基因、免疫治疗超进展相关基因等指标,可能是预测免疫治疗疗效的关键。
期待这一天,在全球相关领域工作者的共同努力下,可以早点到来。让肿瘤免疫治疗给全人类带来更多福祉。
来源:动脉网 作者:王世薇
为你推荐
 资讯
资讯 药品试验数据保护9问?为什么中药不适用于数据保护制度? 国家药监局发布 《药品试验数据保护实施办法》
数据保护是指,符合条件的化学药品和生物制品获批上市时,国家药监局对申请人提交的自行取得且未披露的试验数据和其他数据实施保护,给予最长不超过6年的数据保护期。数据保护期...
2026-05-15 18:16
 资讯
资讯 博腾股份首个欧洲基地遭诺华单方面节约
5月13日,博腾股份(300363 SZ)发布《关于对外投资进展及重大风险提示的公告》,根据公告,其位于斯洛文尼亚的研发生产基地遭到诺华公司(Novartis)的单方面解约,诺华单方要...
2026-05-15 14:43
 资讯
资讯 甘李药业先后两款胰岛素产品在欧盟获批
5月14日晚间,甘李药业发布公告称,甘李药业股份有限公司及其欧洲全资子公司甘李药业欧洲有限责任公司(Gan&LeePharmaceuticalsEurope GmbH)于近日收到欧盟委员会(EuropeanCo...
2026-05-15 12:00
 资讯
资讯 2026年度国家医保基金飞行检查正式全面启动
5月14日,国家医保基金飞行检查湖南现场启动会暨警示教育会在长沙召开,这标志着2026年度国家医保基金飞行检查正式全面启动。国家医保局党组成员、副局长黄华波出席会议并讲话。
2026-05-15 08:29
 资讯
资讯 泰格医药实控人被立案,还拖累了哪些上市公司
5月12日晚间,国内CRO龙头企业泰格医药(300347 SZ;3347 HK)发布公告称,公司实际控制人叶小平、曹晓春收到中国证监会《立案告知书》,二人因涉嫌持股变动相关信息披露违法...
2026-05-14 18:11
 资讯
资讯 诺贝尔化学奖获得者创办的AI制药公司 Isomorphic Labs 完成21亿美元B轮融资
据国外媒体消息,由谷歌DeepMind孵化、AI制药企业Isomorphic Labs完成21亿美元(约合人民币142 5亿元)B轮融资。
2026-05-14 13:29
 资讯
资讯 CDE:2025年度药品审评报告
2025 年受理 16130 件技术审评类药品注册申请,以药品类型统计,中药注册申请 2723 件,化学药品注册申请10587 件,生物制品注册申请 2820 件。
2026-05-14 11:54
 资讯
资讯 欧洲肥胖大会:诺和诺德Wegovy在所有绝经阶段的女性中均实现了显著减重
丹麦当地时间5月12日,诺和诺德公布数据显示,Wegovy(诺和盈)在女性肥胖症患者不同生育生命阶段中均达成了显著且一致的减重效果,涵盖绝经前阶段、绝经期和绝经后阶段[1]。绝...
2026-05-13 12:59
 资讯
资讯 伊米诺康完成 2.5 亿元 A 轮融资 加速打造全球领先全人源抗体发现平台
本轮融资由维梧资本领投,高脉元航跟投,老股东熙诚金睿、泰煜投资大比例超额追加投资,资金将重点用于核心技术迭代、平台商业化落地与创新能力升级。
2026-05-13 09:58
 资讯
资讯 减重之后怎么办?礼来ECO最新数据将行业视线推向“长期维持”
2026年5月13日,礼来公布SURMOUNT-MAINTAIN和ATTAIN-MAINTAIN两项后期临床研究详细结果。
2026-05-13 09:53
 资讯
资讯 147亿,A股医药板块有史以来最大的年度亏损
147亿,A股医药板块有史以来最大的年度亏损。近日,A股疫苗明星企业智飞生物(300122 SZ)发布的2025年年报公布了这一“成绩”。这也是智飞生物上市以来首个亏损。
2026-05-12 20:21
 资讯
资讯 恒瑞医药与BMS达成总交易额可达约152亿美元的战略与许可合作
本次合作协议共包含 4 项恒瑞肿瘤学及血液学项目、4 项 BMS 免疫学项目,以及双方依托恒瑞研发引擎与多元创新技术平台共同研发的 5 项创新项目,值得注意的是,这13在研...
2026-05-12 13:40
 资讯
资讯 徐和平教授荣膺国际视觉与眼科研究协会(ARVO)金质会士(FARVO Gold)荣誉称号
近日,国际视觉与眼科研究协会(The Association for Research in Vision and Ophthalmology, ARVO)在美国丹佛召开的2026年年会上正式公布了本年度金质会士(ARVO Gold Fellow,FARVO)评选结果。
2026-05-12 13:35
 资讯
资讯 中国生物技术发展中心:细胞组分及衍生物治疗新技术临床研究备案指引(第1版)
本指引适用于在我国境内开展的非以药品注册为目的的细胞组分及衍生物治疗新技术临床研究,本指引所指的细胞组分及衍生物治疗新技术不依赖完整活细胞,是指利用人自体或异体干细...
2026-05-12 10:05
 资讯
资讯 迈瑞遭证监会监管六问
5月8日,中国证监会对外公布最新一期《境外发行上市备案补充材料要求》(2026年4月27日—2026年5月8日),国际司共对7家企业出具补充材料要求,其中包括已于2025年11月10日向港交...
2026-05-10 19:21
 资讯
资讯 复星医药至多10.15亿元取得两款FAK抑制剂中国大陆区域独家商业化权利
5月8日,应世生物宣布与复星医药达成战略合作。根据协议约定,应世生物将授予复星医药其自主开发的两款创新 FAK 抑制剂IN10018(Ifebemtinib)、IN10028在中国(不含港澳台地...
2026-05-09 16:14