5月4日,华东医药(000963.SZ)发布公告,公司美国合作方ImmunoGen对外宣布用于治疗卵巢癌的全球首创(first-in-class)ADC药物ELAHERE 在Ⅲ期临床MIRASOL试验中获得了积极的关键数据(top-line data),于FRα阳性铂类药卵巢癌患者中证明了总体生存获益。ImmunoGen计划于2023年下半年在美国提交补充生物制品许可申请 (sBLA),以将ELAHERE的加速批准转为完全批准,并在欧洲提交上市许可申请 (MAA)。
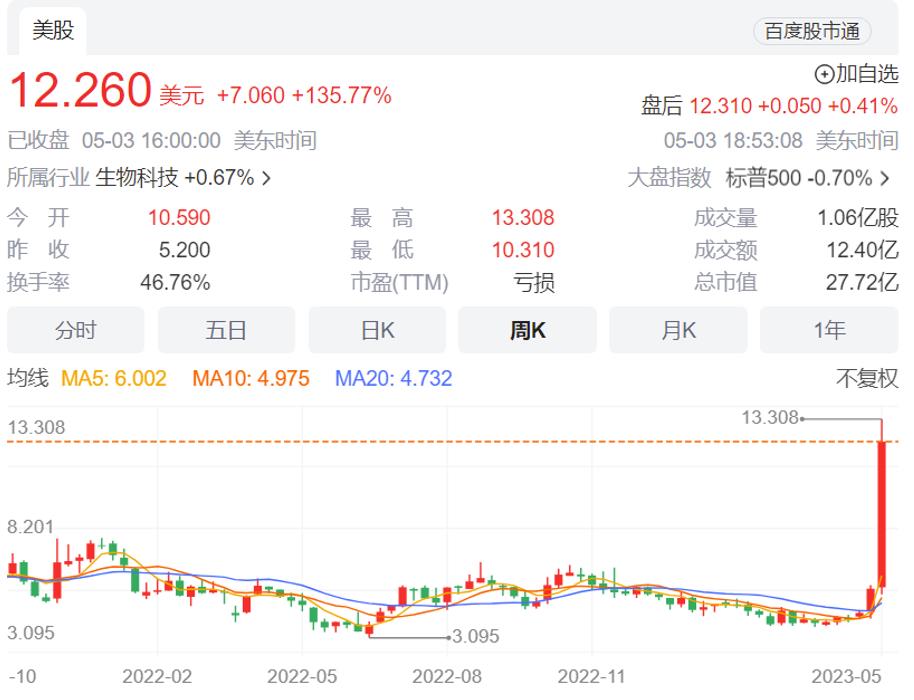
受此消息影响,ImmunoGen股价当天大涨136%,市值达到27.7亿美元。
图:ImmunoGen 股价走势图
全球首个卵巢癌ADC 预计今年国内申报上市
ELAHERE 为华东医药与ImmunoGen合作开发的全球首个针对叶酸受体α(FRα)阳性卵巢癌的ADC药物。
此次公布的MIRASOL 试验一共招募了 453 名患者,最终数据结果显示:ELAHERE 治疗组相比于IC化疗组,中位OS从12.75个月延长到16.46个月,死亡风险降低33%;中位PFS从3.98个月延长到5.62个月,疾病进展或死亡风险降低35%。ELAHERE组中研究者评估的ORR为 42.3%,包括12个完全缓解(CR),而 IC化疗组为15.9%,无CR。安全性方面,与IC化疗相比,ELAHERE不良事件发生率更低,没有发现新的不良安全信号。
ImmunoGen 表示随着MIRASOL获得成功,ELAHERE 有潜力成为治疗FRα阳性的卵巢癌新标准。
卵巢癌被认为妇科恶性肿瘤中最为凶险的癌种,据统计,全球卵巢癌的年新发病例数约31万,每年死亡病例数约21万。由于卵巢癌早期症状隐匿且非特异,约80%的患者确诊时已为晚期,5年生存率仅有40%。根据《Global Cancer Burden in 2020》,2022年国内卵巢癌发病人数达5.76万人,浙商证券研究所预计到2025年,国内卵巢癌发病人数将达6.11万人。
图:国内卵巢癌发病及治疗人数(《Global Cancer Burden in 2020》,浙商证券研究所)
然而,全球铂耐药复发性卵巢癌(PROC)的治疗选择十分有限,传统非铂类化疗、抗血管生成药物和 PARP 抑制剂均无法满足铂耐药患者的治疗需求。当下各类非铂单药有效率仅4%-13%左右;非铂化疗联合贝伐珠单抗的中位OS不足1年半,治疗需求仍未满足;由于存在增加铂耐药患者死亡风险的可能,2022年多家PARP抑制剂接连撤回PROC后线治疗适应症。
ELAHERE 是目前唯一获得III期临床数据的FRα ADC药物,通过特异性识别肿瘤细胞表面的靶标蛋白,释放药物分子,进而实现对肿瘤细胞的精确打击,开创了卵巢癌治疗新途径。
因此,ELAHERE 在去年11月获FDA加速批准上市后,销售额迅速放量,2023年一季度销售额达2950万美元,进一步填补了临床治疗的空白。随后被2023年最新版NCCN指南首选推荐用于单药或联合治疗FRα阳性PROC。
华东医药拥有 ELAHERE 在大中华区(含中国大陆,香港、澳门和台湾地区)的独家临床开发及商业化权益,并计划于2023下半年向NMPA提交ELAHERE上市申请,有望为更多国内PROC患者带来福音。
此外,ELAHERE 在国内的其他临床试验也在积极开展。2022年7月,ELAHERE 在中国的I期临床试验PK药代研究已完成全部受试者入组。2022年12月,该产品完成中国Ⅲ期单臂临床试验全部受试者入组。
华东医药表示,后续公司及合作方将通过进一步临床研究,用于铂敏感人群,以及前线人群的治疗,并将ELAHERE作为卵巢癌的首选联合用药。
前瞻性差异化创新 全球研发生态圈再获重要里程碑
华东医药于2020年10月从ImmunoGen引入ELAHERE,交易总金额超过3亿美元,其中包括4000万美元的首付款和2.65亿美元的潜在里程碑付款。ELAHERE 也成为国内首个靶向FRα的在研ADC药物,临床竞争格局良好,研发进度也远超同类产品。
此次ELAHERE 3期临床试验大获成功,对其在中国获批上市构成积极影响,充分体现了华东医药独到的眼光,在国内ADC赛道靶点扎堆“内卷” 的环境下,着眼于临床治疗需求,前瞻性引入ELAHERE,实现了差异化创新布局。
近年来,华东医药在ADC领域持续加大差异化纵深布局,并且与ADC领域全球新兴的科技公司Heidelberg Pharma开展股权投资及产品合作,成为其第二大股东,同时引入多款ADC创新产品,进一步提升了在ADC领域全球一流的研发技术和临床注册能力。其中HDP-101 为针对多发性骨髓瘤 BCMA 靶点的 ADC 药物,正在开展海外 I/II 期临床; HDP-103 为针对前列腺癌 PSMA 靶点的 ADC 药物,正在临床前研究阶段。
目前华东医药的创新研发生态圈已形成体系并开始持续产生新管线项目。公司于去年成立独立的 ADC 研发中心,目标是逐步打造差异化的 ADC 自主研发平台,做强做优 ADC 领域生态链,2022-2024 年立项开发不少于 10 款 ADC 创新产品并积极推动注册临床研究。
截至2023年一季报披露,公司已自主立项 6 个临床前或探索性的全新靶点 ADC 项目。预计在 2025 年前将获得额外至少 4 个自研 PCC 的确认和 2 个自研 ADC 项目 IND 获批。目前首个原创 ADC 项目已完成PCC 确认,正进行 IND 开发并计划于 2024 年内申报临床。公司将继续加大 ADC 抗肿瘤领域布局,基于尚未满足的临床需求,不断研发针对不同癌种的差异性、迭代性 ADC 产品。
随着华东医药的创新研发持续推进,七款创新产品将有望在未来两年陆续获批上市,从而进一步丰富扩充商业化产品管线。
肿瘤领域,公司first-in-class产品HDM2002(ELAHERE)是与ImmunoGen合作开发的全球首个针对叶酸受体α阳性卵巢癌ADC药物,该产品已于2022年11月获得美国FDA加速批准上市。华东医药已于2023年3月完成中国Pre-BLA递交,计划今年内提交BLA申请。公司在研的迈华替尼片,用于治疗晚期EGFR敏感突变非小细胞肺癌,2021年6月已完成III期临床末例受试者入组,目前正在进行PFS事件数随访,预计2023年第二季度获得III期研究PFS事件数后开展上市申报工作。
与此同时,今年年初华东医药迅速切入CAR-T细胞疗法赛道,宣布与科济药业就其BCMA CAR-T细胞产品泽沃基奥仑赛注射液达成在中国大陆地区的商业化合作。泽沃基奥仑赛注射液上市许可申请于2022年10月获国家药品监督管理局受理,并被纳入优先审评审批程序,目前国内尚无同类产品上市,非常有希望于年内获批上市。
在自身免疫领域,华东医将在2023年正式向NMPA递交ARCALYST BLA申请,这是美国FDA批准的唯一一款适用于12岁及以上人群的治疗复发性心包炎药物,在国内被列入临床急需境外新药目录。公司与参股企业荃信生物合作开发的乌司奴单抗生物类似药HDM3001也计划于2023年第三季度递交BLA申请。
在内分泌领域,华东医药GLP-1抑制剂利鲁平已于今年3月获NMPA批准上市,适用于成人2型糖尿病,成为首款获批上市的国产利拉鲁肽注射液。公司利拉鲁肽注射液减重适应症的上市许可申请也已于2022年7月获得受理,有望于2023年内获批,申报审批进度同样为国内最快。公司以 GLP-1 靶点为核心,打造了全球领先的肥胖、糖尿病和糖尿病并发症创新药物研发平台。目前,公司已建立了涵盖口服、注射剂等多种剂型的长效和多靶点全球创新药和生物类似药相结合的 GLP-1 及相关靶点产品管线,包括4个临床项目和2个IND开发项目,其中部分药物具有Best in Class潜力。
公司与美国MediBeacon, Inc.联合开发的肾小球滤过率动态监测系统和MB-102注射液这一药械组合,目前处于审评阶段。与该系统配合使用的MB-102注射液为全球创新药,已于2023年4月完成中国pre-NDA递交。
此次ELAHERE 3期临床试验大获成功,足以证明华东医药对于创新管线的认知深度和战略眼光,是华东医药针对尚未满足的临床需求,借助ADC领域全球一流的自主研发产业平台,持续推进创新研发的重要进展。未来,华东医药将持续加强华东医药研发创新,围绕新一代的核酸药物、细胞和基因治疗药物等进行布局, 壮大研发生态圈技术平台, 不断丰富差异化、引领性创新医药产品管线。华东医药将加大肿瘤领域ADC药物的布局,不断满足患者需求,带来更多具有国际领先水平的创新药物。
为你推荐
 资讯
资讯 药品附条件批准上市申请审评审批工作程序
附条件批准时,每个附条件批准的适应症单独设置药品注册证书有效期,原则上,在确证性研究完成时限的基础上增加一年。确证性研究完成时限由药审中心在审评中与申请人沟通交流后...
2026-04-26 10:58
 资讯
资讯 CDE:抗体偶联药物首次申报临床试验药学资料撰写指导原则
本指导原则基于 ICH M4Q( R1)总体框架, 格式体例与之保持一致, 在其框架下结合抗体偶联药物的药学研究特点,细化了 IND 申报药学资料的撰写要求,旨在为该类药物 IN...
2026-04-25 21:39
 资讯
资讯 蚂蚁健康向医院开放“智慧医疗AI一体化方案” 支持智能体、云陪诊、本地化模型部署
4月25日,在2026中国医院信息网络大会(CHIMA 2026)上,蚂蚁健康面向全国医院及医疗机构推出“智慧医疗AI一体化方案”。
2026-04-25 20:09
 资讯
资讯 美敦力 5.5 亿美元收购 Scientia Vascular,加码神经血管赛道布局
Scientia Vascular 是专注于神经血管创新器械研发的新兴企业,核心产品管线聚焦颅内血管病变介入治疗领域
2026-04-25 15:50
 资讯
资讯 聚焦预防接种全龄升级,多方合力开展“成人全周期免疫促进暨带状疱疹公益科普”
4月25日,国家疾病预防控制局在上海举办主题宣传活动,呼吁“预防接种,苗助健康,全民行动”。
2026-04-25 15:41
 资讯
资讯 超亿元 A 轮融资!奥明星程以 AI4S 定义下一代生物智能基础设施
由深创投与复星医药(复健资本)联合领投,太平股权、广东中医药大健康基金、杭实集团等多家头部投资机构、产业链龙头企业及多地国资跟投。
2026-04-24 18:28
 资讯
资讯 Cytiva ÄKTA与Biacore系列产品实现本地生产, 以“桐庐样本”赋能生物医药“加速度”
依托桐庐生产基地,Cytiva持续提升本土供应能力,以更短的交付周期与定制化支持,精准匹配中国研发节奏,深度践行“在中国,为中国”承诺
2026-04-24 18:13
 资讯
资讯 全球首个治疗遗传性耳聋基因疗法获批
4 月 23 日,再生元宣布,美国 FDA 已经加速批准其在研基因疗法Otarmeni(lunsotogene parvec-cwha)上市,该药品成为首个也是目前唯一获批用于治疗遗传性听力损失的基因疗法。
2026-04-24 18:01
 资讯
资讯 CDE:治疗用重组蛋白药物首次申报临床试验药学资料撰写指导原则
本指导原则基于 ICH M4Q( R1)总体框架, 格式体例与之保持一致, 在其框架下结合治疗用重组蛋白药物的药学研究特点,细化了 IND 申报药学资料的撰写要求,旨在为该类药...
2026-04-24 12:44
 资讯
资讯 甘李药业GLP-1R博凡格鲁肽Ⅲ期临床试验完成首例受试者给药
4月23日,甘李药业发布公告,博凡格鲁肽(研发代号:GZR18)注射液正在中国开展的适应症成人肥胖患者的中度至重度阻塞性睡眠呼吸暂停(OSA)的Ⅲ期临床试验,于近日成功完成首例...
2026-04-24 10:25
 资讯
资讯 应世生物再冲港交所 IPO:手握国内唯一 III 期 FAK 抑制剂,专攻肿瘤耐药后市场
公司战略性聚焦黏着斑激酶(FAK)及整合素通路,这些靶点对肿瘤细胞的顽强生存能力至关重要。
2026-04-23 22:00
 资讯
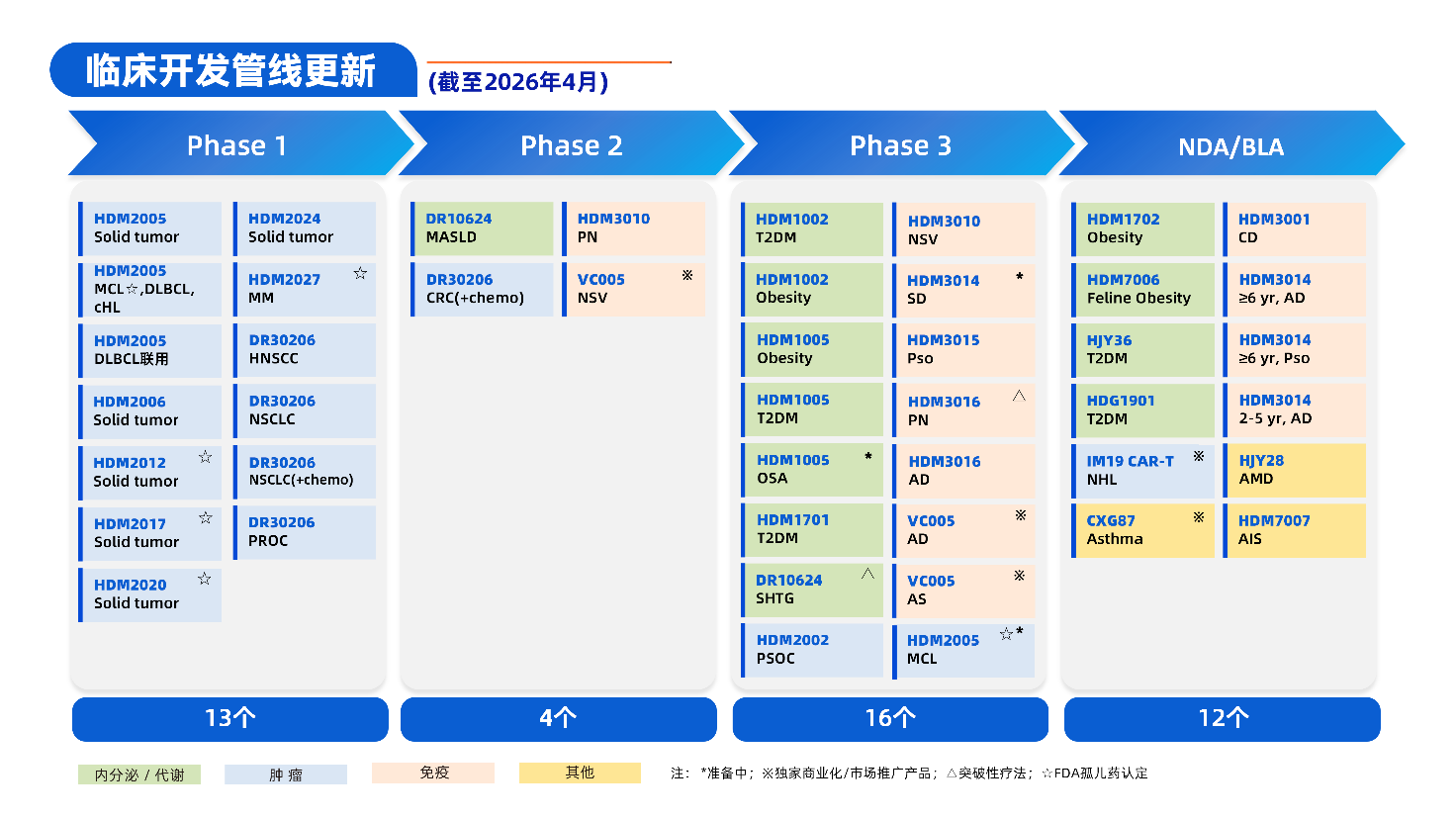
资讯 华东医药2025年创新收入大增64.2%,2026Q1扣非净利创单季历史新高
2026年4月23日晚间,华东医药(000963 SZ)发布2025年年度报告及2026年第一季度业绩。
2026-04-23 21:45
 资讯
资讯 默克与谷歌云达成一项10亿美元的AI合作
此次合作,默克期望将自身在药物研发、科学管理、市场运营等方面能力与人工智能、云平台相结合,帮助默克全球约7 5万名员工提升生产力。
2026-04-23 13:00
 资讯
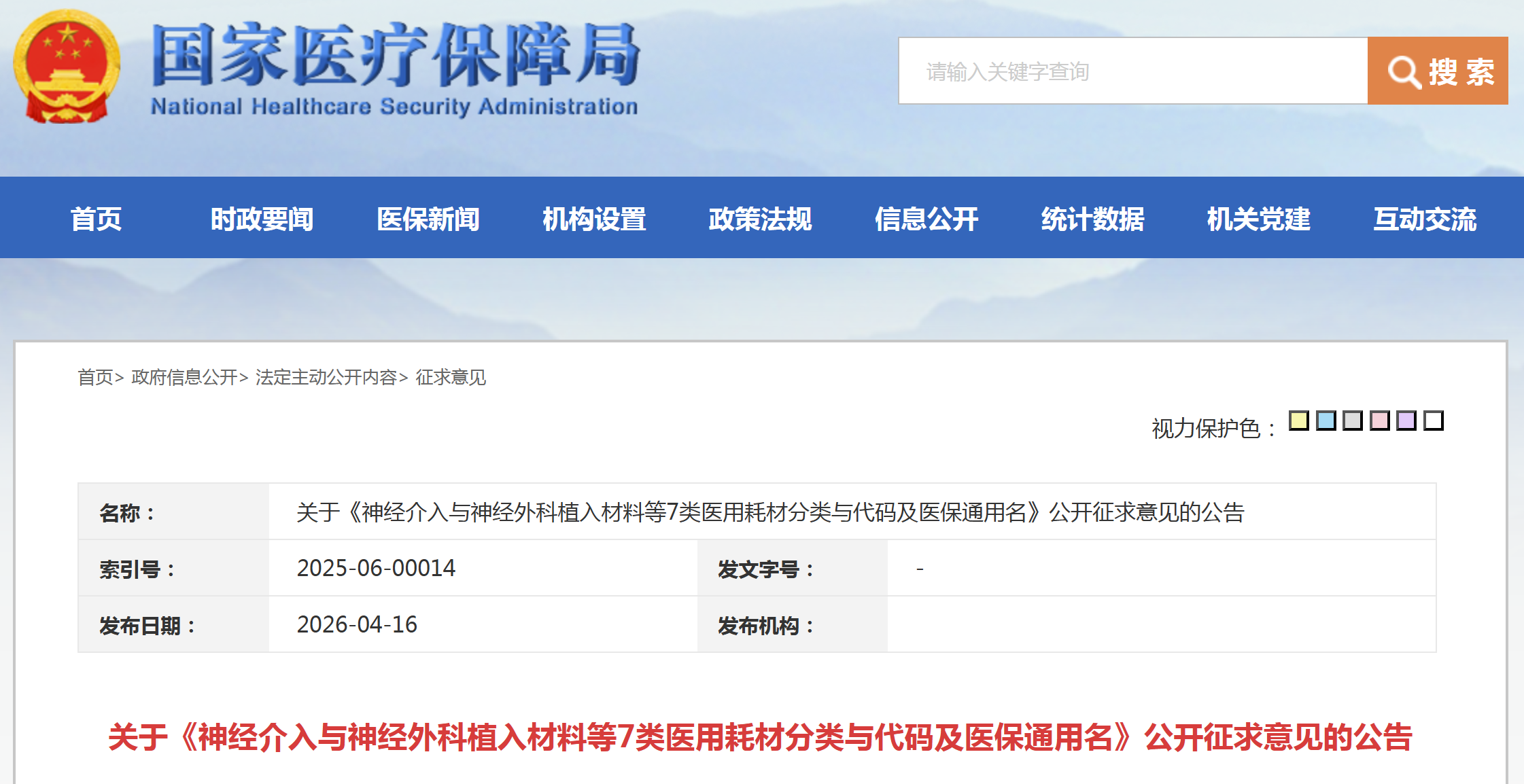
资讯 神经介入与神经外科植入材料等7类医用耗材分类与代码及医保通用名
近日,国家医保局发布《神经介入与神经外科植入材料等7类医用耗材分类与代码及医保通用名》公开征求意见的公告。
2026-04-23 11:29
 资讯
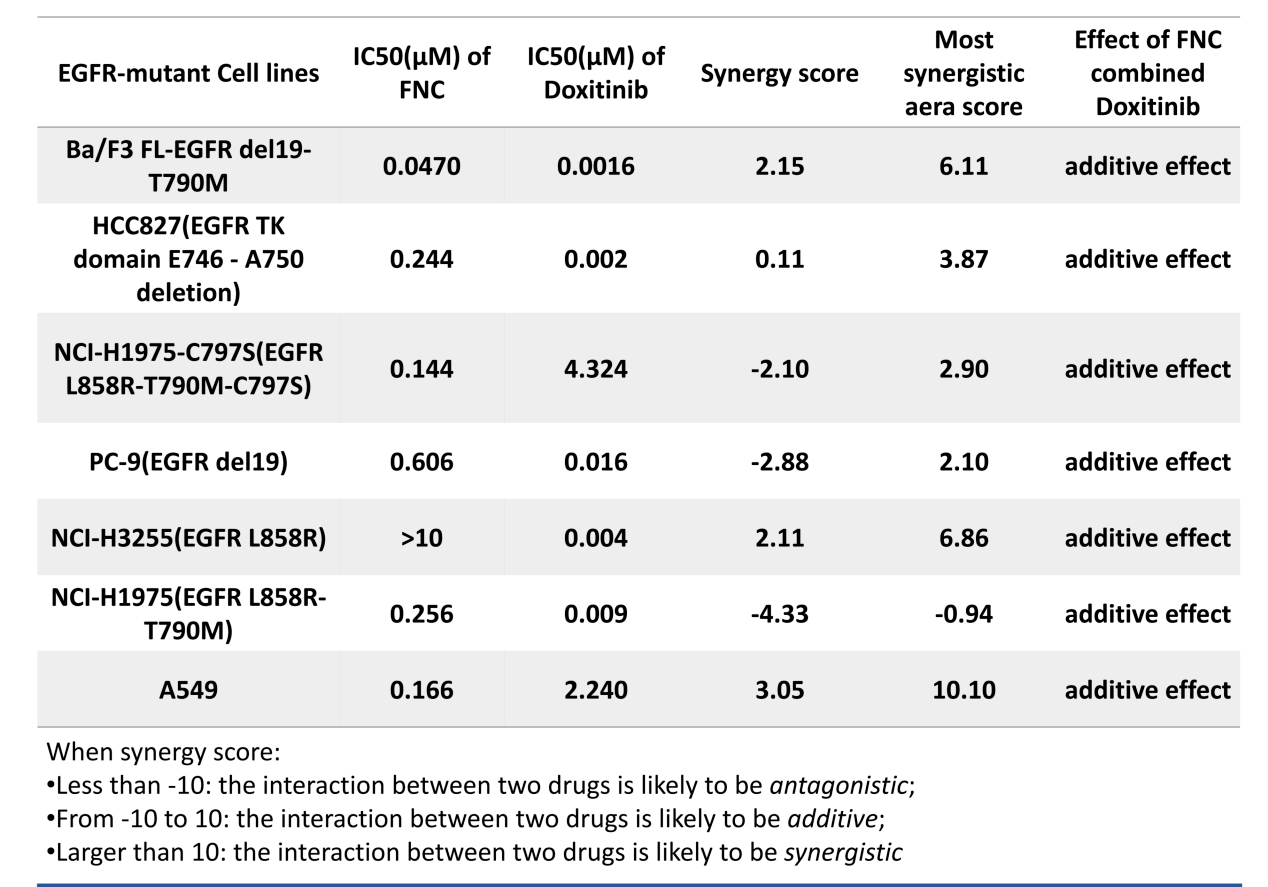
资讯 真实生物阿兹夫定与哆希替尼联合疗法最新消息
近日,真实生物在美国癌症研究协会(AACR 2026)年会以壁报形式展示了阿兹夫定与哆希替尼联合疗法的临床前研究成果,标题为标题:Azvudine Combined with Doxitinib,a Potential Therapy for EGFRm+ NSCLC。
2026-04-23 11:07