昨日,贵州百灵对外发布关于签订《技术转让合同》的公告,根据公告,贵州百灵于2016年9月5日与成都恩多施生物工程技术有限公司签订《技术转让合同》,受让公司研发的头颈部肿瘤基因治疗药物EDS01(重组人内皮抑素腺病毒注射剂),该药物为四川大学副校长、生物治疗国家重点实验室主任、中国科学院魏于全院士团队的研究成果。目前已经完成Ⅰ期临床试验,正在开展Ⅱ期临床试验。所采用的重组腺病毒为独立自主构建,拥有自主知识产权。
头颈部肿瘤是我国常见疾病,约占全身恶性肿瘤的 19.9%-30.2%。患者就诊时 60%-70%已是晚期(Ⅲ-Ⅳ),五年生存率只有30%,局部复发率高(40%-60%)。目前,包括手术、放疗、化疗等综合治疗是晚期头颈部肿瘤常见的治疗模式,通常只能提高5%的五年总生存率,许多患者因治疗不佳最终死于肿瘤的复发与转移。
EDS01是将血管生成抑制因子----内皮抑素通过腺病毒导入体内,表达的内皮抑素可进入血液,通过血流循环扩散到远端,抑制远端肿瘤及转移灶;同时内皮抑素作用于肿瘤血管,而与肿瘤的类型无关,适用于绝大多数的恶性肿瘤治疗;而且,EDS01为复制缺陷型腺病毒,在被感染细胞内无法复制,不会扩散到环境中,不存在生物安全性方面的问题。EDS01 具有世界领先的技术,优势明显,有条件和可能成为世界上第一个通过抑制血管生长达到治疗恶性肿瘤目的的基因药物。
临床前研究表明:EDS01 对喉癌细胞 HEP2 和人鼻咽癌细胞 HNE 荷瘤裸鼠的肿瘤生长有抑制作用;对人肺腺癌细胞 SPC-A-1、A549 人非小细胞性肺腺癌细胞和小鼠 Lewis 肺癌细胞裸鼠皮下移植瘤具有明显的治疗效果,与化疗药物卡铂联用具有增强作用;安全性评价实验证实在恒河猴用量为人临床拟用剂量的 18 倍也是安全的。
I期临床研究单药剂量递增实验表明:肿瘤病人耐受良好,未出现剂量限制性毒性(DLT)和最大耐受剂量(MTD)。主要不良反应为发热和局部注射部位疼痛,并有流感样症状发生。多剂量给药,每周两次,连续两周瘤内注射方式治疗,同样安全、可耐受,但药物不良反应增加。单次或多次给药后均见到目标病灶初步疗效反应,多次给药的有效缓解率达 16.67%。
根据公告,本次技术转让费为5000万元人民币,其中:技术服务和指导费为根据实际情况另行书面协商确定后支付,不包含在以上技术转让费之内。 技术转让费按项目实施进度由甲方分三期支付给乙方或乙方指定的账户。
医谷+
合同主要内容
1、乙方转让甲方的技术内容如下:
(1)技术的范围:
① EDS01 申报新药的全部临床前研究资料,该资料内容包括但不限于制备工艺方法、工艺条件和工艺参数、产品质量标准、检测方法、药理等内容;
②国家食品药品监督管理总局(以下简称:CFDA)的临床研究批件(原件);
③Ⅰ期临床研究资料以及已开展Ⅱ期临床研究资料;
④现有的该产品已取得的相关专利。专利号:ZL200510021720.7;专利有效期:2025 年 9 月;
⑤乙方与第三方签订的与本项目后续开展事宜相关的合同;
⑥ 与后续技术开发实施相关的其它文件。
(2)技术指标和参数:成品质量符合已申报的质量标准(草案)。
2、甲方应以如下范围、方式和期限实施本项技术:
(1) 实施范围:生产治疗头颈部肿瘤的重组人内皮抑素腺病毒注射剂。
(2) 实施方式:组织完成Ⅱ期、Ⅲ期临床研究和申报新药并承担全部费用;生产、销售上述药物。
(3) 实施计划:
①签订合同后立即接受开展启动Ⅱ期临床研究;
②获得新药证书和生产批文后一年内生产该新药。
3、 乙方保证本项技术的真实性、合法性,并保证本项技术不侵犯任何第三人的合法权利,亦不存在任何权利瑕疵。如发生第三方指控甲方实施技术侵权成立的,乙方应当赔偿甲方全部损失(包括诉讼费、律师费、赔偿费等一切费用)并承担相关法律责任。
4、 为保证甲方有效实施本项技术,乙方应向甲方提供以下技术服务和技术指导:
(1) 技术服务和技术指导的内容:指导、帮助甲方生产场地建设并完成临床研究样品及三批中试产品;协助甲方开展Ⅱ、Ⅲ期临床研究,但所发生的全部费用和技术指导费用(另行书面协商确定)由甲方承担,双方应就技术指导的内容、方式及费用建议另行签订相关协议。
(2) 技术服务和技术指导的方式:现场指导和培训相关人员。 5、甲方向乙方支付受让该项技术的转让费(含知识产权转让费)及支付方式为:
(1) 技术转让费为:¥50,000,000.00 元(大写:人民币伍仟万元整)。其中:技术服务和指导费为根据实际情况另行书面协商确定后支付,不包含在以上技术转让费之内。
(2) 技术转让费按项目实施进度由甲方分三期支付给乙方或乙方指定的账户。
6、双方确定:
(1) 新药所有权归甲方,但乙方享有署名权、发明人申报权。科研成果排名乙方:1、3、5、7 名,甲方 2、4、6、8 名。
(2) 甲方有权利用乙方让与的技术进行后续改进,由此产生的具有实质性改变或创造性技术进步特征的新技术成果,归甲方所有。
(3) 乙方有权对让与甲方的技术进行后续改进(除治疗头颈部肿瘤),由此产生具有实质性改变或创造性技术进步特征的新技术成果,归乙方所有,但同等条件下甲方拥有优先受让权。
7、 本合同签订后,乙方不得在再将重组人内皮抑素腺病毒注射剂技术转让给他人,或许可第三人使用,否则,甲方有权单方解除本合同,乙方应当退回甲方已支付的转让费并向甲方支付合同总金额30%的违约金,该违约不足以弥补甲方所遭受损失的,乙方还应负责赔偿。
8、 双方确定:“EDS01”为暂定名,今后取得国家新药正式名称与其不一致的,不影响双方本合同权利义务。
来源:医谷网
为你推荐
 资讯
资讯 OpenAI 发布首款药物研发专用 AI 模型 GPT-Rosalind
不同于通用大模型,GPT-Rosalind 是 OpenAI 首个针对单一行业构建的前沿推理模型
2026-04-17 15:33
 资讯
资讯 创新泡沫剂型银屑病药物恩适达(卡泊三醇倍他米松泡沫剂)在华获批
是中国首个且目前唯一用于成人斑块状银屑病外用治疗的泡沫剂,专利的起泡装置可帮助患者轻松将药物均匀涂抹于皮肤,包括有毛发的部位。
2026-04-17 15:17
 资讯
资讯 安诺优达三闯港交所:NIPT 龙头转型 IVD 聚焦临床,亏损收窄仍承压
从强调 "一体化生命科学测序解决方案 ",转向 "聚焦临床 IVD、以营销拉动增长 ",并已开始剥离低毛利的检测服务业务,集中资源发展高附加值的 IVD 产品业务。
2026-04-17 12:43
 资讯
资讯 礼来口服小分子GLP-1RA药物orforglipron进一步证实其心血管及整体安全性
ACHIEVE-4: orforglipron迄今随访时间最长的3期研究显示可持续改善心血管代谢健康关键指标
2026-04-17 12:33
 资讯
资讯 国药控股原党委书记、董事长魏玉林以受贿罪判处有期徒刑12年
2026年4月14日,内蒙古自治区阿拉善左旗人民法院一审公开宣判国药控股股份有限公司原党委书记、董事长魏玉林受贿一案,对被告人魏玉林以受贿罪判处有期徒刑十二年,并处罚金人民...
2026-04-17 11:10
 资讯
资讯 国家中医药管理局原局长于文明被提起公诉
被告人于文明利用担任国家中医药管理局副局长职务上的便利以及职权或者地位形成的便利条件,为他人谋取利益,非法收受他人财物,数额特别巨大,依法应当以受贿罪追究其刑事责任。
2026-04-17 11:06
 资讯
资讯 黄果任国家药品监督管理局党组书记
2026年4月16日下午,中央组织部有关负责同志出席国家药品监督管理局领导干部会议,宣布中央决定:黄果同志任国家药品监督管理局党组书记,免去李利同志的国家药品监督管理局党组...
2026-04-16 22:10
 资讯
资讯 拜耳赫新诺(塞伐艾替尼片)治疗HER2突变非小细胞肺癌国内获批
用于治疗存在HER2(ERBB2)激活突变且既往接受过至少一种系统治疗的不可切除的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者
2026-04-16 18:27
 资讯
资讯 主动召回:一家药企的责任选择题
根据国家药监局发布的《药品召回管理办法》,持有人应当主动收集、记录药品的质量问题、药品不良反应 事件、其他安全风险信息,对可能存在的质量问题或者其他安全隐患进行调查...
2026-04-16 16:07
 资讯
资讯 《关于健全药品价格形成机制的若干意见》政策吹风会实录
所谓全周期就是根据药品上市后的不同环节,完善药品的价格政策,对于新上市的药品引入了药品首发价格机制,根据企业对临床价值和创新程度的自评结果,区分高水平创新药、改良新...
2026-04-16 14:18
 资讯
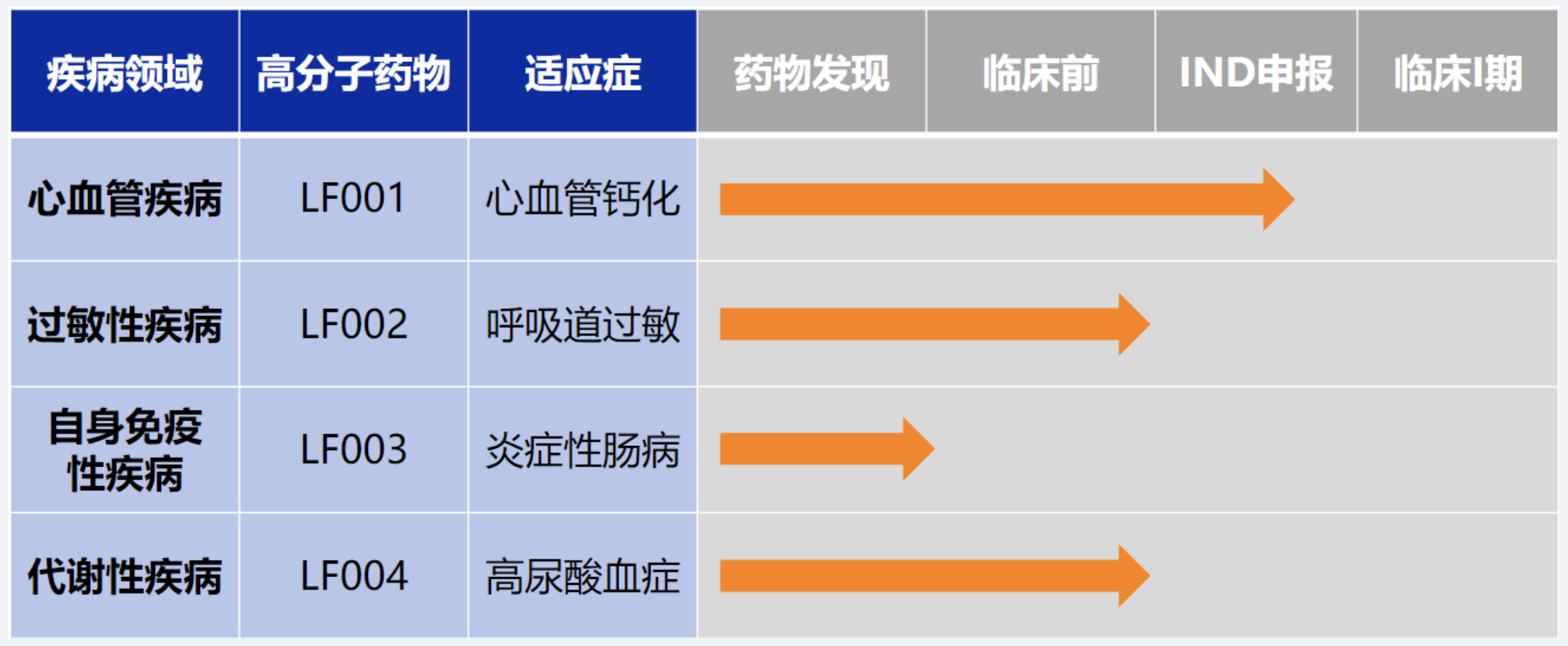
资讯 珞方生物获数千万种子轮融资,深耕高分子创新药开辟慢病治疗新路径
本轮融资由源来资本领投,飞镖创新种子基金跟投,募集资金将主要用于推进首个面向心血管钙化这一慢性疾病的高分子药物管线临床前研究与IND申报
2026-04-16 12:55
 资讯
资讯 创新药价格重磅文件,多部委将举办政策吹风会
4月14日,国办正式对外发布备受业内关注的《关于健全药品价格形成机制的若干意见》。该文件曾在去年2月份对外发布了征求意见稿,此后1年间,业内普遍关注该《意见》何时正式落地。
2026-04-14 22:37
 资讯
资讯 映恩生物拟登陆科创板,募资不超67.5亿元加码ADC研发
根据公告,映恩生物-B此次科创板IPO拟发行不超过1577 9190万股人民币股份,占发行后总股本的15%(不含超额配股权)
2026-04-14 19:26
 资讯
资讯 华东医药司美格鲁肽注射液减重适应症上市申请获受理,剑指GLP-1千亿蓝海
公司全资子公司杭州中美华东制药江东有限公司收到国家药品监督管理局(NMPA)签发的《受理通知书》,司美格鲁肽注射液上市许可申请获得受理,适用于在控制饮食和增加体力活动的...
2026-04-14 19:03
 资讯
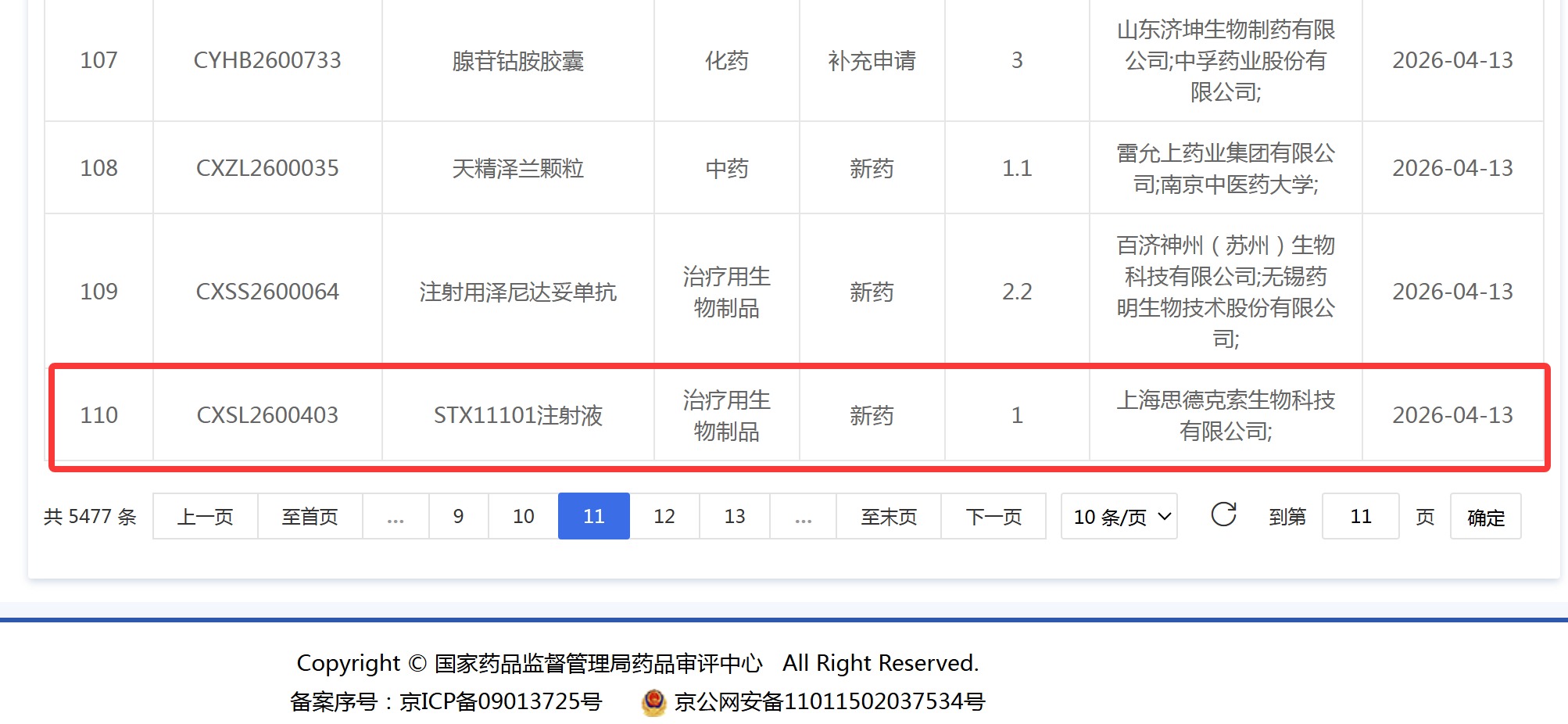
资讯 全国首款外泌体创新药申报IND
国家药监局药品审评中心(CDE)官网显示,4月13日,上海思德克索生物科技有限公司申报的STX11101注射液新药临床试验申请(IND)正式获得受理,受理号为CXSL2600403,药品类型为...
2026-04-14 18:11