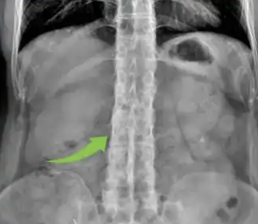
6月25日,强生公司宣布,旗下创新治疗药物泰立珂(特立妥单抗注射液)正式获得国家药品监督管理局(NMPA)批准,单药适用于既往至少接受过三线治疗(包括一种蛋白酶体抑制剂、一种免疫调节剂和一种抗CD38单克隆抗体)的复发或难治性多发性骨髓瘤(RRMM)成人患者 。 泰立珂是首个被批准用于治疗RRMM、靶向B细胞成熟抗原(BCMA)和CD3的双特异性抗体,此前已于美国和欧盟等国家或地区获批上市。
泰立珂是一款全球首创、即用型、基于体重给药的皮下注射双特异性抗体,可将CD3+ T细胞重定向到表达BCMA的骨髓瘤细胞,以诱导杀伤肿瘤细胞。经临床验证,泰立珂在既往至少接受过三线治疗的复发或难治性多发性骨髓瘤患者中的缓解率高,中国患者获益更佳,总缓解率(ORR)达76.9% 。
泰立珂是强生在中国获批的第四个用于治疗多发性骨髓瘤的产品,进一步丰富了其在多发性骨髓瘤和血液肿瘤治疗领域领先的产品组合,让更多患者能够有机会实现功能性治愈 。
多发性骨髓瘤在我国是血液肿瘤领域第二大常见恶性肿瘤。1990年至2019年间,该疾病的发病率增加了209%。作为一种高度异质性的血液肿瘤,几乎所有患者在治疗过程中都会面临复发或耐药。随着疾病的进展,患者复发次数越多,后续治疗难度越高,复发后的缓解深度也随之降低,持续缓解时间不断缩短 。因此,既往至少接受过三线治疗的复发或难治性多发性骨髓瘤患者迫切需要更有效的治疗选择 。
强生创新制药中国区总裁Cherry Huang女士表示:“强生专注于多发性骨髓瘤领域20年,始终致力于以高质量的创新解决方案满足不断增长的医疗健康需求,推动在业内建立新的治疗标准和规范,旨在让多发性骨髓瘤患者可以长期控制疾病进展,并有机会实现功能性治愈。作为全球首个获批用于治疗多发性骨髓瘤的双特异性抗体,泰立珂再次印证了强生在多发性骨髓瘤诊疗创新、改善患者获益方面的持续努力。未来,我们将继续聚焦于拥有重大未满足医疗需求的领域,以科学领拓医药未来,全力推动肿瘤全生命周期管理,确保我们的突破性成果能够帮助更多患者延长生命、改善生活质量。”
此次泰立珂获批是基于一项单臂、开放性、多中心研究(MajesTEC-1)结果,评估了特立妥单抗在复发或难治性多发性骨髓瘤患者中的安全性和有效性(n=165)。该研究包括既往接受过至少三线治疗(包括一种蛋白酶体抑制剂、一种免疫调节剂和一种抗CD38单克隆抗体)的患者2。研究结果显示,特立妥单抗总缓解率(ORR)达到63%(95%CI:55.2%,70.4%),46.1%的患者达到完全缓解(CR)或更好缓解(CR或严格的完全缓解[sCR])2。首次出现应答的中位时间为1.2个月(范围:0.1-5.5个月)。
值得注意的是,根据EHA最新公布的中位随访30.4个月的结果,中位缓解持续时间为24.0 (17.0-NE) 个月,在达到≥CR或更好缓解的患者中,中位缓解持续时间还未达到(26.7-NE) 。同时,泰立珂可显著降低患者疼痛症状,为复发/难治性多发性骨髓瘤患者带来持续和临床意义的改善 。
研究显示,特立妥单抗注射液的安全性总体可控。最常见的不良反应(≥20%)包括低丙种球蛋白血症、细胞因子释放综合征、中性粒细胞减少症、贫血、骨骼肌肉疼痛、淋巴细胞减少症、血小板减少症、上呼吸道感染、疲劳、注射部位反应、腹泻、感染性肺炎、白细胞减少症、COVID-19、恶心、发热、咳嗽、头痛、低钾血症、便秘和疼痛。
参考文献:
1.Pan D,Richter J.Teclistamab for Multiple Myeloma:Clinical Insights and Practical Considerations for a First-in-Class Bispecific Antibody.Cancer Manag Res.2023 Jul 21;15:741-751.doi:10.2147/CMAR.S372237.PMID:37497430;PMCID:PMC10368105.
2.特立妥单抗注射液说明书,2024年6月。
3.Padala SA et al.Epidemiology,Staging,and Management of Multiple Myeloma.Med Sci(Basel).2021;9(1):3.
4.EHA Library.Cai Z.06/13/2024;421483;PB2717
5.Landgren O,Kazandjian D.Modern Myeloma Therapy+Sustained Minimal Residual Disease-Negative=(Functional)Cure!.J Clin Oncol.2022;40(25):2863-2866.doi:10.1200/JCO.22.00622.
6.Chin Med J(Engl).2023 Dec 5;136(23):2834–2838.
7.Fonseca R,et al.BMC Cancer 2020;20:1087;
8.Yong K,et al.Br J Haematol 2016;175:252-264;
9van de Donk NWCJ,et al.Lancet.2021 Jan 30;397(10272):410-427.
10.Dimopoulos MA,Moreau P,Terpos E,et al.Multiple myeloma:EHA-ESMO clinical practice guidelines for diagnosis,treatment and follow-up.Ann Oncol.2021;32(3):309-322.doi:10.1016/j.annonc.2020.11.014.
11.EHA Library.Oriol A.06/13/2024;421006;P942
12.Martin TG,Moreau P,Usmani SZ,Garfall A,Mateos MV,San-Miguel JF,Oriol A,Nooka AK,Rosinol L,Chari A,Karlin L,Krishnan A,Bahlis N,Popat R,Besemer B,Martínez-López J,Delforge M,Trancucci D,Pei L,Kobos R,Fastenau J,Gries KS,van de Donk NWCJ.Teclistamab Improves Patient-Reported Symptoms and Health-Related Quality of Life in Relapsed or Refractory Multiple Myeloma:Results From the Phase II MajesTEC-1 Study.Clin Lymphoma Myeloma Leuk.2024 Mar;24(3):194-202.
来源:医谷网
为你推荐
 资讯
资讯 这家市值仅23亿的科创板上市公司要筹划控制权变更
5月7日晚间,仁度生物(688193 SH)发布公告于2026年5月8日(星期五)开市起停牌。停牌原因,公告显示为公司控股股东、实际控制人居金良正在筹划可能导致公司控制权发生变更的重大事项。
2026-05-09 10:30
 资讯
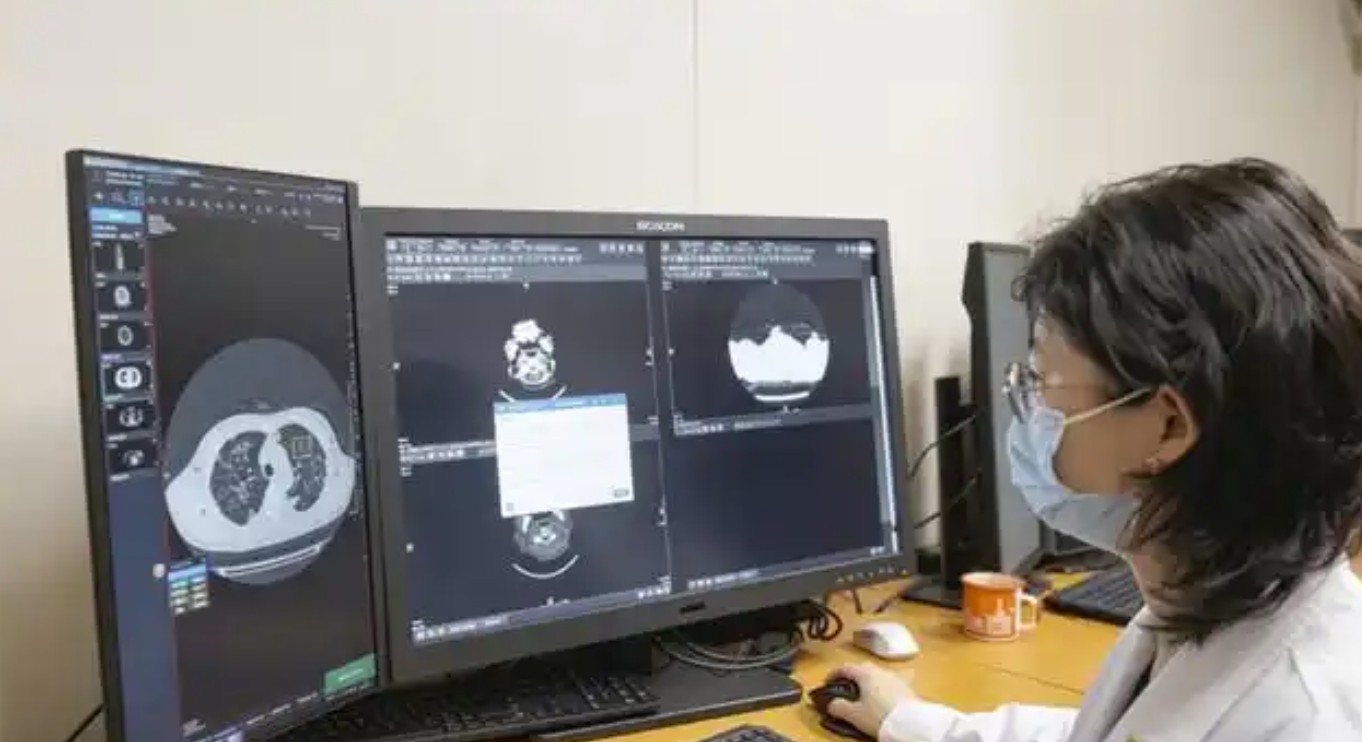
资讯 全国首款大模型多病种AI医疗产品进入国家药监局创新医疗器械特别审查程序
近日,国家人工智能应用中试基地(医疗领域)中试推广的智能应用——胸部CT图像辅助诊断软件,成功进入国家药监局创新医疗器械特别审查程序。这是全国首款进入该审查通道的大模...
2026-05-08 13:57
 资讯
资讯 国家集采,儿童专用药与成人用药将分组采购
5月7日,国家卫健委官网发布《关于改革完善儿童用药供应保障机制的实施意见》,明确提出在国家组织药品集中带量采购中,对儿童专用药与成人用药分组采购。
2026-05-08 11:19
 资讯
资讯 泽安生物完成3800万美元融资,加速推进“髓系细胞衔接器”免疫治疗管线
本轮融资由高瓴创投(GL Ventures)领投,一家国际主权财富基金大额跟投,博裕创投、五源资本、蓝驰创投等多家现有股东亦追加投资
2026-05-07 11:07
 资讯
资讯 拜耳asundexian(BAY 2433334片)用于降低缺血性卒中或短暂性脑缺血发作成人患者的卒中(复发)风险的注册申请获国家药品监督管理局药品审评中心受理
用于降低缺血性卒中或短暂性脑缺血发作(TIA)成人患者的 卒中(复发)风险,不包含心源性栓塞性卒中患者”的上市申请已获国家药品监督管理局药品审评中心受理。
2026-05-07 10:48
 资讯
资讯 全球首个CDK2/4/6抑制剂获批第二个适应症
5月6日,中国生物制药发布公告,下属企业正大天晴自主研发的库莫西利胶囊(商品名:赛坦欣)获得国家药品监督管理局批准,联合氟维司群用于激素受体(HR)阳性、人表皮生长因子...
2026-05-06 18:13
 资讯
资讯 蚂蚁阿福启动“健康中国体检关怀行动”,为1亿人免费解读体检报告
春季是传统的体检季,可很多人拿到体检报告却犯了难。一项5000名网友参与的调研显示,80%的受访者表示体检报告没有得到详细讲解,也不知道检后该怎么做;75%的受访者没有按体检...
2026-05-06 17:13
 资讯
资讯 第28个世界哮喘日:儿童哮喘早识别、规范治疗,守护患儿健康呼吸
进入5月,气温波动、花粉增多、呼吸道病毒活跃,哮喘也随之进入急性发作的高峰期。今年5月5日,恰逢第28个“世界哮喘日”——以“确保每位
2026-05-05 20:33
 资讯
资讯 康方生物授权的Summit美股大跌
2025年4月30日,美股上市公司Summit Therapeutics对外公布截至 2026 年 3 月 31 日第一季度财务业绩及业务进展,其中最受关注的无疑是从康方生物(09926 HK)获得授权的...
2026-05-05 20:02
 资讯
资讯 对比,生物医学新技术临床转化应用审批工作规范征求意见稿与正式稿有哪些不同?
4月30日,国家卫健委官网正式发布《生物医学新技术临床转化应用审批工作规范(试行)》,与4月19日发布的征求意见稿有哪些变化?
2026-05-05 10:58
 资讯
资讯 生物医学新技术与药品、医疗器械的界定
4月30日,国家卫健委官网发布《生物医学新技术与药品、医疗器械界定指导原则(暂行)》。对于生物医学新技术与药品、医疗器械的操作边界进行指导。
2026-05-05 10:51
 资讯
资讯 又一家药企被取消国家药品集采中选资格
4月30日,国家组织药品联合采购办公室发布公告,取消哈尔滨力强药业有限责任公司洛索洛芬钠凝胶贴膏中选资格并将该企业列入违规名单。
2026-04-30 15:19
 资讯
资讯 国家药监局原副局长陈时飞被判14年
4月29日,上海市第二中级人民法院一审公开宣判国家药品监督管理局原党组成员、副局长陈时飞受贿案,对被告人陈时飞以受贿罪判处有期徒刑14年,并处罚金人民币400万元;扣押在案...
2026-04-30 10:08
 资讯
资讯 微滔生物完成超 5000 万美元 A 轮、A + 轮融资,专注体内 CAR-T 细胞疗法赛道
本轮融资由正心谷资本与德诚资本分别领投,OrbiMed(奥博资本)、汉康资本、卫材创新风投基金、建发新兴投资等知名机构跟投,老股东启明创投、顺禧资本、杏泽资本持续加码
2026-04-29 13:21