日前,Nature旗下《信号转导与靶向治疗》( STTT)(SCI IF=52.7)在《中国创新药研发与监管支持现状》一文中,引用了中国首个抗艾滋病口服新药——江苏艾迪药业集团自主研发的艾诺韦林及其复方制剂艾诺米替(复邦德®)的全套临床研究[1]。
文中特别指出:“艾诺韦林及其复方制剂是国内首个自主研发的新型抗艾联合疗法,为患者提供了更多的治疗选择。这些药物因其在应对关键公共卫生需求方面的突破性作用而备受关注,并通过国家药监局的优先审评审批通道加速上市,使中国患者能更快地获得这些急需的治疗方案,提升了药物可及性。”
在艾诺韦林(艾邦德®)及复邦德®的临床开发进程中,多项严谨研究持续验证了其在代谢安全和持久病毒抑制方面的双重优势:
在神经安全性方面,RACER研究48周随访数据给出了明确答案[2]。研究显示,使用艾诺韦林治疗的患者,各类神经系统不良事件发生率仅为17.5%,远低于使用依非韦伦治疗组的54.1%。这一数据意味着,艾诺韦林能显著降低头晕、失眠等神经不适反应,让患者在长期服药过程中更舒适,也有助于提升服药依从性。
复邦德®在代谢安全上的表现同样亮眼。SPRINT研究48周结果表明[3],服用复邦德®的患者,血脂异常相关不良事件的发生率和严重程度均优于对照组。不仅出现血脂问题的比例更低,中重度血脂异常的情况也显著减少,能有效改善患者血脂状况,降低长期服药带来的心血管疾病风险,兼顾治疗效果与全身健康。
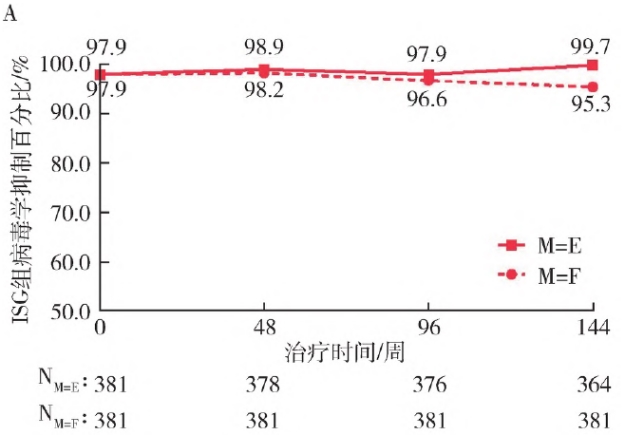
长期治疗的有效性与耐受性,更是复邦德®的核心竞争力之一。SPRINT研究的96周及144周[4-5]长期延伸数据进一步证实,复邦德®能实现持久稳定的病毒抑制,同时保持良好的耐受性,无明显长期不良反应。这为HIV感染者实现终身规范治疗、回归正常生活提供了有力保障。
0-144周ISG组(A)和DSG组(B)病毒学抑制百分比
从临床突破到国际认可,从药物上市到积累长期证据,复邦德®作为新一代抗艾复方制剂,有望持续领衔现在及未来的艾滋病抗病毒治疗之路,为更多患者带来长期治疗选择。
作为中国抗艾创新药研发龙头企业,艾迪药业积极响应“社会共治,守正创新,终结艾滋”的理念,始终以临床需求为核心,以科学实证为基石,推动中国抗艾创新走向世界前沿,致力于为最终实现“终结艾滋”的目标贡献中国力量。
参考文献:
[1] Tan R, Hua H, Zhou S, et al. Current landscape of innovative drug development and regulatory support in China. Sig Transduct Target Ther. 2025;10:220.
[2] Su B, Gao G, Wang M, et al. Efficacy and safety of ainuovirine versus efavirenz combination therapies with lamivudine/tenofovir disoproxil fumarate for medication of treatment-naïve HIV-1-positive adults: week 48 results of a randomized controlled phase 3 clinical trial followed by an open-label setting until week 96. Lancet Reg Health West Pac. 2023;36:100769.
[3] Zhang F, Wu H, Cai W, et al. Switch to fixed-dose ainuovirine, lamivudine, and tenofovir DF versus elvitegravir, cobicistat, emtricitabine, and tenofovir alafenamide in virologically suppressed people living with HIV-1: the 48-week results of the SPRINT trial, a multi-centre, randomised, double-blind, active-controlled, phase 3, non-inferiority trial. Lancet Reg Health West Pac. 2024;49:101143.
[4] Zhang F, Cai W, Wu H, et al. Immediate and delayed switches to tenofovir DF-containing, ainuovirine-based antiretroviral regimen: the SPRINT extensional study. BMC Med. 2025;23:524.
[5] 杨涤, 吴昊, 蔡卫平, 等. 基于真实世界数据的艾诺米替转换治疗HIV-1感染者144周有效性和安全性研究. 中国艾滋病性病. 2025;31(9):952-9.
来源:医谷网
为你推荐
 资讯
资讯 国家药监局原副局长陈时飞被判14年
4月29日,上海市第二中级人民法院一审公开宣判国家药品监督管理局原党组成员、副局长陈时飞受贿案,对被告人陈时飞以受贿罪判处有期徒刑14年,并处罚金人民币400万元;扣押在案...
2026-04-30 10:08
 资讯
资讯 微滔生物完成超 5000 万美元 A 轮、A + 轮融资,专注体内 CAR-T 细胞疗法赛道
本轮融资由正心谷资本与德诚资本分别领投,OrbiMed(奥博资本)、汉康资本、卫材创新风投基金、建发新兴投资等知名机构跟投,老股东启明创投、顺禧资本、杏泽资本持续加码
2026-04-29 13:21
 资讯
资讯 “A to H 18A第一股”诞生!迈威生物正式登陆香港联交所主板
2026年4月28日,迈威(上海)生物科技股份有限公司(以下简称“迈威生物”,A股代码:688062 SH,港股代码:02493 HK)在香港联合交易所主板正式挂牌上市,成为首家“A to H”的18A上市公司。
2026-04-28 19:22
 资讯
资讯 全面接轨国际,药物临床试验质量管理规范再升级
根据国家药监局发布的2025年第125号公告,自2026年3月31日后实施的药物临床试验,均适用《E6(R3):药物临床试验质量管理规范技术指导原则》(下称 ICH E6(R3))。
2026-04-28 19:13
 资讯
资讯 百济神州引入PD-1/CTLA-4/VEGF-A三抗
4月28日,百济神州发布公告称,2026年4 月 24 日,百济神州有限公司的全资子公司广州百济神州生物制药有限公司与华辉安健(北京)生物科技有限公司签订了一份《独家选择权、...
2026-04-28 09:49
 资讯
资讯 药品附条件批准上市申请审评审批工作程序
附条件批准时,每个附条件批准的适应症单独设置药品注册证书有效期,原则上,在确证性研究完成时限的基础上增加一年。确证性研究完成时限由药审中心在审评中与申请人沟通交流后...
2026-04-26 10:58
 资讯
资讯 CDE:抗体偶联药物首次申报临床试验药学资料撰写指导原则
本指导原则基于 ICH M4Q( R1)总体框架, 格式体例与之保持一致, 在其框架下结合抗体偶联药物的药学研究特点,细化了 IND 申报药学资料的撰写要求,旨在为该类药物 IN...
2026-04-25 21:39
 资讯
资讯 蚂蚁健康向医院开放“智慧医疗AI一体化方案” 支持智能体、云陪诊、本地化模型部署
4月25日,在2026中国医院信息网络大会(CHIMA 2026)上,蚂蚁健康面向全国医院及医疗机构推出“智慧医疗AI一体化方案”。
2026-04-25 20:09
 资讯
资讯 美敦力 5.5 亿美元收购 Scientia Vascular,加码神经血管赛道布局
Scientia Vascular 是专注于神经血管创新器械研发的新兴企业,核心产品管线聚焦颅内血管病变介入治疗领域
2026-04-25 15:50
 资讯
资讯 聚焦预防接种全龄升级,多方合力开展“成人全周期免疫促进暨带状疱疹公益科普”
4月25日,国家疾病预防控制局在上海举办主题宣传活动,呼吁“预防接种,苗助健康,全民行动”。
2026-04-25 15:41
 资讯
资讯 超亿元 A 轮融资!奥明星程以 AI4S 定义下一代生物智能基础设施
由深创投与复星医药(复健资本)联合领投,太平股权、广东中医药大健康基金、杭实集团等多家头部投资机构、产业链龙头企业及多地国资跟投。
2026-04-24 18:28
 资讯
资讯 Cytiva ÄKTA与Biacore系列产品实现本地生产, 以“桐庐样本”赋能生物医药“加速度”
依托桐庐生产基地,Cytiva持续提升本土供应能力,以更短的交付周期与定制化支持,精准匹配中国研发节奏,深度践行“在中国,为中国”承诺
2026-04-24 18:13
 资讯
资讯 全球首个治疗遗传性耳聋基因疗法获批
4 月 23 日,再生元宣布,美国 FDA 已经加速批准其在研基因疗法Otarmeni(lunsotogene parvec-cwha)上市,该药品成为首个也是目前唯一获批用于治疗遗传性听力损失的基因疗法。
2026-04-24 18:01
 资讯
资讯 CDE:治疗用重组蛋白药物首次申报临床试验药学资料撰写指导原则
本指导原则基于 ICH M4Q( R1)总体框架, 格式体例与之保持一致, 在其框架下结合治疗用重组蛋白药物的药学研究特点,细化了 IND 申报药学资料的撰写要求,旨在为该类药...
2026-04-24 12:44
 资讯
资讯 甘李药业GLP-1R博凡格鲁肽Ⅲ期临床试验完成首例受试者给药
4月23日,甘李药业发布公告,博凡格鲁肽(研发代号:GZR18)注射液正在中国开展的适应症成人肥胖患者的中度至重度阻塞性睡眠呼吸暂停(OSA)的Ⅲ期临床试验,于近日成功完成首例...
2026-04-24 10:25