批准药物数量创5年新低
2016年 (截止至2016年12月30日),一共有868个药物获美国食品药品监督管理局(FDA)批准上市,总体药品批准数量较往年有明显的减少,且新药批准数量也创下了5年最低点。然而批准的生物制剂数量却是历年之最。今年批准的NDA新药一共104个,其中包括了14个新分子实体药物(NME)。批准生物制品(BLA)12个,耐人寻味的是其中尽有3个生物仿制药,占据批准BLA药品数量的25%,已属井喷现象,这势必为全球生物制药市场带来了一场不小的腥风血雨。
图1数据来源:中国医药工业信息中心,中国新药研发监测数据库(CPM)
生物仿制药粉墨登场,将带动全球市场格局的变化
2016可谓生物仿制药元年,随着Sandoz生产的Zarxio(filgrastim-sndz)作为第一个生物仿制药获得FDA批准上市,生物仿制药于2015年开始正式走向美国这一最大的医药市场,并在今年呈现井喷态势,已有3个品种正式获得FDA批准上市,另有3个在等待审批的过程中。今年获批上市的3个生物仿制药分别是Remicade?(infliximab)的一种生物仿制药Inflectra,由美国辉瑞公司和韩国赛尔群公司(Celltrion)联合开发,于今年4月5日得到批准,成为第一个单克隆抗体生物仿制药,用于类风湿性关节炎、银屑病等炎症性疾病的治疗;Sandoz开发的Enbrel(etanercept)生物类似药Erelzi(etanercept-szzs),用于治疗多种炎症疾病,是FDA批准的第三个生物类似药;最后一个是安进公司生产的Amjevita(adalimumab-atto,阿达木单抗),可用于艾伯维品牌药Humira(修美乐,通用名:adalimumab,阿达木单抗)全部的适应症。去年,安进宣布正在开发9个重磅生物药的仿制药,并计划在2017年开始陆续将产品推向市场。安进表示,这些产品最终将带来超过30亿美元的年销售额。Amjevita便是其中一个!
这些生物仿制药的原研药品本身都是当年上市的重磅药物,曾创下极佳的销售业绩,随着这些生物仿制药的上市,必然会带动全球药品市场格局的变动,Remicade?(infliximab)的生物仿制药Inflectra就已经为Remicade?的销售带来了不小的冲击,去年同比下降了4%。而美国作为全球举足轻重的医药市场,他的生物仿制药审批政策可以为此类医药企业提供相当有用的参考价值,如生物等效性评价、专利规避、临床适应症等。
表1数据来源:中国医药工业信息中心,PDB药物综合数据库
FDA的新药审批工作卓效显著
FDA在今年的药品加速审批中取得卓效进展,突破疗法认定、优先审评、快速审批通道和罕用药地位等都是今年FDA加速审批的重要策略。根据CPM数据库统计显示,在今年的批准新药中,有32%(6个)药物获得突破性疗法认定,68%(13个)获得优先审评,37%(7个)获得罕用药地位,这为新药研发中创新药品的快速上市及罕用药的临床应用都带来了重要的意义。
新药批准热点领域集中,重磅药物层出不穷
2016年,从批准新药的治疗领域分布来看,神经系统用药、抗感染用药和抗肿瘤用药的批准数量名列前茅,占据总批准数量的50%以上。
2016年FDA批准新药的治疗领域分布情况
图2数据来源:中国医药工业信息中心,中国新药研发监测数据库(CPM)
其中值得一提的重磅药物有:
抗肿瘤药物Tecentriq,基因泰克(罗氏子公司)研发的用于治疗膀胱癌药物atezolizumab注射剂,是FDA批准的首个PD-1/PD-L1抑制剂。后又因其在肺癌患者的三期临床试验中疗效显着,于今年10月18日再次获得FDA批准新适应症,成为非小细胞肺癌治疗的重磅药物。
抗丙肝药物Zepatier,美国默克公司的格佐普韦-依巴司韦(Grazoprevir-Elbasvir)口服制剂,用于基因型1和4(GT-1,GT-4)慢性丙型肝炎病毒感染者治疗。是继吉利德Harvoni和艾伯维Viekira之后,获批上市的全球第三款突破性丙肝鸡尾酒疗法。
抗肿瘤药物Vencleta,艾伯维公司的治疗慢性淋巴细胞白血病药物venetoclax口服片剂,用于治疗染色体17p基因缺失的慢性淋巴白血病患者,是FDA批准的首个B细胞淋巴瘤-2(BCL-2)抑制剂。
抗帕金森病药物Nuplazid,美国生物制药公司Acadia Pharmaceuticals推出的首个获批用于治疗帕金森(PD)患者所经历幻觉和妄想等精神症状的药物。
软组织肉瘤新药Lartruvo,是40年以来首个治疗软组织肉瘤的突破性药物,与多柔比星联合治疗成人软组织肉瘤,由礼来研发生产,通过快速审评通道于今年10月19号被FDA批准上市。
来源:医药地理(微信号 pharmadl) 作者:江雯
为你推荐
 资讯
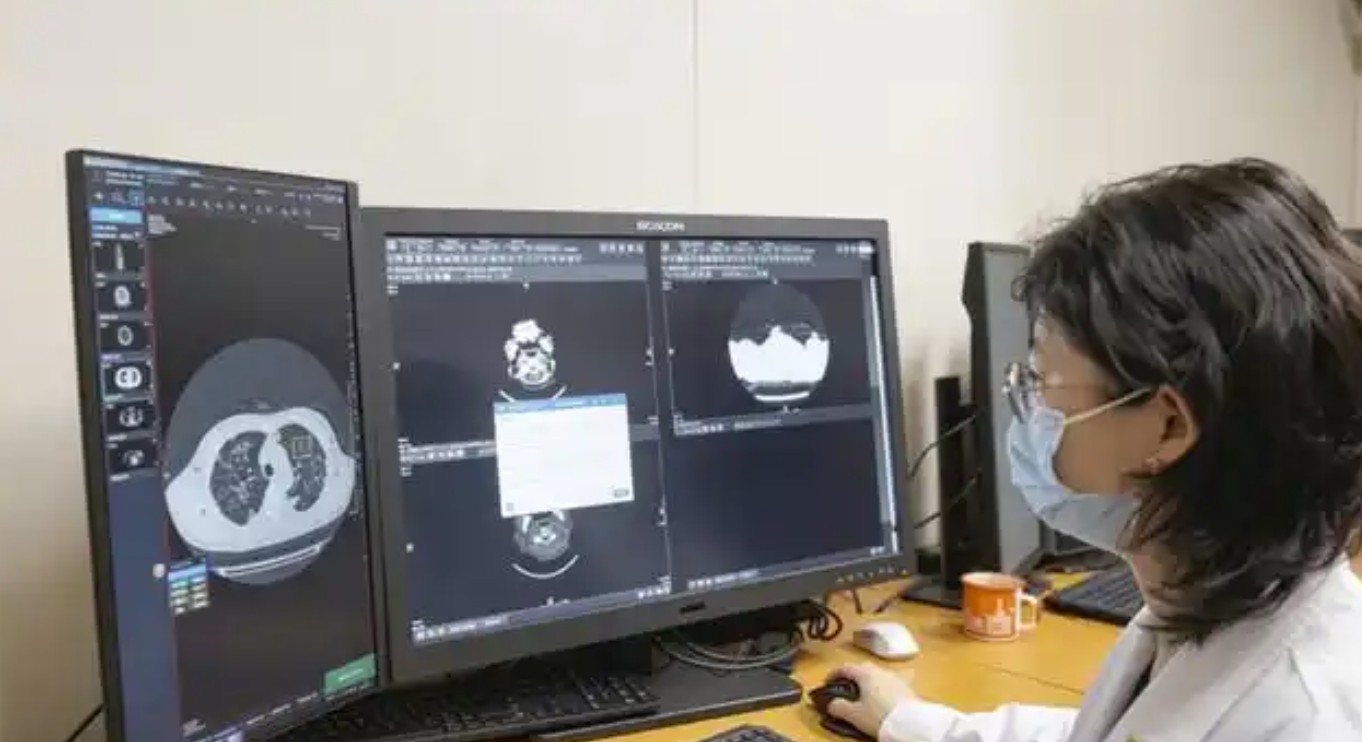
资讯 全国首款大模型多病种AI医疗产品进入国家药监局创新医疗器械特别审查程序
近日,国家人工智能应用中试基地(医疗领域)中试推广的智能应用——胸部CT图像辅助诊断软件,成功进入国家药监局创新医疗器械特别审查程序。这是全国首款进入该审查通道的大模...
2026-05-08 13:57
 资讯
资讯 国家集采,儿童专用药与成人用药将分组采购
5月7日,国家卫健委官网发布《关于改革完善儿童用药供应保障机制的实施意见》,明确提出在国家组织药品集中带量采购中,对儿童专用药与成人用药分组采购。
2026-05-08 11:19
 资讯
资讯 泽安生物完成3800万美元融资,加速推进“髓系细胞衔接器”免疫治疗管线
本轮融资由高瓴创投(GL Ventures)领投,一家国际主权财富基金大额跟投,博裕创投、五源资本、蓝驰创投等多家现有股东亦追加投资
2026-05-07 11:07
 资讯
资讯 拜耳asundexian(BAY 2433334片)用于降低缺血性卒中或短暂性脑缺血发作成人患者的卒中(复发)风险的注册申请获国家药品监督管理局药品审评中心受理
用于降低缺血性卒中或短暂性脑缺血发作(TIA)成人患者的 卒中(复发)风险,不包含心源性栓塞性卒中患者”的上市申请已获国家药品监督管理局药品审评中心受理。
2026-05-07 10:48
 资讯
资讯 全球首个CDK2/4/6抑制剂获批第二个适应症
5月6日,中国生物制药发布公告,下属企业正大天晴自主研发的库莫西利胶囊(商品名:赛坦欣)获得国家药品监督管理局批准,联合氟维司群用于激素受体(HR)阳性、人表皮生长因子...
2026-05-06 18:13
 资讯
资讯 蚂蚁阿福启动“健康中国体检关怀行动”,为1亿人免费解读体检报告
春季是传统的体检季,可很多人拿到体检报告却犯了难。一项5000名网友参与的调研显示,80%的受访者表示体检报告没有得到详细讲解,也不知道检后该怎么做;75%的受访者没有按体检...
2026-05-06 17:13
 资讯
资讯 第28个世界哮喘日:儿童哮喘早识别、规范治疗,守护患儿健康呼吸
进入5月,气温波动、花粉增多、呼吸道病毒活跃,哮喘也随之进入急性发作的高峰期。今年5月5日,恰逢第28个“世界哮喘日”——以“确保每位
2026-05-05 20:33
 资讯
资讯 康方生物授权的Summit美股大跌
2025年4月30日,美股上市公司Summit Therapeutics对外公布截至 2026 年 3 月 31 日第一季度财务业绩及业务进展,其中最受关注的无疑是从康方生物(09926 HK)获得授权的...
2026-05-05 20:02
 资讯
资讯 对比,生物医学新技术临床转化应用审批工作规范征求意见稿与正式稿有哪些不同?
4月30日,国家卫健委官网正式发布《生物医学新技术临床转化应用审批工作规范(试行)》,与4月19日发布的征求意见稿有哪些变化?
2026-05-05 10:58
 资讯
资讯 生物医学新技术与药品、医疗器械的界定
4月30日,国家卫健委官网发布《生物医学新技术与药品、医疗器械界定指导原则(暂行)》。对于生物医学新技术与药品、医疗器械的操作边界进行指导。
2026-05-05 10:51
 资讯
资讯 又一家药企被取消国家药品集采中选资格
4月30日,国家组织药品联合采购办公室发布公告,取消哈尔滨力强药业有限责任公司洛索洛芬钠凝胶贴膏中选资格并将该企业列入违规名单。
2026-04-30 15:19
 资讯
资讯 国家药监局原副局长陈时飞被判14年
4月29日,上海市第二中级人民法院一审公开宣判国家药品监督管理局原党组成员、副局长陈时飞受贿案,对被告人陈时飞以受贿罪判处有期徒刑14年,并处罚金人民币400万元;扣押在案...
2026-04-30 10:08
 资讯
资讯 微滔生物完成超 5000 万美元 A 轮、A + 轮融资,专注体内 CAR-T 细胞疗法赛道
本轮融资由正心谷资本与德诚资本分别领投,OrbiMed(奥博资本)、汉康资本、卫材创新风投基金、建发新兴投资等知名机构跟投,老股东启明创投、顺禧资本、杏泽资本持续加码
2026-04-29 13:21
 资讯
资讯 “A to H 18A第一股”诞生!迈威生物正式登陆香港联交所主板
2026年4月28日,迈威(上海)生物科技股份有限公司(以下简称“迈威生物”,A股代码:688062 SH,港股代码:02493 HK)在香港联合交易所主板正式挂牌上市,成为首家“A to H”的18A上市公司。
2026-04-28 19:22