1月18日,国家医保局公示了国家医保药品目录的结果,我们发现受到临床高度关注的德谷胰岛素利拉鲁肽注射液(Insulin Degludec/Liraglutide Injection, 简称IDegLira)进入《2022年国家基本医疗保险、工伤保险和生育保险药品目录》,2023年3月1日起正式执行。
早在2021 年 10 月,IDegLira在国家药品监督管理局(NMPA)获批,2022年3月正式上市。仅仅1年的时间,该药是凭借怎样的[硬核实力],顺利进入国家医保目录?
胰岛β细胞功能障碍和胰岛素抵抗是我国T2DM的主要发病根源
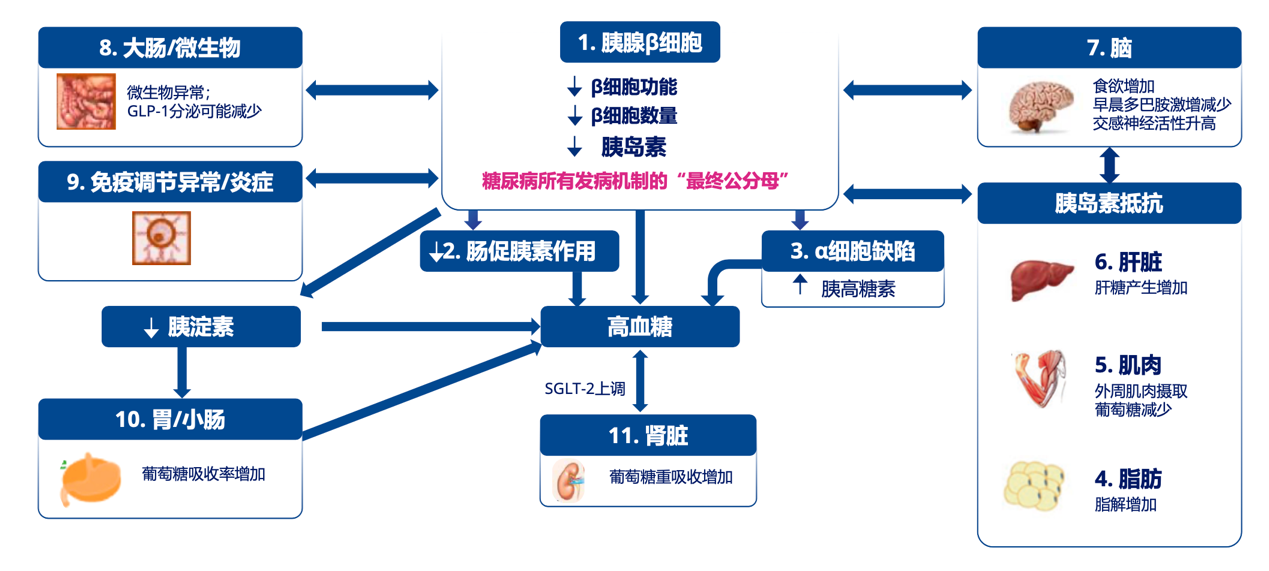
多年来,随着对2型糖尿病(T2DM)发病机制的不断探索,对T2DM的认识从胰岛β细胞功能缺陷所导致的胰岛素分泌减少(相对减少)与胰岛素调控葡萄糖代谢能力的下降(胰岛素抵抗,IR)的「二重性」,逐渐演变为胰岛β细胞分泌功能下降、IR、肝糖产生增加、脂肪细胞代谢紊乱,肠促胰岛素效应减弱,胰岛α细胞分泌胰高血糖素增加,肾脏葡萄糖重吸收增加,中枢神经系统功能障碍、大肠/微生物异常、免疫调节异常/炎症、胃/小肠葡萄糖吸收增加的「十一重奏」(图1)。
图1 T2DM 发病机制的[十一重奏]
既往研究表明,我国T2DM的发病机制主要为胰岛β细胞功能障碍。近期发表在Lancet Diabetes & Endocrinology的一项大型中国心脏代谢疾病和癌症队列研究,纳入94952例基线未合并糖尿病、年龄≥40岁的患者,评估IR、胰岛β细胞功能障碍及二者的交互作用对T2DM发生风险的影响。结果表明,大约 24.4% 的糖尿病归因于IR,12.4% 归因于胰岛β细胞功能障碍,研究者认为这可能和饮食的西方化相关。
因此,T2DM的治疗应强调针对IR和胰岛β细胞功能障碍的联合治疗。临床上,基础胰岛素和胰高血糖素样肽-1受体激动剂(GLP-1RA)日益成为联合治疗的选择。作为全球首个基础胰岛素与GLP-1RA的生物复方制剂,IDegLira更是为T2DM 患者有效控糖开辟了全新的治疗思路。让我们一起从作用机制、疗效证据等方面深入了解。
作用于双受体,实现机制互补、多靶调节
众所周知,不同肽类生物活性分子结合的复方制剂,对其稳定性要求很高。IDegLira是一种不同肽类活性分子结合的基础胰岛素 GLP-1RA 注射液,主要活性成分包含德谷胰岛素和利拉鲁肽,前者为长效基础胰岛素类似物,后者为长效 GLP-1RA类似物。通过独特的配方和工艺创新实现两种组分的稳定和共存,互不干扰。而且药代动力学特征与单独注射时相当,药效学特征也能够各自保持。
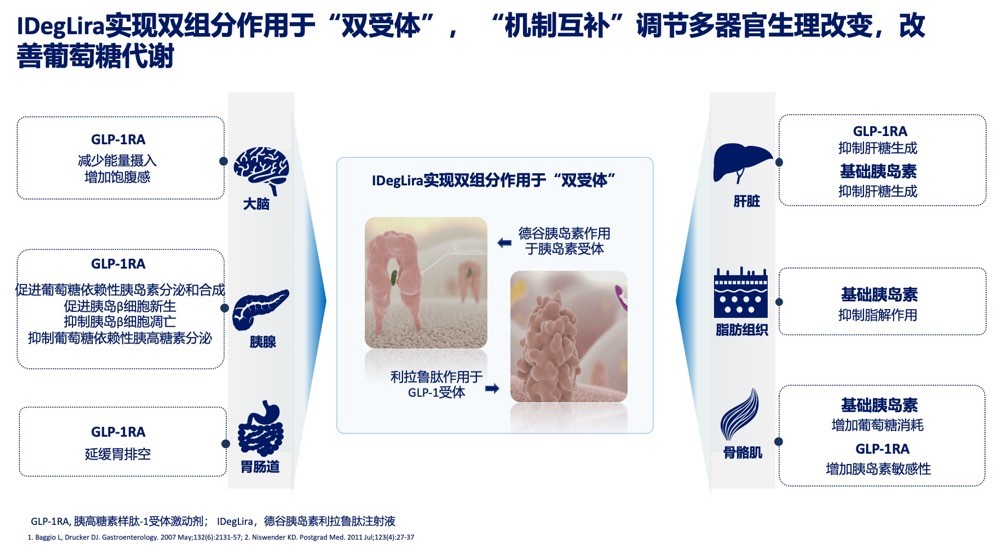
在IDegLira中,德谷胰岛素与利拉鲁肽通过[双受体机制]发挥协同、互补作用,同时作用于多个靶器官和组织。德谷胰岛素作用于肝脏、脂肪组织和骨骼肌等靶器官和组织的胰岛素受体,通过抑制肝糖生成、抑制脂解作用、增加葡萄糖消耗改善葡萄糖代谢;利拉鲁肽作用于大脑、胰腺、胃肠道等靶器官和组织的GLP-1受体,发挥葡萄糖浓度依赖性降糖、保护胰岛β细胞、延缓胃排空、增加胰岛素敏感性等代谢调节作用(图2)。
图2 IDegLira作用机制
三类人群增效减副,疗效屡获验证
在上市之初,IDegLira积累了丰富的循证证据,多项全球(DUAL I~IX系列研究)和中国(DUAL I、DUAL II研究)的3期临床试验均证实了其在不同类型T2DM 患者中的疗效和安全性。入组人群分别涵盖既往使用口服降糖药物(OAD)、GLP-1RA 、基础胰岛素治疗的 T2DM 患者。结果表明,使用IDegLira后,显著降低糖化血红蛋白(HbA1c)1.4%~2.0%,HbA1c 达标率(<7.0%)更高(最高达89.9%)。而且,与基础胰岛素相比,低血糖风险更低,并具有明显的体重获益;与GLP-1RA相比,胃肠道不良事件发生率更低。
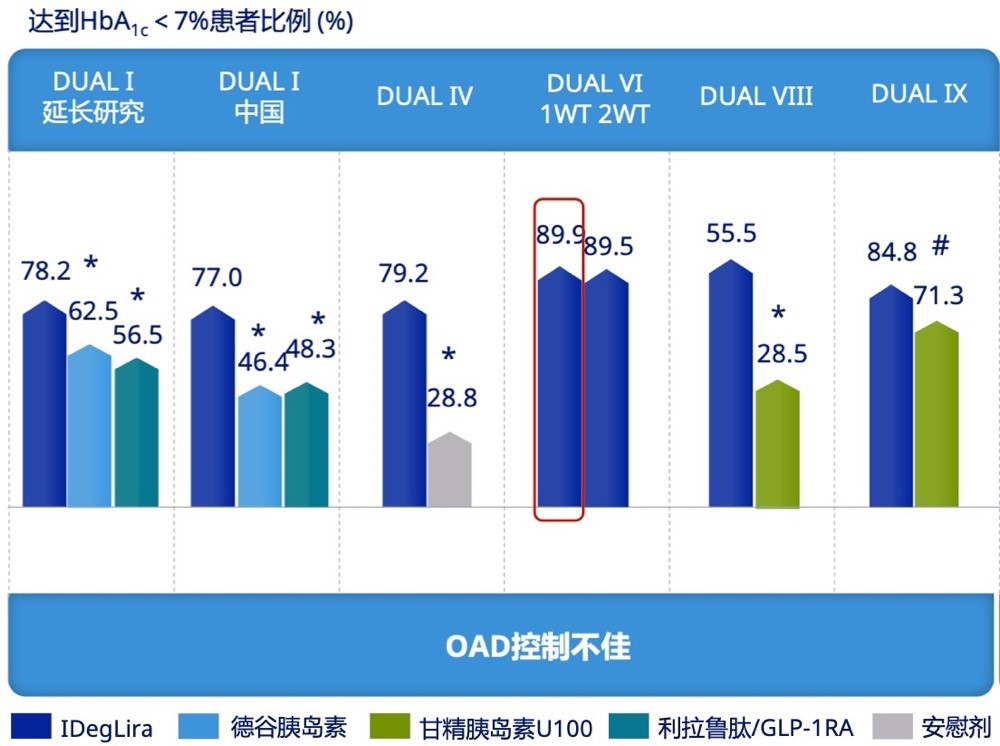
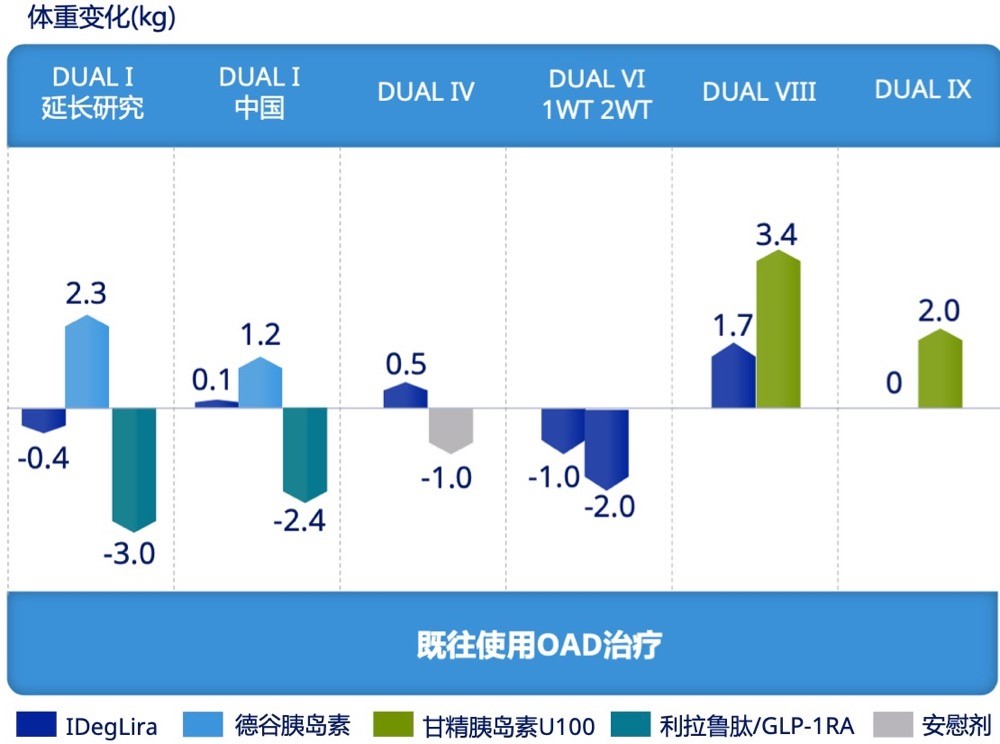
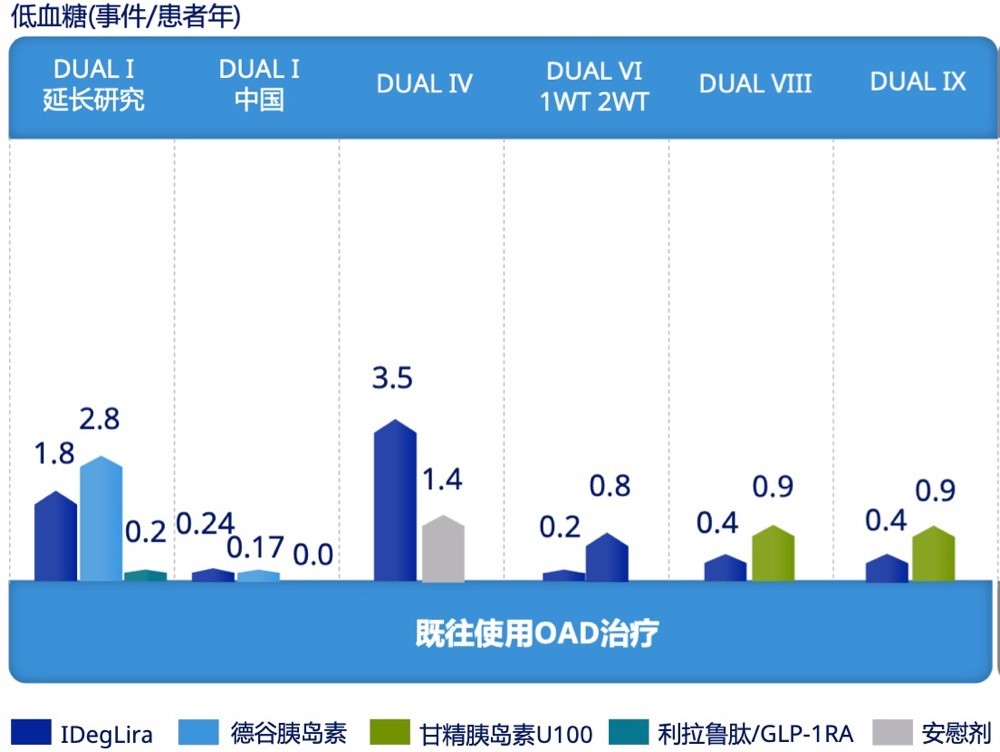
既往使用OAD控制不佳的T2DM患者:研究显示,在 OAD 治疗的基础上,使用IDegLira显著降低 T2DM 患者 HbA1c,HbA1c达标(<7.0%)的患者比例更高(55.5%~89.9%),缓解体重增加或体重减少(-1.0~1.7 kg),低血糖发生风险也更低(0.2~3.5事件/患者年)(图3)。
图 3 OAD控制不佳的T2DM 患者,使用IDegLira的HbA1c达标情况、体重变化、低血糖发生情况
同时,DUAL VIII 事后分析显示,治疗结束时IDegLira组葡萄糖目标范围内时间(dTIR) 更高(90% vs. 85%,估计治疗差异 5.17%,95% CI 2.07-8.27,P=0.0011)。
既往GLP-1 RA控制不佳的 T2DM 患者:DUAL III 研究表明11,在使用最大剂量 GLP-1RA血糖仍不达标的患者中,与使用 GLP-1RA 相比,换用IDegLira的T2DM 患者 HbA1c 进一步降低 0.94%(-1.3% vs.- 0.3%,95%CI[-1.11%,-0.78%],p<0.001),HbA1c<7% 的达标率更高(75% vs. 36%)。
既往基础胰岛素控制不佳的 T2DM 患者:DUAL V研究表明,在联合二甲双胍治疗的基础上,与甘精胰岛素 U100 相比,使用IDegLira的 T2DM 患者 HbA1c 下降更显著(−1.8% vs. −1.1%,P<0.001),体重下降更显著(–1.4 kg vs. 1.8 kg,P<0.001),确证性低血糖发生率更低(2.2事件/患者年 vs. 5.0事件/患者年,P<0.001)(图4)。事后分析显示,治疗结束时IDegLira组dTIR更高(84% vs. 79%,估计治疗差异 4.18%,95% CI 0.48-7.89,P=0.027)。
图4 DUAL V 研究结果
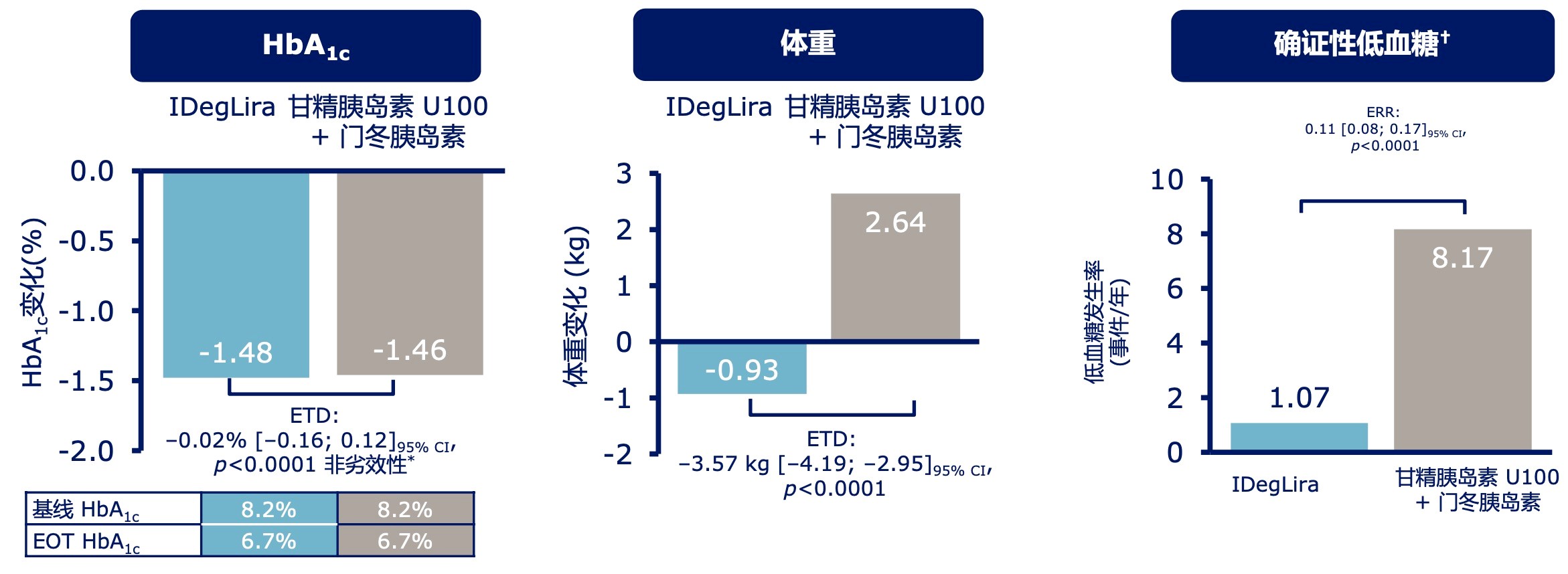
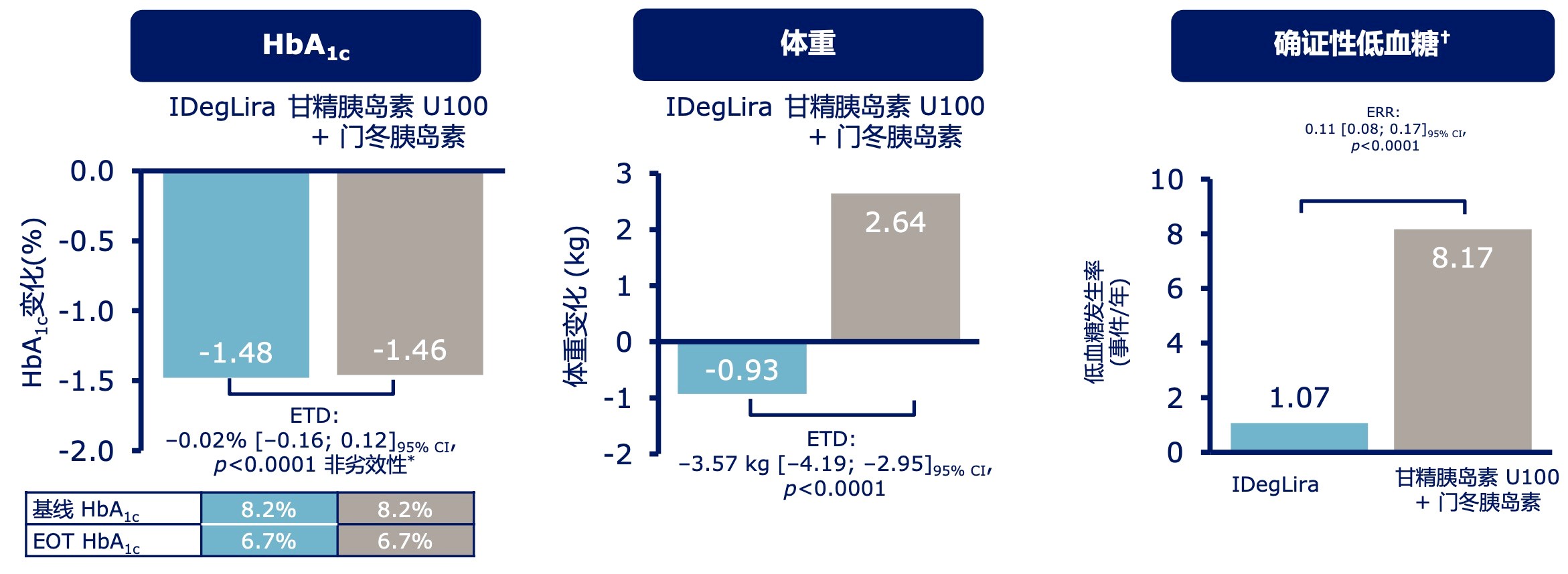
DUAL VII是在联合二甲双胍的基础上,比较IDegLira和基础-餐时治疗方案(甘精胰岛素U100+门冬胰岛素)的疗效。试验结束时,两组平均 HbA1c从基线时的 8.2% 降至 6.7%(P<0.0001)。与基础-餐时治疗方案相比,IDegLira组患者体重显著降低(-0.93kg vs. 2.64kg,P<0.0001)、确证性低血糖发生风险更低(1.07事件/患者年vs.8.17事件/患者年,P<0.0001)。
图5 DUAL VII研究结果
扩展临床使用场景,继续添加新证据
IDegLira的RCT研究已积累了大量循证医学证据。相关研究者持续关注和探索,不断扩展其在临床上的使用场景。
2022美国糖尿病学会(ADA)年会上公布的 HIGH 研究。在既往接受过基础胰岛素或多种 OAD 治疗仍血糖控制不佳(HbA1c≥9%-15%)的成人T2DM患者中,IDegLira与基础-餐时胰岛素治疗改善HbA1c疗效相似。然而,IDegLira治疗组低血糖(<70 mg/dl)发生率更低(22% vs. 36%,P=0.05)(图6),且有明显体重获益(-3.7±4.1 kg vs. +8.4±5.4 kg,P<0.01(图7)。
图6 IDegLira较基础-餐时胰岛素治疗低血糖风险更小
图7 IDegLira较基础-餐时胰岛素治疗体重获益更显著
2022 欧洲糖尿病研究协会(EASD)上公布的早期胰岛素强化治疗转换治疗研究。结果显示,在基础-餐时胰岛素转换为IDegLira治疗4个月后,HbA1c从12.3%±1.8%降至6.3%±0.9%(P<0.0001)(图8),体重从87.6±17.9 kg降至86.2±16.9 kg(P=0.299)。强化治疗期间,胰岛素平均日剂量为42.4±10.3 U,IDegLira治疗4个月后剂量为20.6±5.7剂量单位(对应的胰岛素剂量为德谷胰岛素20.6±5.7 U)。
图8 短期强化胰岛素治疗早期转换为IDegLira后,HbA1c显著下降
基于大量的循证医学证据,国内外多项指南均明确提出,基础胰岛素GLP-1RA 联合制剂可作为 T2DM 治疗新选择(表1)。
表1 国内外指南/共识对基础胰岛素GLP-1RA 联合制剂的推荐
小结
T2DM的发病机制涉及多器官和靶点。其中,胰岛β细胞功能障碍和IR是我国 T2DM发病的重要根源。因此,降糖治疗策略上应兼顾胰岛β细胞功能保护和改善IR,临床上基础胰岛素和GLP-1RA日益成为联合治疗的选择之一。
IDegLira同时作用于胰岛素受体和GLP-1RA受体,机制互补。大量研究证据显示IDegLira能有效改善T2DM患者血糖水平和TIR,提高血糖达标率,而且具有低血糖发生率低、体重获益明显等优势,受到国内外指南一致推荐。未来,相信IDegLira进入医保后,将惠及更多中国T2DM患者。
参考文献
1.Schwartz SS, Epstein S, Corkey BE, et al. The Time Is Right for a New Classification System for Diabetes: Rationale and Implications of the β-Cell-Centric Classification Schema. Diabetes Care, 2016, 39(2):179-86.
2.王天歌,陆洁莉,毕宇芳,等. 中国糖尿病持续攀升新解:中年肥胖相关胰岛素抵抗成为主要威胁. 中华内分泌代谢杂志, 2020, 36(03):198-200.
3.Saisho Y. An emerging new concept for the management of type 2 diabetes with a paradigm shift from the glucose-centric to beta cell-centric concept of diabetes - an Asian perspective. Expert Opin Pharmacother, 2020, 21(13):1565-1578..
4.母义明,胡蓓.新型糖尿病治疗药物:德谷胰岛素利拉鲁肽注射液. 临床药物治疗杂志, 2022, 20(06):16-20.
5.Kapitza C, Bode B, Ingwersen SH, et al. Preserved pharmacokinetic exposure and distinct glycemic effects of insulin degludec and liraglutide in IDegLira, a fixed-ratio combination therapy. J Clin Pharmacol, 2015, 55(12):1369-77.
6.Liu H, Luo B, Chen X, et al. Preserved pharmacokinetics and pharmacodynamics of insulin degludec and liraglutide when administered as insulin degludec/liraglutide in a Chinese population. J Diabetes Investig, 2022, 13(4):652-656..
7.Baggio LL, Drucker DJ. Biology of incretins: GLP-1 and GIP. Gastroenterology, 2007, 132(6):2131-57..
8.Niswender KD. Basal insulin: beyond glycemia. Postgrad Med, 2011, 123(4):27-37..
9.GOUGH S C, BODE B W, WOO V C, et al. One-year efficacy and safety of a fixed combination of insulin degludec and liraglutide in patients with type 2 diabetes: results of a 26-week extension to a 26-week main trial. Diabetes Obes Metab, 2015, 17(10): 965-73.
10.BUSE J B, VILSBøLL T, THURMAN J, et al. Contribution of liraglutide in the fixed-ratio combination of insulin degludec and liraglutide (IDegLira). Diabetes Care, 2014, 37(11): 2926-33.
11.LINJAWI S, BODE B W, CHAYKIN L B, et al. The Efficacy of IdegLira (Insulin Degludec/Liraglutide Combination) in Adults with Type 2 Diabetes Inadequately Controlled with a GLP-1 Receptor Agonist and Oral Therapy: DUAL III Randomized Clinical Trial. Diabetes Ther, 2017, 8(1): 101-14.
12.RODBARD H W, BODE B W, HARRIS S B, et al. Safety and efficacy of insulin degludec/liraglutide (IdegLira) added to sulphonylurea alone or to sulphonylurea and metformin in insulin-naïve people with Type 2 diabetes: the DUAL IV trial. Diabet Med, 2017, 34(2): 189-96.
13.LINGVAY I, PéREZ MANGHI F, GARCíA-HERNáNDEZ P, et al. Effect of Insulin Glargine Up-titration vs Insulin Degludec/Liraglutide on Glycated Hemoglobin Levels in Patients With Uncontrolled Type 2 Diabetes: The DUAL V Randomized Clinical Trial. Jama, 2016, 315(9): 898-907.
14.Presented at ADA 2021, 606-P.
15.HARRIS S B, KOCSIS G, PRAGER R, et al. Safety and efficacy of IdegLira titrated once weekly versus twice weekly in patients with type 2 diabetes uncontrolled on oral antidiabetic drugs: DUAL VI randomized clinical trial. Diabetes Obes Metab, 2017, 19(6): 858-65.
16.BILLINGS L K, DOSHI A, GOUET D, et al. Efficacy and Safety of IdegLira Versus Basal-Bolus Insulin Therapy in Patients With Type 2 Diabetes Uncontrolled on Metformin and Basal Insulin: The DUAL VII Randomized Clinical Trial . Diabetes Care, 2018, 41(5): 1009-16.
17.ARODA V R, GONZáLEZ-GALVEZ G, GRøN R, et al. Durability of insulin degludec plus liraglutide versus insulin glargine U100 as initial injectable therapy in type 2 diabetes (DUAL VIII): a multicentre, open-label, phase 3b, ontrolled controlled trial. Lancet Diabetes Endocrinol, 2019, 7(8): 596-605.
18.PHILIS-TSIMIKAS A, BILLINGS L K, BUSCH R, et al. Superior efficacy of insulin degludec/liraglutide versus insulin glargine U100 as add-on to sodium-glucose co-transporter-2 inhibitor therapy: A randomized clinical trial in people with uncontrolled type 2 diabetes. Diabetes Obes Metab, 2019, 21(6): 1399-408.
19.NORDISK N. Cover Page for Statistical Analysis Plan Sponsor name: Novo Nordisk AS NCT number NCT03172494 Sponsor trial ID: NN9068-4148 Official title of study: A trial comparing the efficacy and safety of insulin degludec/liraglutide, insulin degludec, and liraglutide in Chinese subjects with type 2 diabetes inadequately controlled on oral antidiabetic drugs (OADs) [Z]. 2020
20.PEI Y, AGNER B R, LUO B, et al. DUAL II China: Superior HbA1c reductions and weight loss with insulin degludec/liraglutide (IdegLira) versus insulin degludec in a randomized trial of Chinese people with type 2 diabetes inadequately controlled on basal insulin. Diabetes Obes Metab, 2021, 23(12): 2687-96.
21.Rodolfo J. Galindo, et al. A randomized controlled trial comparing the safety and efficacy of IdegLira versus basal bolus in patients with poorly ontrolled type 2 diabetes and very high HbA1c (≥9~15%): IdegLira HIGH trial. Presented at ADA2022 meeting. 217-OR.
22.Taybani Z, et al. Early e-escalation with IdegLira in patients with type 2 diabetes using short-term intensive insulin therapy to correct severe hyperglycaemia. Presented at EASD2022 meeting. SO55-690A.
23.ADA. Pharmacologic Approaches to Glycemic Treatment: Standards of Medical Care in Diabetes-2023. Diabetes Care, 2022, 46:S140-S157..
24.Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycaemia in type 2 diabetes, 2022. A consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetologia, 2022, 65(12):1925-1966.
25.中华医学会糖尿病学分会. 中国2型糖尿病防治指南(2020). 中华糖尿病杂志, 2021, 13(4):315-408.
26.《2型糖尿病短期胰岛素强化治疗专家共识》编写委员会. 2型糖尿病短期胰岛素强化治疗专家共识(2021年版). 中华糖尿病杂志, 2022, 14(1) : 21-31.
来源:医谷网
为你推荐
 资讯
资讯 药明生物不超4亿美元回购股份
5月26日,药明生物发布公告称,公司于二零二六年五月二十四日,其已议决动用购回授权,以及(如适用)股东于本公司股东大会上批准以购回股份的任何未来一般授权,以不时在公开市...
2026-05-26 15:15
 资讯
资讯 君实生物收到关于销售费用等的问询函
近日,上海君实生物医药科技股份有限公司收到上海证券交易所下发的《关于上海君实生物医药科技股份有限公司2025年年度报告的信息披露监管问询函》(上证科创公函【2026】0121号)。
2026-05-26 13:40
 资讯
资讯 不得人工智能审方,国家药监局发布《处方药网络零售合规指南》
今日,国家药监局综合司印发《处方药网络零售合规指南》,《指南》对售药商家、售药行为和电商平台及网页展示细节做出了更明确规范的要求,同时针对目前网络售药存在的不凭处方...
2026-05-25 15:38
 资讯
资讯 CRO百诚医药停牌,谋划控股权转让
5月24日晚间,百诚医药发布公告,,公司于近日收到公司控股股东、实际控制人邵春能、楼金芳的通知,控股股东、实际控制人邵春能、楼金芳及其一致行动人正在筹划涉及公司控制权变...
2026-05-25 13:53
 资讯
资讯 罗伯医疗完成数千万元 B + 轮融资,加速全球消化内镜手术机器人商业化进程
本次融资资金将主要用于核心产品 EndoFaster®(速易必)消化内镜手术机器人的全国临床落地、下一代产品 EndoDreams 的研发、智能化生产基地建设与供应链优化,以及国际市场...
2026-05-25 12:14
 资讯
资讯 对上海医保支付集采药品新政的解读
近期,上海市医保局发布的 《关于优化第十一批国家组织集采药品医保支付协同的通知》 (沪医保医管发〔2026〕12号),相关政策的变化引起业内广泛关注。目前该政策已于2026年5...
2026-05-25 11:45
 资讯
资讯 云顶新耀年销超14亿的当家花旦迎来新的挑战者
5月21日晚间,石药集团发布公告宣布,其开发的布地奈德肠溶胶囊(4mg)已获得国家药品监督管理局颁发的药品注册批件,用于治疗具有疾病进展风险的原发性免疫球蛋白A肾病成人患者...
2026-05-24 22:38
 资讯
资讯 5月20日起,提交注册申请的品种按照《M13A:口服固体速释制剂的生物等效性》执行
自本公告发布之日起,提交注册申请的品种均适用M13A指导原则(含问答文件)。对于已按照既往临床试验方案和统计分析计划开展生物等效性试验,并在本公告发布之日起12个月内申报...
2026-05-23 11:56
 资讯
资讯 呋喹替尼联合疗法获批晚期肾细胞癌患者二线治疗新适应症
5月21日,和黄医药宣布,其自主研发创新药物呋喹替尼获得中国国家药品监督管理局(NMPA)批准,联合信迪利单抗用于治疗既往接受血管内皮生长因子受体酪氨酸激酶抑制剂(VEGFR-...
2026-05-22 15:56
 资讯
资讯 刚果(金)与乌干达埃博拉疫情:国际SOS发布企业员工支持建议
近日,世界卫生组织(WHO)宣布,当前影响刚果民主共和国和乌干达的埃博拉疫情构成“国际关注的突发公共卫生事件”(PHEIC)。
2026-05-22 13:47
 资讯
资讯 早筛 戒烟 筑牢膀胱癌第一道防线
每年的5月是“膀胱关爱月”,根据国家癌症中心发布的《2024年全国癌症报告》显示,膀胱癌位居我国恶性肿瘤发病第 11 位。2022年中国膀胱癌发病率为7 3 10万人,死亡率为4...
文/刘思 2026-05-22 13:31
 资讯
资讯 再鼎医药总裁兼首席运营官离职
5月22日早间,再鼎医药发布公告称,公司董事会已于5月18日决定,Josh Smiley不再担任公司总裁兼首席运营官,相关决定自当日起生效,其在公司的最后任职日期为5月22日。
2026-05-22 11:45
 资讯
资讯 共建多元支付,加速创新可及:镁信健康与辉瑞中国达成战略合作
双方将依托长期合作基础,以多元支付为基石,以数据洞察和AI技术为引擎,加速前沿创新药落地中国,全方位提升患者用药可及性与健康服务体验,助力构建多层次医疗保障体系。
2026-05-21 17:57
 资讯
资讯 拜耳可申达(非奈利酮片)在中国获批用于LVEF≥40%的心力衰竭成人患者
拜耳宣布中国国家药品监督管理局(NMPA)批准高选择性非甾体类盐皮质激素受体拮抗剂可申达(非奈利酮片)用于射血分数(LVEF)≥40%的心力衰竭成人患者,以降低心血管死亡、因心...
2026-05-21 17:51
 资讯
资讯 冯慧宇教授:从“活下去”到“活得好”,重症肌无力迈入精准治疗时代
作为深耕重症肌无力领域数十年的临床专家,她用一个个真实的患者故事,揭示了这个有着 300 多年历史的古老疾病在当代诊疗中的核心痛点,并分享了对创新药发展和患者全程管理的...
文/张蓉蓉 2026-05-21 15:48
 资讯
资讯 2026年“家庭健康促进计划-健康同行1+1公益项目” 在西安医学院正式启动
5月18日,由中国妇女发展基金会主办,陕西省妇联、陕西妇女儿童发展基金会、西安医学院协办,默沙东公益支持的“家庭健康促进计划-健康同行1+1公益项目西安高校健康跑暨2026启动...
2026-05-21 15:37
 资讯
资讯 爱尔眼科补交税款及滞纳金5.24亿元
5月20日,爱尔眼科(300015 SZ)发布公告称,其根据国家税收法律法规相关要求进行自查后,需补缴税款3 48亿元,并支付滞纳金1 76亿元,合计金额达5 24亿元。目前,上述税款...
2026-05-21 15:36