生物类似药明显降低患者负担,同时助力生命科学创新惠及更多人群,具有特别的意义!
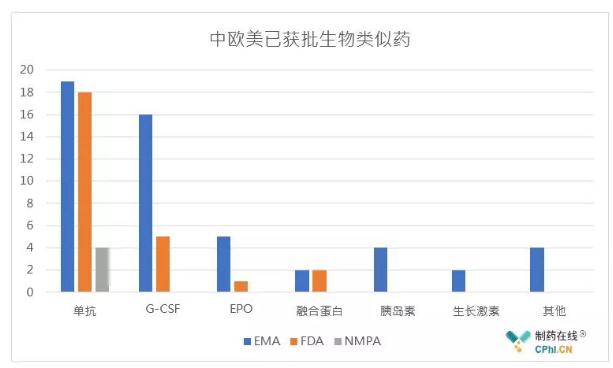
中欧美等国家地区看,欧盟是生物类似药时代的先行者!2006年04月11日,EMA便批准首款生物类似药,即生长激素Omnitrope (somatropin),截止目前,EMA已批准53款生物类似药获批,2款生物类似药上市申请被驳回,其中包括19款单抗,16款G-CSF类,5款EPO,2款融合蛋白 (依那西普)。
2015年03月06日,非格司亭Zarxio (filgrastim-sndz) 美国获批,揭开美国生物类似药序幕。FDA已批准27款生物类似药上市,其中单抗18款,融合蛋白 (依那西普) 2款,G-CSF类5款,EPO类1款。
2019年02月22日,中国首款按照生物类似药标准申报的汉利康获批并成功商业化,这意味着中国生物类似药时代正式开启。截至目前,已有4款生物类似药中国获批,均为单克隆抗体,目前均已经商业化。
数据源自EMA & FDA & NMPA
欧盟地区生物类似药数量按照通用名计算,包含部分主动撤回产品;
中国未计算依那西普
全球多个超级重磅炸弹级别药物专利到期,本文希望立足中欧美生物类似药审评审批的差异,简单对比各个国家和地区生物类似药的可及性。考虑到中欧美生物类似药审评政策差异,本文仅涉及单抗、 G-CSF类、依那西普。
一.欧盟乃生物类似药先行者
在生物类似药审评审批上,欧盟起步早于FDA近 10年,早于中国近15年,是一个先行者!
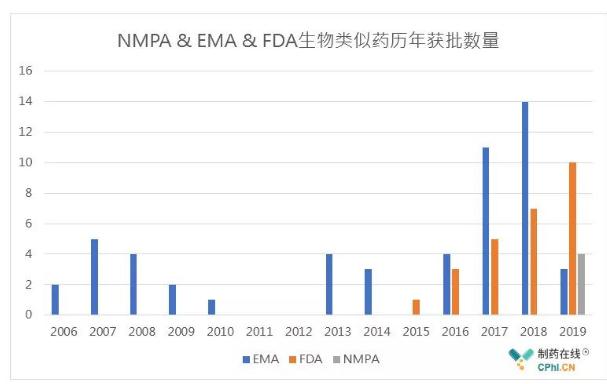
2006年04月11日,生长激素Omnitrope (somatropin)的生物类似药便获批,中欧美历年获批上市的生物类似药数量上看:
数据源自NMPA & EMA & FDA;
欧盟地区生物类似药数量按照通用名计算,包含部分主动撤回产品。
中国未计算依那西普
1. 从首款生物类似药获批看,FDA的生物类似药时代迟到了近10年, NMPA迟到了近15年;
2. 2018年成为欧盟生物类似药审评审批的一个转折点,达到一个高峰,当年批准14款生物类似药上市;
3. 2015年起,FDA生物类似药审评审批逐年稳步增加,2019年达到一个新的高峰,全年批准10款生物类似药;
4. 2019年,中国生物类似药元年,4款单抗获批上市,并快速商业化;
5. 撇开审评审批政策的差异,仅从单克隆抗体、融合蛋白、G-CSF类产品看,全球超级重磅炸弹级别药物(单抗+融合蛋白)的生物类似药欧美获批已经基本持平。
二.单克隆抗体、融合蛋白、G-CSF类生物类似药欧美对比
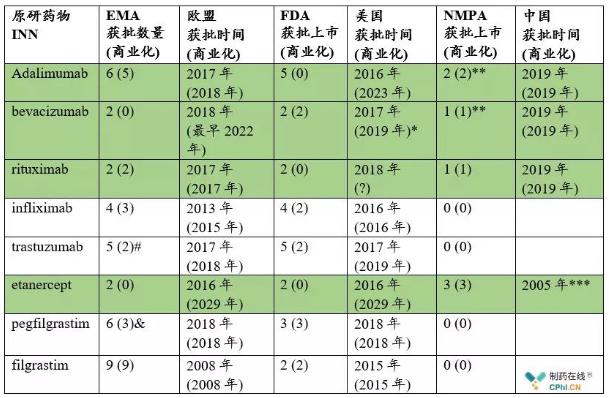
笔者根据公开信息,整理了中欧美单克隆抗体、融合蛋白、G-CSF类生物类似药获批上市以及商业化的状态,从各自获批数量、商业化数量,最早的获批时间和商业化时间对比了可及性。
中欧美主要生物类似药可及性对比
2019年12月31日正式商业化;#Ogivri, Trazimera, Kanjinti是否商业化尚不清楚; &Fulphila, Udenyca, Grasustek是否商业化不清楚;**公布挂网价格,便认为是商业化。Boehringer Ingelheim开发的生物类似药Cyltezo已在欧盟获批上市,但是已放弃欧盟市场,专注美国市场,预期于2023年07月01日美国商业化;***依那西普并非是按照生物类似药标准申报上市的类似药。
部分生物类似药的商业化状态未知,从目前情况看:
1. 单克隆抗体、融合蛋白、G-CSF类生物类似药总量看,欧盟36款,美国25款,中国4款;成功商业化比例70%,美国44%,中国100%;
2. 单克隆抗体、融合蛋白、G-CSF类生物类似药可及性看,除阿达木单抗和依那西普外,欧美均已有至少一个生物类似药商业化;
3. 中国在依那西普、阿达木单抗的可及性上,做得最好,益赛普国内获批比原研药物都要早;
4. 中国生物类似药数量虽然尚少,但是商业化速度相当快,可及性并未迟到很久。
5. 2020年,中国首款曲妥珠单抗生物类似药将会获批,预计也将很快商业化
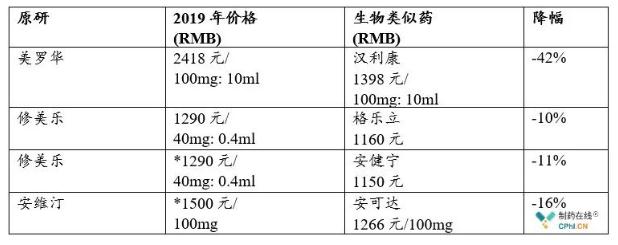
最后,从最近公开的挂网价格看,生物类似药的可及大大降低患者负担,例如安健宁和安可达,相比2019年原研药物医药谈判价格,继续降10-16%!
生物类似药,让创新惠及更多患者,意义重大!
中国生物类似药原研药物和生物类似药价格
*2019医保谈判价格
来源:CPhI制药在线 作者:1°C
为你推荐
 资讯
资讯 不得人工智能审方,国家药监局发布《处方药网络零售合规指南》
今日,国家药监局综合司印发《处方药网络零售合规指南》,《指南》对售药商家、售药行为和电商平台及网页展示细节做出了更明确规范的要求,同时针对目前网络售药存在的不凭处方...
2026-05-25 15:38
 资讯
资讯 CRO百诚医药停牌,谋划控股权转让
5月24日晚间,百诚医药发布公告,,公司于近日收到公司控股股东、实际控制人邵春能、楼金芳的通知,控股股东、实际控制人邵春能、楼金芳及其一致行动人正在筹划涉及公司控制权变...
2026-05-25 13:53
 资讯
资讯 罗伯医疗完成数千万元 B + 轮融资,加速全球消化内镜手术机器人商业化进程
本次融资资金将主要用于核心产品 EndoFaster®(速易必)消化内镜手术机器人的全国临床落地、下一代产品 EndoDreams 的研发、智能化生产基地建设与供应链优化,以及国际市场...
2026-05-25 12:14
 资讯
资讯 对上海医保支付集采药品新政的解读
近期,上海市医保局发布的 《关于优化第十一批国家组织集采药品医保支付协同的通知》 (沪医保医管发〔2026〕12号),相关政策的变化引起业内广泛关注。目前该政策已于2026年5...
2026-05-25 11:45
 资讯
资讯 云顶新耀年销超14亿的当家花旦迎来新的挑战者
5月21日晚间,石药集团发布公告宣布,其开发的布地奈德肠溶胶囊(4mg)已获得国家药品监督管理局颁发的药品注册批件,用于治疗具有疾病进展风险的原发性免疫球蛋白A肾病成人患者...
2026-05-24 22:38
 资讯
资讯 5月20日起,提交注册申请的品种按照《M13A:口服固体速释制剂的生物等效性》执行
自本公告发布之日起,提交注册申请的品种均适用M13A指导原则(含问答文件)。对于已按照既往临床试验方案和统计分析计划开展生物等效性试验,并在本公告发布之日起12个月内申报...
2026-05-23 11:56
 资讯
资讯 呋喹替尼联合疗法获批晚期肾细胞癌患者二线治疗新适应症
5月21日,和黄医药宣布,其自主研发创新药物呋喹替尼获得中国国家药品监督管理局(NMPA)批准,联合信迪利单抗用于治疗既往接受血管内皮生长因子受体酪氨酸激酶抑制剂(VEGFR-...
2026-05-22 15:56
 资讯
资讯 刚果(金)与乌干达埃博拉疫情:国际SOS发布企业员工支持建议
近日,世界卫生组织(WHO)宣布,当前影响刚果民主共和国和乌干达的埃博拉疫情构成“国际关注的突发公共卫生事件”(PHEIC)。
2026-05-22 13:47
 资讯
资讯 早筛 戒烟 筑牢膀胱癌第一道防线
每年的5月是“膀胱关爱月”,根据国家癌症中心发布的《2024年全国癌症报告》显示,膀胱癌位居我国恶性肿瘤发病第 11 位。2022年中国膀胱癌发病率为7 3 10万人,死亡率为4...
文/刘思 2026-05-22 13:31
 资讯
资讯 再鼎医药总裁兼首席运营官离职
5月22日早间,再鼎医药发布公告称,公司董事会已于5月18日决定,Josh Smiley不再担任公司总裁兼首席运营官,相关决定自当日起生效,其在公司的最后任职日期为5月22日。
2026-05-22 11:45
 资讯
资讯 共建多元支付,加速创新可及:镁信健康与辉瑞中国达成战略合作
双方将依托长期合作基础,以多元支付为基石,以数据洞察和AI技术为引擎,加速前沿创新药落地中国,全方位提升患者用药可及性与健康服务体验,助力构建多层次医疗保障体系。
2026-05-21 17:57
 资讯
资讯 拜耳可申达(非奈利酮片)在中国获批用于LVEF≥40%的心力衰竭成人患者
拜耳宣布中国国家药品监督管理局(NMPA)批准高选择性非甾体类盐皮质激素受体拮抗剂可申达(非奈利酮片)用于射血分数(LVEF)≥40%的心力衰竭成人患者,以降低心血管死亡、因心...
2026-05-21 17:51
 资讯
资讯 冯慧宇教授:从“活下去”到“活得好”,重症肌无力迈入精准治疗时代
作为深耕重症肌无力领域数十年的临床专家,她用一个个真实的患者故事,揭示了这个有着 300 多年历史的古老疾病在当代诊疗中的核心痛点,并分享了对创新药发展和患者全程管理的...
文/张蓉蓉 2026-05-21 15:48
 资讯
资讯 2026年“家庭健康促进计划-健康同行1+1公益项目” 在西安医学院正式启动
5月18日,由中国妇女发展基金会主办,陕西省妇联、陕西妇女儿童发展基金会、西安医学院协办,默沙东公益支持的“家庭健康促进计划-健康同行1+1公益项目西安高校健康跑暨2026启动...
2026-05-21 15:37
 资讯
资讯 爱尔眼科补交税款及滞纳金5.24亿元
5月20日,爱尔眼科(300015 SZ)发布公告称,其根据国家税收法律法规相关要求进行自查后,需补缴税款3 48亿元,并支付滞纳金1 76亿元,合计金额达5 24亿元。目前,上述税款...
2026-05-21 15:36
 资讯
资讯 复宏汉霖引进第三代口服EGFR-TKI产品
近日,复宏汉霖宣布与江苏正大丰海制药有限公司及其旗下江苏创特医药科技有限公司达成战略合作。根据约定,复宏汉霖将获得由江苏创特自主研发的口服小分子三代表皮生长因子受体...
2026-05-21 11:28
 资讯
资讯 冠脉支架国家集采第二轮接续采购在天津开标,27个产品拟中选
5月20日,国家组织冠脉支架集中带量采购第二轮接续采购在天津开标。共15家企业的30个产品参与投标,投标企业全部中选,27个产品获拟中选资格。
2026-05-20 21:05