2017年12月24日,Eisai和Biogen宣布旗下阿尔茨海默病(AD)候选药物,抗β淀粉样原纤维抗体BAN2401在12个月的二期临床试验中,未能达到主要终点。虽然研究者表示会继续完成18个月的观察,但大家心里都明白,又一款新药倒在了AD面前。
这不是失败的开始,也远不是结束。
2018年1月,辉瑞宣布裁撤整个神经退行性疾病药物研发管线,彻底放弃了AD这个天坑;2月,Merck的BACE抑制剂verubecestat三期临床试验提前宣告失败;5月,强生的BACE抑制剂atabecestat因严重的副作用中止试验;6月,礼来与阿斯利康合作的同类药物lanabecestat同样止步三期。
靶向β淀粉样蛋白药物屡屡失败,研究者们不禁怀疑,这个理论,真的站得住脚吗?
或许我们需要的只是再坚持一下!
7月初,Eisai与Biogen宣布对BAN2401二期临床数据进行了重新分析,当治疗延长至18个月,最高剂量组患者与安慰剂组相比,认知衰退速度明显放缓,脑内β淀粉样蛋白“由阳转阴”!本周三的阿尔茨海默病协会国际会议(AAIC 2018)上,两家企业公布了正式的数据,高剂量组中81%患者β淀粉样蛋白水平显着下降,认知表现下降放缓30%[1]!
能够看到Aβ药物表现如此优秀,真想大呼一声有生之年!
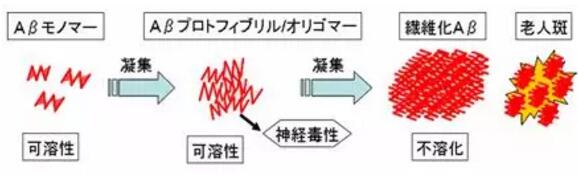
BAN2401是一种抗β淀粉样原纤维抗体,它可以有选择地结合脑内可溶性的Aβ原纤维,将其中和或清除,防止损伤神经以及形成β淀粉样蛋白沉淀。
本次二期临床试验共纳入了865名患者,分为6个剂量组,最高剂量组每隔双周接受10mg/kg剂量的BAN2401注射,还有1组是安慰剂组[6]。研究采用PET扫描检测患者脑内β淀粉样蛋白水平,Adcoms综合认知测试测定患者认知。
鉴于Adcoms是一种新开发的、针对早期患者较轻的认知和功能障碍的评估量表[2],这也是它首次应用于临床试验,因此也有学者质疑,所谓的“认知衰退速度减缓30%”,到底在临床上是什么意义呢,似乎很难评估。
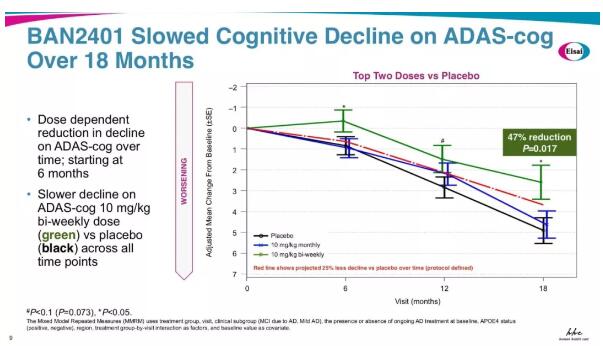
研究者也采用其他量表对患者认知水平进行了评估。在临床试验更加常用的阿尔茨海默病评估量表-认知子量表(ADAS-Cog)中,与安慰剂组(n=247)相比,采用10mg/kg剂量、每隔双周注射的高剂量组(n=161)患者表现出了47%的认知衰退减缓,其实数据要比Adcoms更漂亮。不过在临床痴呆评分(CDR)中,高剂量组也表现出了26%的下降,但是数据无统计学意义。[3]
从数据来看,治疗进行到第6个月,患者的认知衰退即有好转,但是在第18个月才会表现出统计学差异。
ADAS-Cog分析:高剂量组(绿)认知衰退明显放缓[3]
对患者脑部进行的PET扫描提供了更有力的证据。所有参与者在试验开始时都存在脑内β淀粉样蛋白斑块,18个月后81%高剂量组患者斑块基本消失,斑块平均减少达到70%,最高能够达到93%[4]!
Eisai首席医学官Lynn Kramer认为,采用PET技术也是试验成功的原因之一。较早的研究发现,许多参与者在试验开始时脑内并不存在β淀粉样蛋白斑块,自然也不涉及清除的问题了[5]。
在靶向β淀粉样蛋白沉淀的药物中,常见名为淀粉样蛋白相关影像异常(ARIA)的副作用,可能引起脑水肿或出血,停药即可解决。早期的安全性实验表明,BAN2401耐受性良好,副作用发生率比其他治疗方法要更低。高剂量组中16%的患者因ARIA中止治疗,安慰剂组则为6%。在所有参与者中,副作用的发生率不足10%。
Kramer声称,“48例ARIA中,只有5例有MRI可以检测的症状,其中只有2例表现出了外在的疾病表征。”[5]
这也带来了另一个问题。具有APOE4突变的AD患者,发生ARIA的几率更高,因此一家监管机构曾要求研究者将APOE4+患者移出高剂量组,随机分配到其他组别。
众所周知,APOE4患者病情发展更加迅速,这或许会对研究结果带来一些影响。
阿尔茨海默病协会首席科学馆Maria Carrillo表示,我们应当对这项研究保持“谨慎乐观”。
不过不管怎么说,在二期临床上同时实现减缓认知衰退和清除β淀粉样蛋白的候选药物,BAN2401还是第一个。此外,Biogen还持有另一款备受期待的新药aducanumab,一种β淀粉样蛋白沉淀的单克隆抗体。该药的两项大型三期临床预计2021年结束。
月初公布BAN2401可减缓早期AD患者疾病进展后,Biogen股价一天之内上涨19.6%,是14年来最大涨幅;Eisai则在两天内飙升40%[6]。
目前Eisai和Biogen已经在着手与FDA沟通,准备为BAN2401申请快速审批通道。
期待很快能有新药面世,患者们已经等得太久了。
参考资料:
[1]https://www.nytimes.com/2018/07/25/health/alzheimers-dementia-drug-treatment.html?rref=collection%2Fsectioncollection%2Fhealth
[2] https://www.ncbi.nlm.nih.gov/pubmed/27010616
[3]https://endpts.com/eisai-biogen-outline-an-impressive-30-and-47-advantage-for-their-alzheimers-drug-ban2401/
[4]https://www.cnbc.com/2018/07/25/biogen-and-eisai-unveil-ban2401-alzheimers-disease-trial-results.html
[5]https://www.cnn.com/2018/07/25/health/alzheimers-dementia-drug-ban2401-biogen-eisai-study/index.html
https://apnews.com/601edc06c69247828f4ef25c2b18a5f8/Hopes-rise-again-for-a-drug-to-slow-Alzheimer's-disease
[6]https://www.clinicaltrials.gov/ct2/show/NCT01767311?term=BAN2401&rank=2
来源:奇点网
作者:奇点糕
来源:奇点网 作者:奇点糕
为你推荐
 资讯
资讯 恒瑞医药与BMS达成总交易额可达约152亿美元的战略与许可合作
本次合作协议共包含 4 项恒瑞肿瘤学及血液学项目、4 项 BMS 免疫学项目,以及双方依托恒瑞研发引擎与多元创新技术平台共同研发的 5 项创新项目,值得注意的是,这13在研...
2026-05-12 13:40
 资讯
资讯 徐和平教授荣膺国际视觉与眼科研究协会(ARVO)金质会士(FARVO Gold)荣誉称号
近日,国际视觉与眼科研究协会(The Association for Research in Vision and Ophthalmology, ARVO)在美国丹佛召开的2026年年会上正式公布了本年度金质会士(ARVO Gold Fellow,FARVO)评选结果。
2026-05-12 13:35
 资讯
资讯 中国生物技术发展中心:细胞组分及衍生物治疗新技术临床研究备案指引(第1版)
本指引适用于在我国境内开展的非以药品注册为目的的细胞组分及衍生物治疗新技术临床研究,本指引所指的细胞组分及衍生物治疗新技术不依赖完整活细胞,是指利用人自体或异体干细...
2026-05-12 10:05
 资讯
资讯 迈瑞遭证监会监管六问
5月8日,中国证监会对外公布最新一期《境外发行上市备案补充材料要求》(2026年4月27日—2026年5月8日),国际司共对7家企业出具补充材料要求,其中包括已于2025年11月10日向港交...
2026-05-10 19:21
 资讯
资讯 复星医药至多10.15亿元取得两款FAK抑制剂中国大陆区域独家商业化权利
5月8日,应世生物宣布与复星医药达成战略合作。根据协议约定,应世生物将授予复星医药其自主开发的两款创新 FAK 抑制剂IN10018(Ifebemtinib)、IN10028在中国(不含港澳台地...
2026-05-09 16:14
 资讯
资讯 河南省药监局局长正接受纪律审查和监察调查
据河南省纪委监委消息:河南省市场监督管理局党组成员,省药品监督管理局党组书记、局长田文才涉嫌严重违纪违法,目前正接受河南省纪委监委纪律审查和监察调查。
2026-05-09 12:55
 资讯
资讯 这家市值仅23亿的科创板上市公司要筹划控制权变更
5月7日晚间,仁度生物(688193 SH)发布公告于2026年5月8日(星期五)开市起停牌。停牌原因,公告显示为公司控股股东、实际控制人居金良正在筹划可能导致公司控制权发生变更的重大事项。
2026-05-09 10:30
 资讯
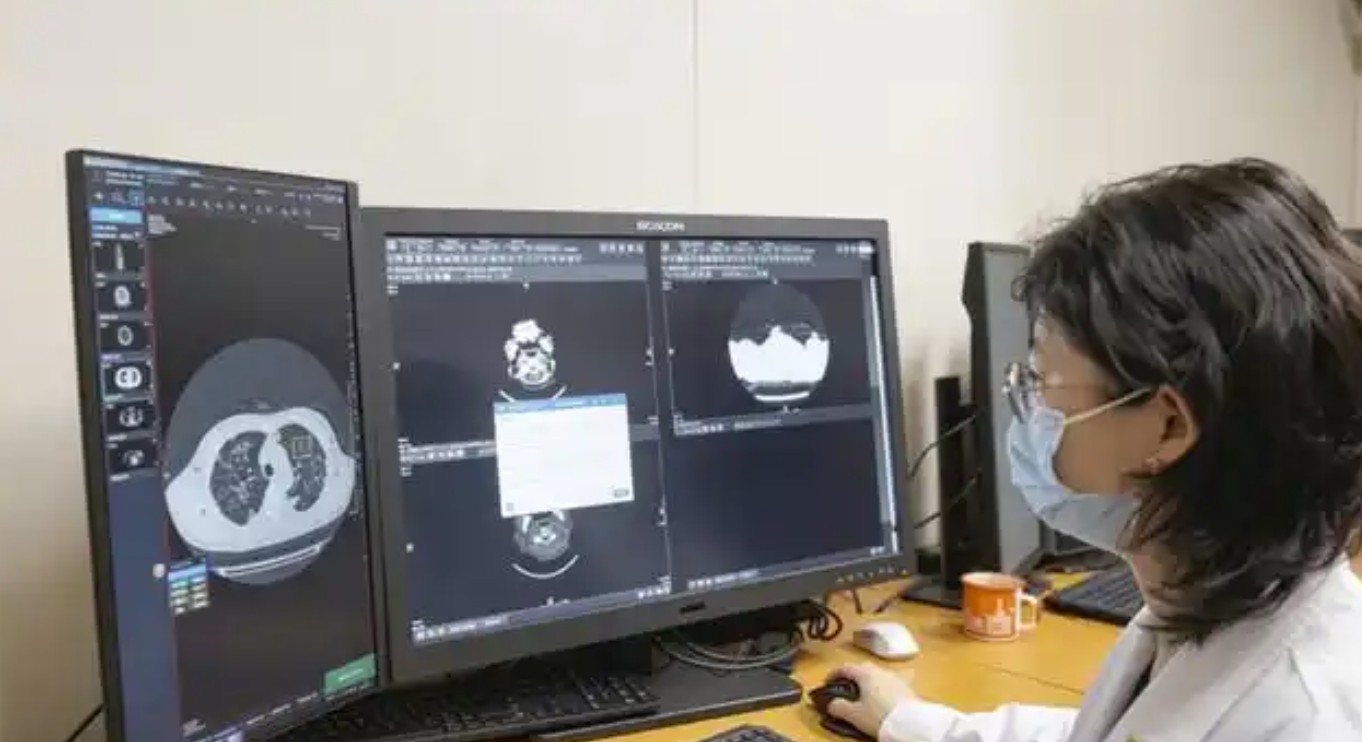
资讯 全国首款大模型多病种AI医疗产品进入国家药监局创新医疗器械特别审查程序
近日,国家人工智能应用中试基地(医疗领域)中试推广的智能应用——胸部CT图像辅助诊断软件,成功进入国家药监局创新医疗器械特别审查程序。这是全国首款进入该审查通道的大模...
2026-05-08 13:57
 资讯
资讯 国家集采,儿童专用药与成人用药将分组采购
5月7日,国家卫健委官网发布《关于改革完善儿童用药供应保障机制的实施意见》,明确提出在国家组织药品集中带量采购中,对儿童专用药与成人用药分组采购。
2026-05-08 11:19
 资讯
资讯 泽安生物完成3800万美元融资,加速推进“髓系细胞衔接器”免疫治疗管线
本轮融资由高瓴创投(GL Ventures)领投,一家国际主权财富基金大额跟投,博裕创投、五源资本、蓝驰创投等多家现有股东亦追加投资
2026-05-07 11:07
 资讯
资讯 拜耳asundexian(BAY 2433334片)用于降低缺血性卒中或短暂性脑缺血发作成人患者的卒中(复发)风险的注册申请获国家药品监督管理局药品审评中心受理
用于降低缺血性卒中或短暂性脑缺血发作(TIA)成人患者的 卒中(复发)风险,不包含心源性栓塞性卒中患者”的上市申请已获国家药品监督管理局药品审评中心受理。
2026-05-07 10:48
 资讯
资讯 全球首个CDK2/4/6抑制剂获批第二个适应症
5月6日,中国生物制药发布公告,下属企业正大天晴自主研发的库莫西利胶囊(商品名:赛坦欣)获得国家药品监督管理局批准,联合氟维司群用于激素受体(HR)阳性、人表皮生长因子...
2026-05-06 18:13